解题方法
1 . 下列离子方程式书写正确的是
| A.Na与水反应:Na+2H2O=Na++2OH-+H2↑ |
B.过量NaOH溶液与NH4HCO3溶液反应:HC +OH-=H2O+C +OH-=H2O+C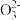 |
| C.FeO溶于稀硝酸:FeO+2H+=Fe2++H2O |
| D.向AgNO3溶液中滴加过量氨水:Ag++2NH3·H2O=[Ag(NH3)2]++2H2O |
您最近一年使用:0次
2 . 按要求回答下列问题:
(1)实验室制备氨气,下列方法中可以选用的是_______ 。
a.固态氯化铵加热分解 b.浓氨水中加入固体氢氧化钠
c.加热浓氨水 d.固态氯化铵与氢氧化钙混合加热
(2)氯化铵溶液显酸性,用离子方程式表示呈酸性的原因_______ 。
(3)NH3常用于检验氯气管道是否泄漏,写出反应的化学方程式_______ 。
(4)将57.6克的铜投入200毫升的硝酸溶液中恰好反应完全,产生标准状况下的NO2、NO共1.4 mol。
①写出刚开始反应的化学方程式_______ ;
②求硝酸的浓度_______ mol·L-1;
③将生成的气体收集在大试管中,然后倒扣在水中,写出二氧化氮与水反应的化学方程式_______ ,若往试管中通入氧气让液体充满试管,则通入氧气的物质的量_______ mol。
(1)实验室制备氨气,下列方法中可以选用的是
a.固态氯化铵加热分解 b.浓氨水中加入固体氢氧化钠
c.加热浓氨水 d.固态氯化铵与氢氧化钙混合加热
(2)氯化铵溶液显酸性,用离子方程式表示呈酸性的原因
(3)NH3常用于检验氯气管道是否泄漏,写出反应的化学方程式
(4)将57.6克的铜投入200毫升的硝酸溶液中恰好反应完全,产生标准状况下的NO2、NO共1.4 mol。
①写出刚开始反应的化学方程式
②求硝酸的浓度
③将生成的气体收集在大试管中,然后倒扣在水中,写出二氧化氮与水反应的化学方程式
您最近一年使用:0次
解题方法
3 . 已知:稀硝酸能与SO2发生氧化还原反应:3SO2+2HNO3+2H2O=3H2SO4+2NO。下列过程中最终的白色沉淀不一定是BaSO4的是
| A.Fe(NO3)2溶液→通入SO2+过量盐酸→加BaCl2溶液→白色沉淀 |
| B.Ba(NO3)2溶液→加过量盐酸→加Na2SO3溶液→白色沉淀 |
| C.无色溶液→加稀HNO3→加BaCl2溶液→白色沉淀 |
| D.无色溶液→加过量盐酸→无色溶液→加BaCl2溶液→白色溶液 |
您最近一年使用:0次
解题方法
4 . 下列离子方程式书写正确的是
A.金属钠投入 溶液中 溶液中 |
B.向 溶液中通入足量 溶液中通入足量 : :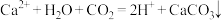 |
C.用氢氧化钠溶液吸收工业废气中的 : :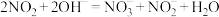 |
D.将FeO与稀 混合: 混合: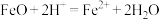 |
您最近一年使用:0次
名校
解题方法
5 . 在下列溶液中,一定能大量共存的离子组是
A.室温时, 的溶液中: 的溶液中: |
B.能使甲基橙试液变红的溶液: |
C.无色透明溶液中: |
D.由水电离出的 的溶液中: 的溶液中: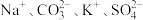 |
您最近一年使用:0次
名校
6 . 常温下,下列各组离子一定能在指定溶液中大量共存的是
A.使紫色石蕊试液变红的溶液中:Fe2+、Mg2+、Cl-、NO |
B. mol /L的溶液中:NH mol /L的溶液中:NH 、Ca2+、Cl-、NO 、Ca2+、Cl-、NO |
C.与Al反应能放出H2的溶液中:Cu2+、 K+、NO 、 、 |
D.水电离产生的c(H+)= 10-12mol/L的溶液中:K+、 Ba2+、Cl-、NO |
您最近一年使用:0次
7 . 下列实验目的操作、实验操作和现象均正确的是
选项 | 实验目的 | 实验操作、实验现象 |
A | 除去甲烷气体中混有的乙烯气体 | 将混合气体通过酸性 |
B | 验证蔗糖已经水解 | 蔗糖和稀硫酸混合加热,冷却后加入NaOH溶液调至碱性,再加入新制 ,加热,有砖红色沉淀产生 ,加热,有砖红色沉淀产生 |
C | 证明高温下铁与水蒸气反应的产物中含有三价铁 | 取铁与水蒸气反应后的固体于试管,先加入稀 溶解,再加入KSCN溶液,溶液变为血红色 溶解,再加入KSCN溶液,溶液变为血红色 |
D | 验证钠的金属性比铜强 | 将金属钠投入 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 某小组研究了铜片与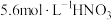 反应的速率,实验现象记录如下表。
反应的速率,实验现象记录如下表。
为探究影响该反应速率的主要因素,小组进行如下实验。
实验Ⅰ:监测上述反应过程中溶液温度的变化,所得曲线如下图: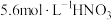 ,结果显示:Cu(NO3)2、NO对Cu和HNO3反应速率的影响均不明显,NO2能明显加快该反应的速率。
,结果显示:Cu(NO3)2、NO对Cu和HNO3反应速率的影响均不明显,NO2能明显加快该反应的速率。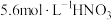 ,当产生气泡较快时,取少量反应液于试管中,检验后发现其中含有NO
,当产生气泡较快时,取少量反应液于试管中,检验后发现其中含有NO 。
。
(1)根据表格中的现象,描述该反应的速率随时间的变化情况:___________ 。
(2)实验Ⅰ的结论:温度升高___________ (填“是”或“不是”)反应速率加快的主要原因。
(3)实验Ⅱ的目的是:___________ 。
(4)小组同学查阅资料后推测:该反应由于生成某中间产物而加快了反应速率。请结合实验Ⅱ、Ⅲ,在下图方框内填入相应的微粒符号,以补全催化机理。①_________ ;②_________ 。 ___________ (请写出操作和现象)。
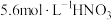 反应的速率,实验现象记录如下表。
反应的速率,实验现象记录如下表。| 实验 | 时间段 | 现象 |
| 0~15min | 铜片表面出现极少气泡 |
| 15~25min | 铜片表面产生较多气泡,溶液呈很浅的蓝色 | |
| 25~30min | 铜片表面均匀冒出大量气泡 | |
| 30~50min | 铜片表面产生较少气泡,溶液蓝色明显变深,液面上方呈浅棕色 |
实验Ⅰ:监测上述反应过程中溶液温度的变化,所得曲线如下图:

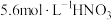 ,结果显示:Cu(NO3)2、NO对Cu和HNO3反应速率的影响均不明显,NO2能明显加快该反应的速率。
,结果显示:Cu(NO3)2、NO对Cu和HNO3反应速率的影响均不明显,NO2能明显加快该反应的速率。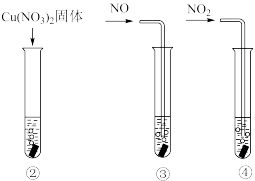
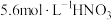 ,当产生气泡较快时,取少量反应液于试管中,检验后发现其中含有NO
,当产生气泡较快时,取少量反应液于试管中,检验后发现其中含有NO 。
。(1)根据表格中的现象,描述该反应的速率随时间的变化情况:
(2)实验Ⅰ的结论:温度升高
(3)实验Ⅱ的目的是:
(4)小组同学查阅资料后推测:该反应由于生成某中间产物而加快了反应速率。请结合实验Ⅱ、Ⅲ,在下图方框内填入相应的微粒符号,以补全催化机理。①

您最近一年使用:0次
2023-10-17更新
|
204次组卷
|
12卷引用:云南省马关县第一中学2021-2022学年高二下学期开学考试化学试题
云南省马关县第一中学2021-2022学年高二下学期开学考试化学试题云南省文山州广南县第二中学校2021-2022学年高二上学期12月考试化学试题【区级联考】北京市西城区2018-2019学年高二上学期期末考试化学试题湖北省荆门市龙泉中学、巴东一中2019-2020学年高二10月联考化学试题北京二中2020-2021学年高二上学期10月月考化学试题北京市第十二中学2020-2021学年高二上学期期末考试化学试题北京市第三十五中学2022-2023学年高二上学期10月月考化学试题北京市育才学校2023-2024学年高二上学期10月月考化学试题北京市第二十二中学2023-2024学年高二上学期10月月考化学试题北京师范大学附属中学2023-2024学年高二上学期期中考试化学试卷北京市第一六一中学2023-2024学年高二上学期10月月考化学试题江西省南昌市第十九中学2023-2024学年高二上学期第一次月考化学试卷
9 . 下列关于物质应用的分析错误的是
| A.常温下,用铁槽车运输浓硝酸利用了浓硝酸的强氧化性 |
B.葡萄酒中添加适量的 利用了 利用了 的水溶液呈酸性的特点 的水溶液呈酸性的特点 |
C.维生素C做 中毒的急救药是利用了维生素C的强还原性 中毒的急救药是利用了维生素C的强还原性 |
D.高铁酸盐可作水处理剂,利用了高铁酸盐的强氧化性和生成的 胶体的吸附性 胶体的吸附性 |
您最近一年使用:0次
2023-10-10更新
|
65次组卷
|
2卷引用:云南省部分名校2023-2024学年高二上学期9月大联考化学试题
解题方法
10 . 实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是
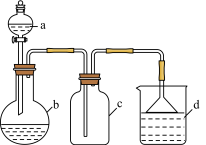
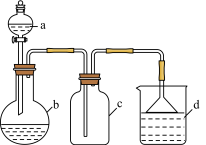
| 选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
| A | 浓硝酸 |  |  |  溶液 溶液 |
| B | 浓硫酸 |  |  |  溶液 溶液 |
| C | 浓硝酸 |  |  |  溶液 溶液 |
| D | 稀盐酸 |  |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 溶液洗气
溶液洗气


