名校
解题方法
1 . 下列各组离子在指定的溶液中,能大量共存的是
A.使甲基橙变红色的溶液: 、 、 、 、 、 、 |
B. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C.在 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.由水电离出的 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
2 . 下列各组中的离子,能在溶液中大量共存的是
A. | B. |
C. | D. |
您最近一年使用:0次
名校
3 . 氮是参与生命活动的重要元素。氮在大气圈、水圈和生物圈中进行元素循环。氨是一种重要的化工原料,主要用于化肥工业,也广泛用于硝酸、纯碱、制药等工业;合成氨反应中,N2(g)与足量H2(g)反应生成1molNH3(g)放出46kJ的热量,实验室用加热NH4Cl和Ca(OH)2固体混合物的方法制取少量氨气,同时生成CaCl2.肼(N2H4)是一种良好的液体燃料。
下列化学反应表示正确的是
下列化学反应表示正确的是
A.用过量氨水吸收废气中的SO2:NH3•H2O+SO2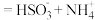 |
B.用烧碱溶液吸收硝酸工业尾气:NO+NO2+2OH﹣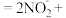 H2O H2O |
| C.合成氨反应:N2(g)+3H2(g)⇌2NH3(g) ΔH=﹣46kJ•mol﹣1 |
D.铜粉和稀硝酸反应:4H+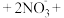 Cu=Cu2++2NO2↑+2H2O Cu=Cu2++2NO2↑+2H2O |
您最近一年使用:0次
名校
4 . 含氮化合物的处理对环境保护意义重大。研究氮及其化合物的性质,可以有效改善人类的生存环境。
(1)N原子的电子式为___________ 。
(2)用 或CO催化还原NO均能消除污染,反应的氧化产物为
或CO催化还原NO均能消除污染,反应的氧化产物为______ 。
(3)实验室常用NaOH溶液吸收 (NO和
(NO和 的混合气体),反应的化学方程式如下:
的混合气体),反应的化学方程式如下:
 ;
; (已知NO不能与NaOH溶液反应,不考虑
(已知NO不能与NaOH溶液反应,不考虑 与
与 的转化)。
的转化)。
①若 能被NaOH溶液完全吸收,则x的取值范围为
能被NaOH溶液完全吸收,则x的取值范围为______ 。
②若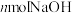 恰好完全反应,则被吸收的
恰好完全反应,则被吸收的 的体积为
的体积为______ L(标准状况)。
③将这两个反应中的产物进行分类,分类方法错误的是______ 。
A.强电解质和弱电解质 B.盐和氧化物
C.离子化合物和共价化合物 D.氧化产物和还原产物
(4)将32.64g铜与200mL一定浓度的硝酸反应,铜完全溶解,产生的NO和 混合气体在标准状况下的体积为11.2L。请回答:
混合气体在标准状况下的体积为11.2L。请回答:
①NO的物质的量为___________ mol, 的体积为
的体积为___________ L(标准状况)。
②待产生的气体全部释放后,向溶液中加入 的NaOH溶液,恰好使溶液中的
的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为___________  。
。
(1)N原子的电子式为
(2)用
 或CO催化还原NO均能消除污染,反应的氧化产物为
或CO催化还原NO均能消除污染,反应的氧化产物为(3)实验室常用NaOH溶液吸收
 (NO和
(NO和 的混合气体),反应的化学方程式如下:
的混合气体),反应的化学方程式如下: ;
; (已知NO不能与NaOH溶液反应,不考虑
(已知NO不能与NaOH溶液反应,不考虑 与
与 的转化)。
的转化)。①若
 能被NaOH溶液完全吸收,则x的取值范围为
能被NaOH溶液完全吸收,则x的取值范围为②若
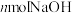 恰好完全反应,则被吸收的
恰好完全反应,则被吸收的 的体积为
的体积为③将这两个反应中的产物进行分类,分类方法错误的是
A.强电解质和弱电解质 B.盐和氧化物
C.离子化合物和共价化合物 D.氧化产物和还原产物
(4)将32.64g铜与200mL一定浓度的硝酸反应,铜完全溶解,产生的NO和
 混合气体在标准状况下的体积为11.2L。请回答:
混合气体在标准状况下的体积为11.2L。请回答:①NO的物质的量为
 的体积为
的体积为②待产生的气体全部释放后,向溶液中加入
 的NaOH溶液,恰好使溶液中的
的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为 。
。
您最近一年使用:0次
名校
解题方法
5 . 某稀硫酸和稀硝酸混合溶液100 mL,逐渐加入铁粉,产生气体的量随铁粉加入量的变化如图所示,求原混合溶液 和
和 的浓度
的浓度___________ 。(需在答题纸上写出计算过程)

 和
和 的浓度
的浓度
您最近一年使用:0次
名校
6 . Ⅰ.部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如图所示。
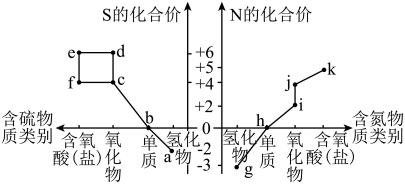
回答下列问题:
(1)j的化学名称是___________ 。
(2)下列有关a和g的叙述中,能说明N的非金属性比S强的是___________ (填字母)。
A.物质a的水溶液为酸性,而物质g的水溶液为碱性
B.物质a在300℃左右分解生成b,而物质g分解生成h的温度高于300℃
C.物质a液化的温度为-60℃,而物质g液化的温度为-34℃
(3)将pH=1的物质k的稀溶液倒入物质f的溶液中,会生成物质e,该反应的离子方程式是___________ 。
Ⅱ.S4N4(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质g通入S2Cl2的CCl4溶液中,可制得该物质:6S2Cl2+16g=S4N4+S8+12NH4Cl(已知S8是硫单质中最稳定的)。
(4)上述制备反应中,物质g体现的性质有___________ ,其中被氧化的元素是___________ (填元素符号)。
(5)S4N4在常温下较稳定,但撞击或加热时会引起爆炸,生成非常稳定的单质产物,该爆炸反应的化学方程式是___________ 。
Ⅲ.二氯化二硫(S2Cl2)可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。S2Cl2可通过硫与少量氯气在110~140℃反应制得,氯气过量则会生成SCl2,S2Cl2遇水剧烈水解,生成SO2、HCl和一种常见的固体。
(6)该固体是___________ (填名称)。
(7)甲同学为了验证两种气体产物,将水解生成的气体依次通过硝酸银与稀硝酸的混合溶液、品红溶液、NaOH溶液,该方案___________ (填“可行”或“不可行”),原因是___________ 。
(8)乙同学按如下实验方案检验S2Cl2是否含有杂质:
①取1.25g产品,在密闭容器中依次加入足量水、双氧水、Ba(NO3)2溶液,过滤;
②往①的滤液中加入足量AgNO3溶液,过滤、洗涤、干燥,称得固体质量为2.87g。
则产品中氯元素的质量分数为___________ ,由此可知产品中___________ (填“含有”或“不含有”)SCl2杂质。

回答下列问题:
(1)j的化学名称是
(2)下列有关a和g的叙述中,能说明N的非金属性比S强的是
A.物质a的水溶液为酸性,而物质g的水溶液为碱性
B.物质a在300℃左右分解生成b,而物质g分解生成h的温度高于300℃
C.物质a液化的温度为-60℃,而物质g液化的温度为-34℃
(3)将pH=1的物质k的稀溶液倒入物质f的溶液中,会生成物质e,该反应的离子方程式是
Ⅱ.S4N4(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质g通入S2Cl2的CCl4溶液中,可制得该物质:6S2Cl2+16g=S4N4+S8+12NH4Cl(已知S8是硫单质中最稳定的)。
(4)上述制备反应中,物质g体现的性质有
(5)S4N4在常温下较稳定,但撞击或加热时会引起爆炸,生成非常稳定的单质产物,该爆炸反应的化学方程式是
Ⅲ.二氯化二硫(S2Cl2)可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。S2Cl2可通过硫与少量氯气在110~140℃反应制得,氯气过量则会生成SCl2,S2Cl2遇水剧烈水解,生成SO2、HCl和一种常见的固体。
(6)该固体是
(7)甲同学为了验证两种气体产物,将水解生成的气体依次通过硝酸银与稀硝酸的混合溶液、品红溶液、NaOH溶液,该方案
(8)乙同学按如下实验方案检验S2Cl2是否含有杂质:
①取1.25g产品,在密闭容器中依次加入足量水、双氧水、Ba(NO3)2溶液,过滤;
②往①的滤液中加入足量AgNO3溶液,过滤、洗涤、干燥,称得固体质量为2.87g。
则产品中氯元素的质量分数为
您最近一年使用:0次
名校
7 . 按要求书写离子或化学方程式
(1)冶炼金属铝的化学方程式___________ ;
(2)碳铵分解的化学方程式___________ ;
(3)过氧化钠和水反应的离子方程式___________ ;
(4)氨的催化氧化的化学方程式___________ ;
(5)大理石和醋酸反应的离子方程式___________ ;
(6)电解饱和食盐水的离子方程式___________ ;
(7)铜和稀硝酸反应的离子方程式___________ ;
(8)漂白粉放置空气中失效的化学方程式___________ ;
(9)向饱和的碳酸钠溶液中通入足量的二氧化碳的离子方程式___________ ;
(10)高锰酸钾和浓盐酸反应制备氯气的化学方程式___________ 。
(1)冶炼金属铝的化学方程式
(2)碳铵分解的化学方程式
(3)过氧化钠和水反应的离子方程式
(4)氨的催化氧化的化学方程式
(5)大理石和醋酸反应的离子方程式
(6)电解饱和食盐水的离子方程式
(7)铜和稀硝酸反应的离子方程式
(8)漂白粉放置空气中失效的化学方程式
(9)向饱和的碳酸钠溶液中通入足量的二氧化碳的离子方程式
(10)高锰酸钾和浓盐酸反应制备氯气的化学方程式
您最近一年使用:0次
名校
解题方法
8 . 利用如图装置(夹持装置略)进行实验并检验生成的气体产物。b中现象不能 证明a中对应气体产物的是
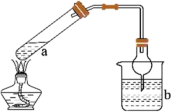

| 选项 | a中试剂 | 检验气体 | b中试剂及现象 |
| A | 浓 |  | 淀粉 溶液变蓝 溶液变蓝 |
| B | 氨水 |  | 酚酞溶液变红 |
| C |  与浓 与浓 |  | 品红溶液褪色 |
| D | 2-溴丙烷和 醇溶液 醇溶液 | 丙烯 | 溴水褪色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 某溶液 ,并含有较多
,并含有较多 、
、 ,那么溶液中不可能含有的负离子是
,那么溶液中不可能含有的负离子是
 ,并含有较多
,并含有较多 、
、 ,那么溶液中不可能含有的负离子是
,那么溶液中不可能含有的负离子是A. | B. | C. | D. |
您最近一年使用:0次
解题方法
10 . 某无色透明溶液能与铝作用放出氢气,此溶液中一定能大量共存的离子组是
A.Cl-、SO 、Na+、K+ 、Na+、K+ | B.K+、ClO-、Na+、NO |
C.HCO 、Na+、NO 、Na+、NO 、K+ 、K+ | D.NO 、Ba2+、Cl-、NH 、Ba2+、Cl-、NH |
您最近一年使用:0次



