名校
解题方法
1 . 化学变化总是伴随着能量的变化。“铝热反应”是将单质铝与金属氧化物混合物反应获得金属单质的化学反应。在野外焊接钢轨时可利用此反应。实验室中可用如图装置实现:_______ 。
(2)实验中能观察到的现象有(例举两点):_______ 。
(3)可表示铝与氧化铁反应的热效应的图是_______ 。
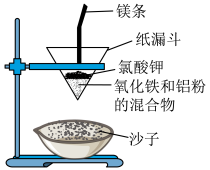
(2)实验中能观察到的现象有(例举两点):
(3)可表示铝与氧化铁反应的热效应的图是
A.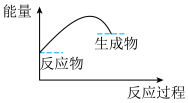 B.
B. C.
C.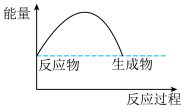
| A.铝还原性较强 | B.锰、钒熔点高 |
| C.铝能形成多种合金 | D.反应放出大量热 |
您最近一年使用:0次
名校
解题方法
2 . 将铝与氧化铁混合制备单质铁的反应称为铝热反应,反应装置如图所示:_____ 。
(2)该铝热反应的化学方程式为_____ ,引发铝热反应的实验操作是_____ 。
(3)取少量反应所得的固体混合物,将其溶于足量稀 ,滴加KSCN溶液无明显现象,能否说明固体混合物中已无
,滴加KSCN溶液无明显现象,能否说明固体混合物中已无 ,请判断并说明理由
,请判断并说明理由_____ 。
(4)写出一种铝热反应的实际应用_____ 。
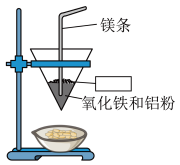
(2)该铝热反应的化学方程式为
(3)取少量反应所得的固体混合物,将其溶于足量稀
 ,滴加KSCN溶液无明显现象,能否说明固体混合物中已无
,滴加KSCN溶液无明显现象,能否说明固体混合物中已无 ,请判断并说明理由
,请判断并说明理由(4)写出一种铝热反应的实际应用
您最近一年使用:0次
名校
解题方法
3 . 钼(Mo)及其化合物广泛地应用于医疗卫生、国防等领域。某镍钼矿中的镍和钼以 和
和 形式存在,从镍钼矿中分离钼,并得到
形式存在,从镍钼矿中分离钼,并得到 的一种工艺流程。
的一种工艺流程。
已知“浸取”过程中发生如下反应: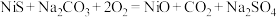
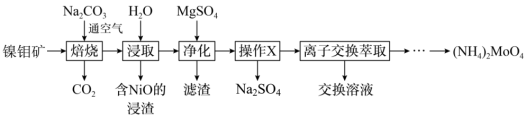
(1) 位于元素周期表第
位于元素周期表第________ 周期第________ 族。
(2)“焙烧”中生成 的反应如下所示,请配平该化学方程式
的反应如下所示,请配平该化学方程式______ 。

上述反应中共价化合物的中心原子杂化方式是________ 杂化。
(3)下列说法正确的是________。(不定项)
 用量对钼浸出率和浸取液中
用量对钼浸出率和浸取液中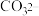 浓度的影响如左下图所示,
浓度的影响如左下图所示, 的溶解度曲线如右下图所示。
的溶解度曲线如右下图所示。

(4)分析实际生产中选择用量为理论用量1.2倍的原因是:________________ 。
(5)为充分分离 ,工艺流程中的“操作
,工艺流程中的“操作 ”应为________。
”应为________。
(6)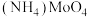 中存在的相互作用有________。
中存在的相互作用有________。
(7)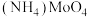 分解可得
分解可得 。高温下,用铝粉还原
。高温下,用铝粉还原 得到金属钼的化学方程式为:
得到金属钼的化学方程式为:________________ 。
 和
和 形式存在,从镍钼矿中分离钼,并得到
形式存在,从镍钼矿中分离钼,并得到 的一种工艺流程。
的一种工艺流程。已知“浸取”过程中发生如下反应:
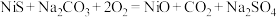

(1)
 位于元素周期表第
位于元素周期表第(2)“焙烧”中生成
 的反应如下所示,请配平该化学方程式
的反应如下所示,请配平该化学方程式
上述反应中共价化合物的中心原子杂化方式是
(3)下列说法正确的是________。(不定项)
A.电负性: | B.离子半径: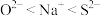 |
C.第一电离能: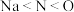 | D.基态 的简化电子排布式 的简化电子排布式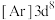 |
 用量对钼浸出率和浸取液中
用量对钼浸出率和浸取液中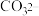 浓度的影响如左下图所示,
浓度的影响如左下图所示, 的溶解度曲线如右下图所示。
的溶解度曲线如右下图所示。
(4)分析实际生产中选择用量为理论用量1.2倍的原因是:
(5)为充分分离
 ,工艺流程中的“操作
,工艺流程中的“操作 ”应为________。
”应为________。| A.蒸发结晶 | B.低温结晶 | C.蒸馏 | D.萃取 |
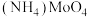 中存在的相互作用有________。
中存在的相互作用有________。| A.分子间作用力 | B.金属键 | C.共价键 | D.离子键 |
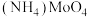 分解可得
分解可得 。高温下,用铝粉还原
。高温下,用铝粉还原 得到金属钼的化学方程式为:
得到金属钼的化学方程式为:
您最近一年使用:0次
名校
解题方法
4 . “铝热反应”是将单质铝与金属氧化物混合物反应获得金属单质的化学反应。在野外焊接钢轨时可利用此反应。实验室中可用如下装置实现:
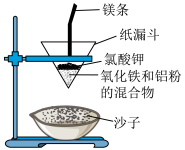
(1)写出该反应的化学方程式_______ 。
(2)实验中能观察到的现象有_______ 、_______ (例举两点)。
(3)可表示铝与氧化铁反应的热效应的图是
A .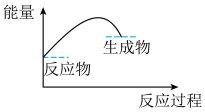 B.
B.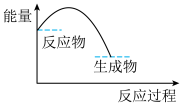 C.
C.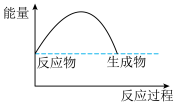
(4)工业上可用铝热反应冶炼锰、钒等金属,其原因与下列无关的是_______
(5)以下实验中属于放热反应的是_______
A.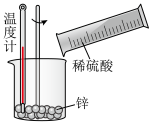 B.
B.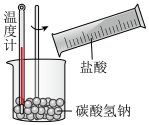 C.
C.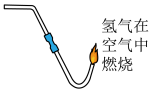

(1)写出该反应的化学方程式
(2)实验中能观察到的现象有
(3)可表示铝与氧化铁反应的热效应的图是
A .
 B.
B. C.
C.
(4)工业上可用铝热反应冶炼锰、钒等金属,其原因与下列无关的是_______
| A.铝还原性较强 | B.锰、钒熔点高 | C.铝能形成多种合金 | D.反应放出大量热 |
(5)以下实验中属于放热反应的是
A.
 B.
B. C.
C.
您最近一年使用:0次
解题方法
5 . 铝是一种重要金属,从铝土矿(主要成分为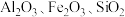 等)中冶炼Al的工业生产流程如下图:
等)中冶炼Al的工业生产流程如下图:
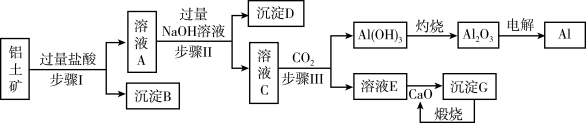
(1)写出步骤Ⅱ生成溶液C 的离子方程式___________ ,步骤I、Ⅱ、Ⅲ都要用到的分离方法是___________ 。
(2)生产中曾用铝与氧化铁的混合物形成铝热剂发生铝热反应焊接钢轨(提示:反应中能生成铁单质),则铝与氧化铁在高温下发生反应的化学方程式为:___________ 。
(3)CO2中心原子的杂化方式为___________ ,VSEPR 模型为___________ 。
 等)中冶炼Al的工业生产流程如下图:
等)中冶炼Al的工业生产流程如下图:
(1)写出步骤Ⅱ生成溶液C 的离子方程式
(2)生产中曾用铝与氧化铁的混合物形成铝热剂发生铝热反应焊接钢轨(提示:反应中能生成铁单质),则铝与氧化铁在高温下发生反应的化学方程式为:
(3)CO2中心原子的杂化方式为
您最近一年使用:0次
名校
解题方法
6 . 如图所示:①~⑩分别代表有关反应中的一种物质,它们均为常见物质。已知①~⑤和⑥~⑩中分别含有同一种元素。试回答下列问题:
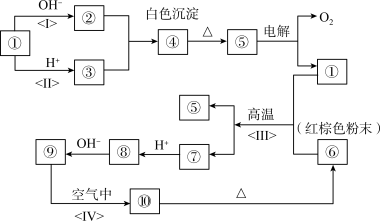
(1)写出指定物质的化学式:④_______ ;⑥_______ ;
(2)写出反应(Ⅲ)的化学方程式_______ ;指出该反应的重要用途之一:_______ ;
(3)写出反应(Ⅰ)的离子方程式_______ ;
(4)反应(Ⅳ)的主要实验现象是_______ ;该反应的化学方程式为:_______ 。

(1)写出指定物质的化学式:④
(2)写出反应(Ⅲ)的化学方程式
(3)写出反应(Ⅰ)的离子方程式
(4)反应(Ⅳ)的主要实验现象是
您最近一年使用:0次
名校
7 . 次锰酸根离子( ),水溶液呈亮蓝色。工业上常用软锰矿(主要成分
),水溶液呈亮蓝色。工业上常用软锰矿(主要成分 ,含有少量的
,含有少量的 、
、 、
、 以及其他少量不溶于水、不反应的杂质)为原料制备。现有一种制备流程如图:
以及其他少量不溶于水、不反应的杂质)为原料制备。现有一种制备流程如图:
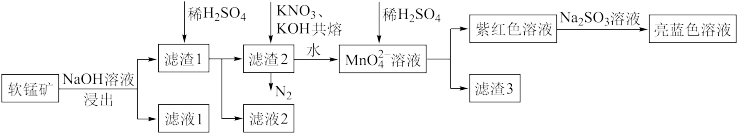
(1)滤渣1的主要成分是___________ , 在周期表中的位置
在周期表中的位置___________ 。
(2)流程中共熔时发生的主要反应的化学方程式为___________ 。
(3)写出 转变为紫红色溶液的离子反应方程式
转变为紫红色溶液的离子反应方程式___________ 。
(4)整个流程中的___________ (填化学式)能重复利用。
(5) 在高温条件下还原软锰矿制备
在高温条件下还原软锰矿制备 的化学方程式为
的化学方程式为___________ 。
 ),水溶液呈亮蓝色。工业上常用软锰矿(主要成分
),水溶液呈亮蓝色。工业上常用软锰矿(主要成分 ,含有少量的
,含有少量的 、
、 、
、 以及其他少量不溶于水、不反应的杂质)为原料制备。现有一种制备流程如图:
以及其他少量不溶于水、不反应的杂质)为原料制备。现有一种制备流程如图: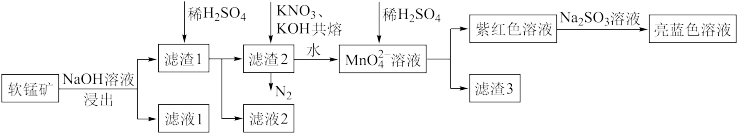
(1)滤渣1的主要成分是
 在周期表中的位置
在周期表中的位置(2)流程中共熔时发生的主要反应的化学方程式为
(3)写出
 转变为紫红色溶液的离子反应方程式
转变为紫红色溶液的离子反应方程式(4)整个流程中的
(5)
 在高温条件下还原软锰矿制备
在高温条件下还原软锰矿制备 的化学方程式为
的化学方程式为
您最近一年使用:0次
2024-02-20更新
|
164次组卷
|
2卷引用:吉林省长春市东北师大附中2023-2024学年高一上学期期末考试化学试题
名校
解题方法
8 . 合理、高效利用金属矿物。将金属从其化合物中还原出来用于生产和制造各种金属材料,利用金属活动性的不同,可以采用不同的冶炼方法。
(1)以 为原料冶炼
为原料冶炼 ,冶炼方法是
,冶炼方法是_______ ,下列能用该方法制得的金属是_______ (填字母)。
A. B.
B. C.
C.
(2)明代《天工开物》记载了“火法”冶炼锌的方法:“炉甘石十斤,装载入一泥罐内,…然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…冷淀,毁罐取出,…,即倭铅也”(已知炉甘石的主要成分为碳酸锌)。下列说法不正确的是_______(填字母)。
(3)铝热法是冶炼金属的方法之一(如下图),写出铝热法炼铁的化学方程式_______ 。引发铝热反应的实验操作是_______ 。

(4)金属镁的冶炼有多种方法,其中一种以白云石(主要成分为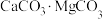 )为原料,经高温煅烧生成氧化物
)为原料,经高温煅烧生成氧化物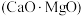 ,氧化物在还原炉中经
,氧化物在还原炉中经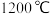 真空条件下用硅铁(硅铁含硅量达
真空条件下用硅铁(硅铁含硅量达 )还原生成镁蒸汽(铁在反应前后化合价不变),镁蒸汽经冷凝器冷聚为粗镁,粗镁再经精炼、铸锭得到成品金属镁。反应工艺流程如图:
)还原生成镁蒸汽(铁在反应前后化合价不变),镁蒸汽经冷凝器冷聚为粗镁,粗镁再经精炼、铸锭得到成品金属镁。反应工艺流程如图:
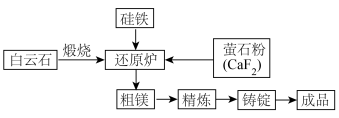
①萤石粉作为活性剂,可增强冶炼过程中的打渣能力,用电子式表示 的形成过程
的形成过程_______ 。
②写出还原炉中高温下发生置换反应的化学方程式_______ 。
(1)以
 为原料冶炼
为原料冶炼 ,冶炼方法是
,冶炼方法是A.
 B.
B. C.
C.
(2)明代《天工开物》记载了“火法”冶炼锌的方法:“炉甘石十斤,装载入一泥罐内,…然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…冷淀,毁罐取出,…,即倭铅也”(已知炉甘石的主要成分为碳酸锌)。下列说法不正确的是_______(填字母)。
| A.煤炭中起作用的主要元素是碳 |
| B.该冶炼锌的方法属于热还原法 |
| C.倭铅是指金属锌和铅的混合物 |
D.冶炼 的反应方程式为 的反应方程式为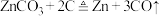 |
(3)铝热法是冶炼金属的方法之一(如下图),写出铝热法炼铁的化学方程式

(4)金属镁的冶炼有多种方法,其中一种以白云石(主要成分为
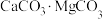 )为原料,经高温煅烧生成氧化物
)为原料,经高温煅烧生成氧化物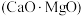 ,氧化物在还原炉中经
,氧化物在还原炉中经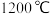 真空条件下用硅铁(硅铁含硅量达
真空条件下用硅铁(硅铁含硅量达 )还原生成镁蒸汽(铁在反应前后化合价不变),镁蒸汽经冷凝器冷聚为粗镁,粗镁再经精炼、铸锭得到成品金属镁。反应工艺流程如图:
)还原生成镁蒸汽(铁在反应前后化合价不变),镁蒸汽经冷凝器冷聚为粗镁,粗镁再经精炼、铸锭得到成品金属镁。反应工艺流程如图:
①萤石粉作为活性剂,可增强冶炼过程中的打渣能力,用电子式表示
 的形成过程
的形成过程②写出还原炉中高温下发生置换反应的化学方程式
您最近一年使用:0次
名校
解题方法
9 . 某铜矿石的主要成分是 ,还含有少量的
,还含有少量的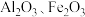 和
和 .某工厂利用此矿石炼制精铜的工艺流程如图所示(已知:
.某工厂利用此矿石炼制精铜的工艺流程如图所示(已知: ;
; 为酸性氧化物,不与盐酸反应但可以和强碱反应).
为酸性氧化物,不与盐酸反应但可以和强碱反应).

(1)滤液A中铁元素的存在形式为______ (填离子符号),生成该离子的离子方程式为______ ,检验滤液A中存在该离子的试剂为______ (填试剂名称);
(2)固体混合物B是______ 和______ 的混合物;
(3)金属E与固体F在高温下发生的某一反应可制得粗铜,该反应的化学方程式为_____________ ;
(4)从固体混合物中提炼粗铜,加入的溶液G为_____________ ;
(5)称取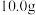 该铜矿石,经以上流程最终制得精铜
该铜矿石,经以上流程最终制得精铜 ,则该铜矿石中
,则该铜矿石中 的纯度为
的纯度为______ 。
 ,还含有少量的
,还含有少量的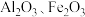 和
和 .某工厂利用此矿石炼制精铜的工艺流程如图所示(已知:
.某工厂利用此矿石炼制精铜的工艺流程如图所示(已知: ;
; 为酸性氧化物,不与盐酸反应但可以和强碱反应).
为酸性氧化物,不与盐酸反应但可以和强碱反应).
(1)滤液A中铁元素的存在形式为
(2)固体混合物B是
(3)金属E与固体F在高温下发生的某一反应可制得粗铜,该反应的化学方程式为
(4)从固体混合物中提炼粗铜,加入的溶液G为
(5)称取
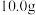 该铜矿石,经以上流程最终制得精铜
该铜矿石,经以上流程最终制得精铜 ,则该铜矿石中
,则该铜矿石中 的纯度为
的纯度为
您最近一年使用:0次
名校
10 . 次锰酸根离子( ),水溶液呈亮蓝色,它在一些有机物的氧化过程中会以中间体出现,该离子不稳定,易发生歧化反应,工业上常用软锰矿(主要成分
),水溶液呈亮蓝色,它在一些有机物的氧化过程中会以中间体出现,该离子不稳定,易发生歧化反应,工业上常用软锰矿(主要成分 ,含有少量的
,含有少量的 、
、 、
、 、
、 以及其他少量不溶于水、不反应的杂质)为原料制备。现有一种制备流程如图:(资料:
以及其他少量不溶于水、不反应的杂质)为原料制备。现有一种制备流程如图:(资料: 属于酸性氧化物。)
属于酸性氧化物。)

(1)滤液1的主要成分是_______ ,Mn在周期表中的位置_______ 。
(2)流程中共熔时发生的主要反应的化学方程式为_______ 。
(3)写出 转变为紫红色溶液的离子方程式
转变为紫红色溶液的离子方程式_______ 。
(4)整个流程中的_______ (填化学式)能重复利用。
(5)A1还原软锰矿制备Mn的化学方程式为_______ 。
 ),水溶液呈亮蓝色,它在一些有机物的氧化过程中会以中间体出现,该离子不稳定,易发生歧化反应,工业上常用软锰矿(主要成分
),水溶液呈亮蓝色,它在一些有机物的氧化过程中会以中间体出现,该离子不稳定,易发生歧化反应,工业上常用软锰矿(主要成分 ,含有少量的
,含有少量的 、
、 、
、 、
、 以及其他少量不溶于水、不反应的杂质)为原料制备。现有一种制备流程如图:(资料:
以及其他少量不溶于水、不反应的杂质)为原料制备。现有一种制备流程如图:(资料: 属于酸性氧化物。)
属于酸性氧化物。)
(1)滤液1的主要成分是
(2)流程中共熔时发生的主要反应的化学方程式为
(3)写出
 转变为紫红色溶液的离子方程式
转变为紫红色溶液的离子方程式(4)整个流程中的
(5)A1还原软锰矿制备Mn的化学方程式为
您最近一年使用:0次
2023-12-14更新
|
202次组卷
|
2卷引用:黑龙江省哈尔滨市第六中学校2023-2024学年高一上学期12月测试化学试题



