真题
解题方法
1 . 室温下,为探究纳米铁去除水样中 的影响因素,测得不同条件下
的影响因素,测得不同条件下 浓度随时间变化关系如下图。
浓度随时间变化关系如下图。
下列说法正确的是
 的影响因素,测得不同条件下
的影响因素,测得不同条件下 浓度随时间变化关系如下图。
浓度随时间变化关系如下图。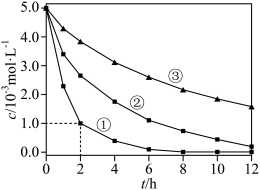
| 实验序号 | 水样体积/ | 纳米铁质量/ | 水样初始 |
| ① | 50 | 8 | 6 |
| ② | 50 | 2 | 6 |
| ③ | 50 | 2 | 8 |
A.实验①中,0~2小时内平均反应速率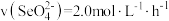 |
B.实验③中,反应的离子方程式为: |
| C.其他条件相同时,适当增加纳米铁质量可加快反应速率 |
D.其他条件相同时,水样初始 越小, 越小, 的去除效果越好 的去除效果越好 |
您最近一年使用:0次
解题方法
2 . NOx(主要指NO和NO2)是大气主要污染物之一。有效去除大气中的NOx是环境保护的重要课题。
(1)用稀硝酸吸收NOx,得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应式:___________ 。
(2)用酸性(NH2)2CO水溶液吸收NOx,吸收过程中存在HNO2与(NH2)2CO生成N2和CO2的反应。写出该反应的化学方程式:___________ 。
(3)用NaOH溶液吸收,主要反应为NO+NO2+2OH−=2NO +H2O 、2NO2+2OH−=NO
+H2O 、2NO2+2OH−=NO +NO
+NO +H2O。吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是
+H2O。吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是___________ (填化学式);吸收后排放的尾气中含量较高的氮氧化物是___________ (填化学式)。
(4)用NaClO溶液吸收。其他条件同,NO转化为NO 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图-1所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图-1所示。 ,其离子方程式为
,其离子方程式为___________ 。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是___________ 。
(5)在有氧条件下,新型催化剂M能催化NH3与NOx生成N2。将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂M的反应器中反应(装置见图-2)。反应相同时间,NOx的去除率随反应温度的变化曲线如图-3所示,在50~250 ℃内随温度的升高,NOx的去除率先迅速上升后上升缓慢的主要原因是___________ ;当反应温度高于380 ℃时,NOx转化率下降,除因为催化剂活性下降、进入反应器的NOx被还原的量减少外,还有___________ (用化学方程式表示)。
(1)用稀硝酸吸收NOx,得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应式:
(2)用酸性(NH2)2CO水溶液吸收NOx,吸收过程中存在HNO2与(NH2)2CO生成N2和CO2的反应。写出该反应的化学方程式:
(3)用NaOH溶液吸收,主要反应为NO+NO2+2OH−=2NO
 +H2O 、2NO2+2OH−=NO
+H2O 、2NO2+2OH−=NO +NO
+NO +H2O。吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是
+H2O。吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是(4)用NaClO溶液吸收。其他条件同,NO转化为NO
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图-1所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图-1所示。
 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高。其原因是
(5)在有氧条件下,新型催化剂M能催化NH3与NOx生成N2。将一定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂M的反应器中反应(装置见图-2)。反应相同时间,NOx的去除率随反应温度的变化曲线如图-3所示,在50~250 ℃内随温度的升高,NOx的去除率先迅速上升后上升缓慢的主要原因是

您最近一年使用:0次
3 . 以金红石(主要成分为 )为原料制备
)为原料制备 的主要过程如下:
的主要过程如下: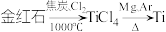 。下列叙述错误的是
。下列叙述错误的是
 )为原料制备
)为原料制备 的主要过程如下:
的主要过程如下: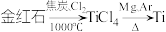 。下列叙述错误的是
。下列叙述错误的是A.利用碳氯化工艺制备 的化学方程式为 的化学方程式为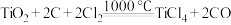 |
B.粗 提纯过程中,具体操作步骤有用水溶解、结晶、过滤等 提纯过程中,具体操作步骤有用水溶解、结晶、过滤等 |
C.制备Ti的主要过程中的 用 用 代替,会影响 代替,会影响 的产率和纯度 的产率和纯度 |
| D.将金红石和焦炭充分混合研磨后,再通入氯气可以提高反应速率 |
您最近一年使用:0次
名校
4 . 探究 反应速率的影响因素,有关实验数据如下表所示:
反应速率的影响因素,有关实验数据如下表所示:
下列说法不正确的是
 反应速率的影响因素,有关实验数据如下表所示:
反应速率的影响因素,有关实验数据如下表所示:| 编号 | 温度/℃ | 酸性 溶液 溶液 |  溶液 溶液 |  的体积 的体积(mL) |  溶液褪色平均时间/min 溶液褪色平均时间/min | ||
| 体积/mL | 浓度/( ) ) | 体积/mL | 浓度/( ) ) | ||||
| 1 | 25 | 4 | 0.1 | 8 | 0.2 | 8 | 12 |
| 2 | 80 | 2 | 0.1 | 8 | 0.2 | a | b |
| 3 | 25 | 2 | 0.1 | 8 | 0.2 | 10 | c |
| A.a=10,b<c,6<c<12 |
B.可通过比较收集相同体积的 所消耗的时间来判断反应速率的快慢 所消耗的时间来判断反应速率的快慢 |
C.用 表示该反应速率,v(实验1)为 表示该反应速率,v(实验1)为 |
D.实验时可依次向试管中加入酸性 溶液、 溶液、 溶液和水 溶液和水 |
您最近一年使用:0次
解题方法
5 . 红矾钠(重铬酸钠: )是重要的基本化工原料,常在印染、电镀等工业中做辅助剂。工业上以铬铁矿(
)是重要的基本化工原料,常在印染、电镀等工业中做辅助剂。工业上以铬铁矿( ,含Al、Si氧化物等杂质)为主要原料制备红矾钠的工艺流程如下。回答下列问题:
,含Al、Si氧化物等杂质)为主要原料制备红矾钠的工艺流程如下。回答下列问题: 转化为
转化为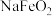 和
和 。
。
②“浸取”时铁元素以 形式存在。
形式存在。
(1)写出“焙烧”时 被氧化的化学方程式:
被氧化的化学方程式:_______ 。
(2)为了加快浸取速率可采取的措施有_______ (请写出两种方法)。
(3)矿物中相关元素可溶性组分的物质的量浓度c与pH的关系如图所示。当溶液中可溶性组分的浓度 时认为已除尽。
时认为已除尽。_______ ,滤渣的主要成分有_______ 。
(4)“酸化”时,不可以将硫酸改为盐酸(HCl),原因是(用离子方程式表示)_______ 。
(5)“冷却结晶”所得母液中,除 外,可在上述流程中循环利用的物质还有
外,可在上述流程中循环利用的物质还有_______ (用化学式表示)。
(6) 的三种结构:①
的三种结构:①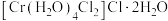 、②
、②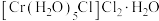 、③
、③ ,下列说法错误的是_______。
,下列说法错误的是_______。
 )是重要的基本化工原料,常在印染、电镀等工业中做辅助剂。工业上以铬铁矿(
)是重要的基本化工原料,常在印染、电镀等工业中做辅助剂。工业上以铬铁矿( ,含Al、Si氧化物等杂质)为主要原料制备红矾钠的工艺流程如下。回答下列问题:
,含Al、Si氧化物等杂质)为主要原料制备红矾钠的工艺流程如下。回答下列问题: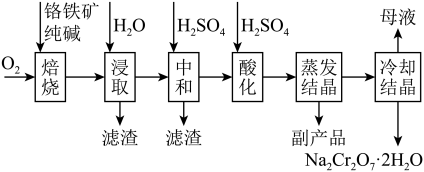
 转化为
转化为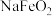 和
和 。
。②“浸取”时铁元素以
 形式存在。
形式存在。(1)写出“焙烧”时
 被氧化的化学方程式:
被氧化的化学方程式:(2)为了加快浸取速率可采取的措施有
(3)矿物中相关元素可溶性组分的物质的量浓度c与pH的关系如图所示。当溶液中可溶性组分的浓度
 时认为已除尽。
时认为已除尽。
(4)“酸化”时,不可以将硫酸改为盐酸(HCl),原因是(用离子方程式表示)
(5)“冷却结晶”所得母液中,除
 外,可在上述流程中循环利用的物质还有
外,可在上述流程中循环利用的物质还有(6)
 的三种结构:①
的三种结构:①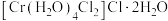 、②
、②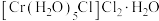 、③
、③ ,下列说法错误的是_______。
,下列说法错误的是_______。A.①中配合离子空间结构为 或 或 (已略去位于正八面体中心的 (已略去位于正八面体中心的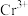 ) ) |
B.②③中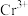 的配位数都是6 的配位数都是6 |
| C.②中存在的作用力有离子键、共价键、配位键和氢键等 |
D.等物质的量浓度、等体积的①②③溶液中, 的物质的量相等 的物质的量相等 |
您最近一年使用:0次
名校
解题方法
6 . 我国最新型055型万吨驱逐舰上使用了最新一代国产有源相控阵雷达,采用了最先进的氮化镓( )半导体技术。某工厂利用铝土矿(主要成分为
)半导体技术。某工厂利用铝土矿(主要成分为 、
、 、
、 )为原料制备
)为原料制备 的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应,
的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应, 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 )半导体技术。某工厂利用铝土矿(主要成分为
)半导体技术。某工厂利用铝土矿(主要成分为 、
、 、
、 )为原料制备
)为原料制备 的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应,
的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应, 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是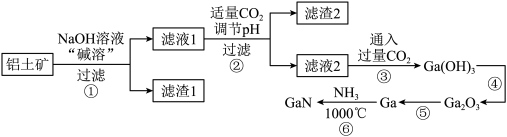
| A.可以通过粉碎铝土矿、搅拌等方法提高“碱溶”效率 |
B.由过程②、③可知, 的酸性比 的酸性比 强 强 |
C.已知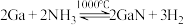 , , 与足量 与足量 反应,转移电子数为 反应,转移电子数为 |
D.滤渣1是 ,生成滤渣2的离子方程式可能为 ,生成滤渣2的离子方程式可能为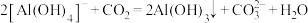 |
您最近一年使用:0次
2024-05-12更新
|
249次组卷
|
2卷引用:安徽师范大学附属中学2024届高三下学期5月测试化学试卷
名校
解题方法
7 . 合成氨是目前转化空气中氮最有效的工业方法,其反应历程和能量变化的简图如图:(图中ad表示物质吸附在催化剂表面时的状态) 2NH3(g)的△H=
2NH3(g)的△H=______ kJ•mol-1,对总反应速率影响较大的是步骤_______ 。(填写编号)
(2)若改变某一条件,使合成氨的化学反应速率加快,下列解释正确的是_______ 。
(3)下列关于硫酸工业和合成氨工业说法错误的是_______ 。
合成氨厂的CO2可用于合成重要化工原料CH3OH,主要反应为:3H2(g)+CO2(g) CH3OH(g)+H2O(g)。向两个容积固定为2L的密闭容器中分别充入比例相同,但总量不同的H2和CO2气体,H2的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如图所示。
CH3OH(g)+H2O(g)。向两个容积固定为2L的密闭容器中分别充入比例相同,但总量不同的H2和CO2气体,H2的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如图所示。_______ mol•L-1•min-1。
(5)由图可判断该反应是_______ (选填“吸热”或“放热”)反应,在______ (填“较高”或“较低”)温度下有利于该反应自发进行。
(6)判断图中n1、n2相对大小:n1______ n2。(选填“<”或“>”)
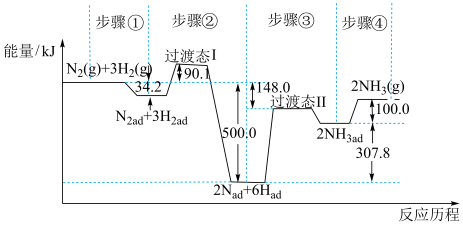
 2NH3(g)的△H=
2NH3(g)的△H=(2)若改变某一条件,使合成氨的化学反应速率加快,下列解释正确的是
| A.升高温度,使单位体积内活化分子百分数增加 |
| B.增加反应物的浓度,使活化分子百分数增加 |
| C.使用催化剂,能降低反应活化能,使单位体积内活化分子数增加 |
| D.增大压强,能降低反应的活化能,使单位体积内活化分子数增加 |
(3)下列关于硫酸工业和合成氨工业说法错误的是
| A.都采用了高压 | B.都使用了催化剂 |
| C.生产流程中都有造气和净化 | D.都使用了热交换器 |
合成氨厂的CO2可用于合成重要化工原料CH3OH,主要反应为:3H2(g)+CO2(g)
 CH3OH(g)+H2O(g)。向两个容积固定为2L的密闭容器中分别充入比例相同,但总量不同的H2和CO2气体,H2的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如图所示。
CH3OH(g)+H2O(g)。向两个容积固定为2L的密闭容器中分别充入比例相同,但总量不同的H2和CO2气体,H2的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如图所示。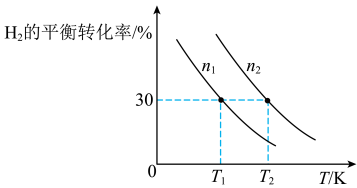
(5)由图可判断该反应是
(6)判断图中n1、n2相对大小:n1
您最近一年使用:0次
解题方法
8 . 工业上以软锰矿(主要成分为MnO2,还含有少量Fe2O3等)和辉铜矿(主要成分为Cu2S,还含有少量Si、Ni等氧化物)为原料,制备碳酸锰和胆矾的工艺流程如图所示。
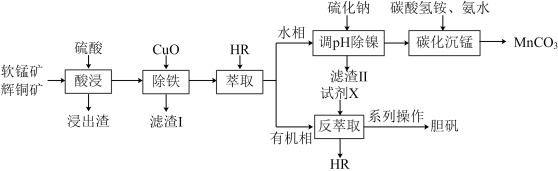
已知:HR萃取Cu2+的原理为Cu2+(aq)+2HR(org) CuR2(org)+2H+(aq)(org为有机相)。
CuR2(org)+2H+(aq)(org为有机相)。
回答下列问题:
(1)为了加快“酸浸”速率,可采取的措施是________ (答出任意两条即可);已知浸出渣中含有单质S,写出“酸浸”时MnO2与Cu2S反应的离子方程式:________ 。
(2)得到“滤渣I”的操作:________ 。
(3)写出“碳化沉锰”过程中发生反应的离子方程式:________ 。
(4)试剂X为________ (填化学式);“系列操作”包括________ 、过滤、洗涤和干燥。

已知:HR萃取Cu2+的原理为Cu2+(aq)+2HR(org)
 CuR2(org)+2H+(aq)(org为有机相)。
CuR2(org)+2H+(aq)(org为有机相)。回答下列问题:
(1)为了加快“酸浸”速率,可采取的措施是
(2)得到“滤渣I”的操作:
(3)写出“碳化沉锰”过程中发生反应的离子方程式:
(4)试剂X为
您最近一年使用:0次
解题方法
9 . 废 催化剂(含
催化剂(含 、
、 、
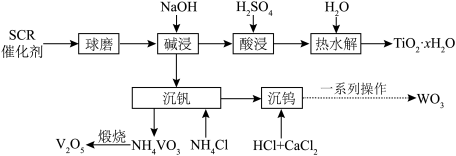
、 等)的回收对环境保护和资源循环利用意义重大。通过如下工艺流程可以回收其中的钛、钒、钨等。
等)的回收对环境保护和资源循环利用意义重大。通过如下工艺流程可以回收其中的钛、钒、钨等。
已知:① 、
、 和
和 都能与
都能与 溶液反应生成可溶性的
溶液反应生成可溶性的 、
、 和不溶性的
和不溶性的 ;
;
② 易水解
易水解
③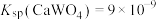 。
。
回答下列问题:
(1)“球磨”的目的是___________ 。
(2)“碱浸”后通过___________ (填操作名称)可以实现钛与钒、钨分离。有同学认为在“碱浸”与“酸浸”之间还应“水洗”,其理由是___________
(3)“酸浸”后钛主要以 形式存在,“热水解”反应的离子方程式为
形式存在,“热水解”反应的离子方程式为___________ 。
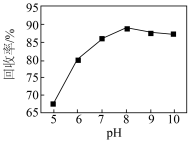
(4)钒的回收率随溶液的pH值变化如图所示,pH=8时回收率最高的原因是___________ 。
(5)“沉钨”中析出 时,需要加入过量
时,需要加入过量 ,其目的是
,其目的是___________ 。
(6)向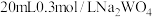 的滤液中加入等体积的
的滤液中加入等体积的 溶液(忽略混合过程中的体积变化),欲使
溶液(忽略混合过程中的体积变化),欲使 浓度小于
浓度小于 ,则
,则 溶液的最小浓度为
溶液的最小浓度为___________ mol/L。
 催化剂(含
催化剂(含 、
、 、
、 等)的回收对环境保护和资源循环利用意义重大。通过如下工艺流程可以回收其中的钛、钒、钨等。
等)的回收对环境保护和资源循环利用意义重大。通过如下工艺流程可以回收其中的钛、钒、钨等。
已知:①
 、
、 和
和 都能与
都能与 溶液反应生成可溶性的
溶液反应生成可溶性的 、
、 和不溶性的
和不溶性的 ;
;②
 易水解
易水解③
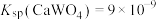 。
。回答下列问题:
(1)“球磨”的目的是
(2)“碱浸”后通过
(3)“酸浸”后钛主要以
 形式存在,“热水解”反应的离子方程式为
形式存在,“热水解”反应的离子方程式为(4)钒的回收率随溶液的pH值变化如图所示,pH=8时回收率最高的原因是

(5)“沉钨”中析出
 时,需要加入过量
时,需要加入过量 ,其目的是
,其目的是(6)向
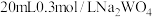 的滤液中加入等体积的
的滤液中加入等体积的 溶液(忽略混合过程中的体积变化),欲使
溶液(忽略混合过程中的体积变化),欲使 浓度小于
浓度小于 ,则
,则 溶液的最小浓度为
溶液的最小浓度为
您最近一年使用:0次
解题方法
10 . 某校化学课外兴趣小组为了探究影响化学反应速率的因素,做了以下实验。
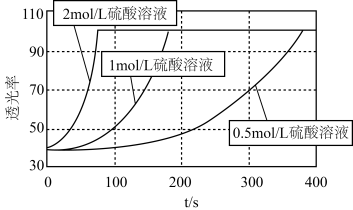
用三支试管各取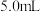 、
、 的酸性
的酸性 溶液,再分别滴入
溶液,再分别滴入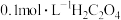 溶液,实验报告如下。
溶液,实验报告如下。
分析实验设计方案和表格中的数据,完成下面的问题:
(1)实验 、
、 研究的是
研究的是___________ 对反应速率的影响。
(2)表中
___________  。
。
(3)实验3用 表示的反应速率为
表示的反应速率为___________ 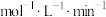 。
。
(4)研究发现 溶液的酸化程度对反应的速率也有较大影响,用不同浓度的硫酸进行酸化,其余条件均相同时,测得反应溶液的透光率(溶液颜色越浅,透光率越高)随时间变化如图所示,由此得出的结论是
溶液的酸化程度对反应的速率也有较大影响,用不同浓度的硫酸进行酸化,其余条件均相同时,测得反应溶液的透光率(溶液颜色越浅,透光率越高)随时间变化如图所示,由此得出的结论是___________ 。
用三支试管各取
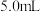 、
、 的酸性
的酸性 溶液,再分别滴入
溶液,再分别滴入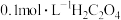 溶液,实验报告如下。
溶液,实验报告如下。| 实验编号 |  酸性 酸性 溶液 溶液 |   溶液 溶液 | 水 | 反应温度/℃ | 溶液颜色褪至无色所需时间/s |
| 1 | 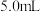 | 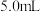 | 0 | 20 | 125 |
| 2 | 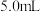 |  | 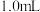 | 20 | 320 |
| 3 | 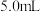 | 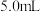 | 0 | 50 | 30 |
(1)实验
 、
、 研究的是
研究的是(2)表中

 。
。(3)实验3用
 表示的反应速率为
表示的反应速率为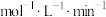 。
。(4)研究发现
 溶液的酸化程度对反应的速率也有较大影响,用不同浓度的硫酸进行酸化,其余条件均相同时,测得反应溶液的透光率(溶液颜色越浅,透光率越高)随时间变化如图所示,由此得出的结论是
溶液的酸化程度对反应的速率也有较大影响,用不同浓度的硫酸进行酸化,其余条件均相同时,测得反应溶液的透光率(溶液颜色越浅,透光率越高)随时间变化如图所示,由此得出的结论是
您最近一年使用:0次



