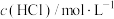真题
解题方法
1 . 室温下,为探究纳米铁去除水样中 的影响因素,测得不同条件下
的影响因素,测得不同条件下 浓度随时间变化关系如下图。
浓度随时间变化关系如下图。
下列说法正确的是
 的影响因素,测得不同条件下
的影响因素,测得不同条件下 浓度随时间变化关系如下图。
浓度随时间变化关系如下图。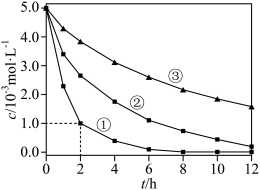
| 实验序号 | 水样体积/ | 纳米铁质量/ | 水样初始 |
| ① | 50 | 8 | 6 |
| ② | 50 | 2 | 6 |
| ③ | 50 | 2 | 8 |
A.实验①中,0~2小时内平均反应速率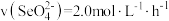 |
B.实验③中,反应的离子方程式为: |
| C.其他条件相同时,适当增加纳米铁质量可加快反应速率 |
D.其他条件相同时,水样初始 越小, 越小, 的去除效果越好 的去除效果越好 |
您最近一年使用:0次
2 . 以金红石(主要成分为 )为原料制备
)为原料制备 的主要过程如下:
的主要过程如下: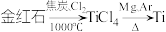 。下列叙述错误的是
。下列叙述错误的是
 )为原料制备
)为原料制备 的主要过程如下:
的主要过程如下: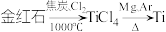 。下列叙述错误的是
。下列叙述错误的是A.利用碳氯化工艺制备 的化学方程式为 的化学方程式为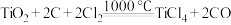 |
B.粗 提纯过程中,具体操作步骤有用水溶解、结晶、过滤等 提纯过程中,具体操作步骤有用水溶解、结晶、过滤等 |
C.制备Ti的主要过程中的 用 用 代替,会影响 代替,会影响 的产率和纯度 的产率和纯度 |
| D.将金红石和焦炭充分混合研磨后,再通入氯气可以提高反应速率 |
您最近一年使用:0次
名校
3 . 探究 反应速率的影响因素,有关实验数据如下表所示:
反应速率的影响因素,有关实验数据如下表所示:
下列说法不正确的是
 反应速率的影响因素,有关实验数据如下表所示:
反应速率的影响因素,有关实验数据如下表所示:| 编号 | 温度/℃ | 酸性 溶液 溶液 |  溶液 溶液 |  的体积 的体积(mL) |  溶液褪色平均时间/min 溶液褪色平均时间/min | ||
| 体积/mL | 浓度/( ) ) | 体积/mL | 浓度/( ) ) | ||||
| 1 | 25 | 4 | 0.1 | 8 | 0.2 | 8 | 12 |
| 2 | 80 | 2 | 0.1 | 8 | 0.2 | a | b |
| 3 | 25 | 2 | 0.1 | 8 | 0.2 | 10 | c |
| A.a=10,b<c,6<c<12 |
B.可通过比较收集相同体积的 所消耗的时间来判断反应速率的快慢 所消耗的时间来判断反应速率的快慢 |
C.用 表示该反应速率,v(实验1)为 表示该反应速率,v(实验1)为 |
D.实验时可依次向试管中加入酸性 溶液、 溶液、 溶液和水 溶液和水 |
您最近一年使用:0次
名校
解题方法
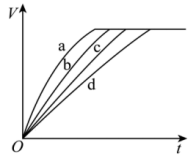
4 . 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定反应过程中产生氢气体积V的数据如图所示,下列说法正确的是
实验组别 |
| 温度/℃ | 形((Fe) |
Ⅰ | 2.0 | 30 | 块状 |
Ⅱ | 2.5 | 30 | 块状 |
Ⅲ | 2.5 | 50 | 粉末状 |
Ⅳ | 2.5 | 50 | 块状 |
A.该反应的离子方程式为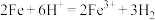 |
| B.对比实验Ⅰ、Ⅱ可探究浓度对化学反应速率的影响 |
| C.对比实验Ⅱ、Ⅲ可探究温度对化学反应速率的影响 |
| D.曲线a、b、c、d对应的实验组别分别为Ⅳ、Ⅲ、Ⅱ、Ⅰ |
您最近一年使用:0次
名校
5 . 在锌与某浓度的稀盐酸(足量)反应的实验中,得到如下结果:
下列说法中正确的是
① ②
② 和
和 均小于200 ③实验2和实验3比较,单位时间内消耗的锌的质量
均小于200 ③实验2和实验3比较,单位时间内消耗的锌的质量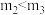 ④若锌均未完全反应,则在相同时间内,产生
④若锌均未完全反应,则在相同时间内,产生 的体积
的体积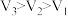
| 序号 | 锌的质量/g | 锌的形式 | 温度/℃ | 锌完全反应所需时间/s | 产生 的体积 的体积 |
| 1 | 2 | 薄片 | 15 | 200 |  |
| 2 | 2 | 粉末 | 15 |  |  |
| 3 | 2 | 粉末 | 35 |  |  |
①
 ②
② 和
和 均小于200 ③实验2和实验3比较,单位时间内消耗的锌的质量
均小于200 ③实验2和实验3比较,单位时间内消耗的锌的质量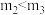 ④若锌均未完全反应,则在相同时间内,产生
④若锌均未完全反应,则在相同时间内,产生 的体积
的体积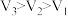
| A.①② | B.①②③ | C.②③④ | D.①②③④ |
您最近一年使用:0次
名校
解题方法
6 . 下列事实或做法与化学反应速率无关的是
| A.加热金属钠制备过氧化钠 | B.用铁触媒作催化剂合成氨 |
| C.将煤块粉碎后燃烧 | D.将食物存放在温度低的地方 |
您最近一年使用:0次
解题方法
7 . 某课外兴趣小组利用硫代硫酸钠(Na2S2O3)与稀硫酸反应探究影响化学反应速率的因素[反应方程式为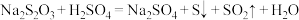 ],设计了如表系列实验。下列说法不正确的是
],设计了如表系列实验。下列说法不正确的是
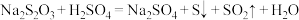 ],设计了如表系列实验。下列说法不正确的是
],设计了如表系列实验。下列说法不正确的是| 实验序号 | 反应温度(℃) | Na2S2O3 | 稀硫酸 | H2O | ||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
| 1 | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| 2 | 40 | V1 | 0.10 | 10.0 | 0.50 | V2 |
| 3 | 20 | V3 | 0.10 | 4.0 | 0.50 | V4 |
| A.设计该实验的基本原理为控制变量法 |
| B.实验1和2可探究温度对反应速率的影响 |
C.若用实验1和3探究稀硫酸浓度对该反应速率的影响,则需 , , |
| D.本实验可通过比较浑浊现象出现所需时间的长短来判断反应进行的快慢 |
您最近一年使用:0次
8 . 用含铁废铜制备胆矾的流程如图所示,下列说法错误 的是

| A.“溶解”时延长浸泡时间,可以提高铜的浸出速率 |
B.流程中 可用 可用 代替 代替 |
C. 时, 时, |
| D.“系列操作”是指蒸发浓缩,冷却结晶,过滤,洗涤,干燥 |
您最近一年使用:0次
名校
解题方法
9 . 我国最新型055型万吨驱逐舰上使用了最新一代国产有源相控阵雷达,采用了最先进的氮化镓( )半导体技术。某工厂利用铝土矿(主要成分为
)半导体技术。某工厂利用铝土矿(主要成分为 、
、 、
、 )为原料制备
)为原料制备 的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应,
的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应, 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 )半导体技术。某工厂利用铝土矿(主要成分为
)半导体技术。某工厂利用铝土矿(主要成分为 、
、 、
、 )为原料制备
)为原料制备 的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应,
的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应, 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是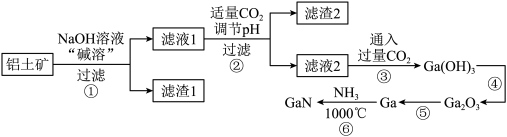
| A.可以通过粉碎铝土矿、搅拌等方法提高“碱溶”效率 |
B.由过程②、③可知, 的酸性比 的酸性比 强 强 |
C.已知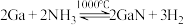 , , 与足量 与足量 反应,转移电子数为 反应,转移电子数为 |
D.滤渣1是 ,生成滤渣2的离子方程式可能为 ,生成滤渣2的离子方程式可能为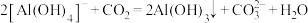 |
您最近一年使用:0次
2024-05-12更新
|
249次组卷
|
2卷引用:安徽师范大学附属中学2024届高三下学期5月测试化学试卷
名校
解题方法
10 . 为了探究温度和浓度对化学反应速率的影响,某同学设计了如下实验:在一张白纸上用黑色记号笔在合适的位置画上三个粗细、深浅一致的“十”字,分别在“十”字上放锥形瓶;按照表格中的试剂和条件进行反应Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,随着反应的进行,锥形瓶底部的“十”字会被遮盖。下列说法错误的是
| 实验序号 | 反应温度/℃ | Na2S2O3溶液 | 硫酸 | H2O | ||
| V/mL | c/(mol·L-1) | V/mL | c/(mol·L-1) | V/mL | ||
| Ⅰ | 20 | 10.0 | 0.10 | 10.0 | 0.10 | 0 |
| Ⅱ | 20 | 5.0 | 0.10 | 10.0 | 0.10 | V1 |
| Ⅲ | 40 | 10.0 | 0.10 | 10.0 | 0.10 | V2 |
| A.V1=0,V2=5.0 |
| B.实验还需要秒表,用于测定锥形瓶底部的“十”字完全被遮盖所需的时间 |
C.锥形瓶内发生反应的离子方程式 +2H+= SO2↑+S↓+H2O +2H+= SO2↑+S↓+H2O |
| D.进行实验Ⅲ时,应分别将Na2S2O3溶液和硫酸加热至40℃,然后在锥形瓶内混合 |
您最近一年使用:0次