上海财经大学附属北郊高级中学2023-2024学年高三上学期开学考试化学试题
上海
高三
开学考试
2023-11-06
108次
整体难度:
适中
考查范围:
认识化学科学、化学反应原理、有机化学基础、化学实验基础
上海财经大学附属北郊高级中学2023-2024学年高三上学期开学考试化学试题
上海
高三
开学考试
2023-11-06
108次
整体难度:
适中
考查范围:
认识化学科学、化学反应原理、有机化学基础、化学实验基础
一、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
1. 某学习小组进行实验探究 溶液和
溶液和 溶液的反应原理。已知:
溶液的反应原理。已知:
①和FeS均为黑色、不溶于水,能溶于酸的固体, 固体常温下易转变为黄绿色。
固体常温下易转变为黄绿色。
② 近似数据:
近似数据: 为
为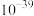 ,
, 为
为 ,FeS为
,FeS为 。
。
(1) 的电子式为
的电子式为_______ ;常温下,0.1
 溶液pH=13的原因是
溶液pH=13的原因是_______ (用离子方程式表示),该溶液中水的电离程度是相同温度下纯水的_______ 倍。
(2)配制 溶液时,先将
溶液时,先将 晶体溶于浓盐酸,再稀释至指定浓度。结合平衡移动原理说明浓盐酸的作用
晶体溶于浓盐酸,再稀释至指定浓度。结合平衡移动原理说明浓盐酸的作用_______ 。
学习小组尝试结合相关原理预测产物。
(3)甲同学依据酸碱理论的相关知识预测 与
与 可能发生双水解生成
可能发生双水解生成 ,则该反应的离子方程式可以表示为
,则该反应的离子方程式可以表示为_______ 。
(4)乙同学依据难溶电解质的溶解平衡理论的相关知识预测反应主要产生 而不是
而不是 。理由是
。理由是_______ 。
(5)丙同学依据氧化还原反应理论的相关知识预测 溶液与
溶液与 溶液反应可生成FeS和S的混合物,则反应的离子方程式为
溶液反应可生成FeS和S的混合物,则反应的离子方程式为_______ 。
学习小组进行实验,探究反应生成沉淀物的成分。
实验一:

实验二:

(6)乙同学设计实验证明试管①中黑色物质含有 ,该同学的实验操作为
,该同学的实验操作为_______ 。
(7)丙同学将试管②中黑色沉淀过滤洗涤后溶解于稀硫酸,获得淡黄色悬浊液并闻到臭鸡蛋气味,判断沉淀为FeS和S的混合物,但甲同学认为此判断不合理,请说明理由:_______ 。
(8)由上述实验可知, 溶液与
溶液与 溶液间可发生复分解反应也可发生氧化反应,且反应的产物、实验的现象与等有关
溶液间可发生复分解反应也可发生氧化反应,且反应的产物、实验的现象与等有关_______ (写出一条即可)。
 溶液和
溶液和 溶液的反应原理。已知:
溶液的反应原理。已知:①和FeS均为黑色、不溶于水,能溶于酸的固体,
 固体常温下易转变为黄绿色。
固体常温下易转变为黄绿色。②
 近似数据:
近似数据: 为
为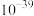 ,
, 为
为 ,FeS为
,FeS为 。
。(1)
 的电子式为
的电子式为
 溶液pH=13的原因是
溶液pH=13的原因是(2)配制
 溶液时,先将
溶液时,先将 晶体溶于浓盐酸,再稀释至指定浓度。结合平衡移动原理说明浓盐酸的作用
晶体溶于浓盐酸,再稀释至指定浓度。结合平衡移动原理说明浓盐酸的作用学习小组尝试结合相关原理预测产物。
(3)甲同学依据酸碱理论的相关知识预测
 与
与 可能发生双水解生成
可能发生双水解生成 ,则该反应的离子方程式可以表示为
,则该反应的离子方程式可以表示为(4)乙同学依据难溶电解质的溶解平衡理论的相关知识预测反应主要产生
 而不是
而不是 。理由是
。理由是(5)丙同学依据氧化还原反应理论的相关知识预测
 溶液与
溶液与 溶液反应可生成FeS和S的混合物,则反应的离子方程式为
溶液反应可生成FeS和S的混合物,则反应的离子方程式为学习小组进行实验,探究反应生成沉淀物的成分。
实验一:

实验二:

(6)乙同学设计实验证明试管①中黑色物质含有
 ,该同学的实验操作为
,该同学的实验操作为(7)丙同学将试管②中黑色沉淀过滤洗涤后溶解于稀硫酸,获得淡黄色悬浊液并闻到臭鸡蛋气味,判断沉淀为FeS和S的混合物,但甲同学认为此判断不合理,请说明理由:
(8)由上述实验可知,
 溶液与
溶液与 溶液间可发生复分解反应也可发生氧化反应,且反应的产物、实验的现象与等有关
溶液间可发生复分解反应也可发生氧化反应,且反应的产物、实验的现象与等有关
您最近一年使用:0次
2023-09-04更新
|
200次组卷
|
3卷引用:上海财经大学附属北郊高级中学2023-2024学年高三上学期开学摸底评估化学试题
2. 实验室常用如下左装置制取溴乙烷。在圆底烧瓶中加入溴化钠、浓 、乙醇和适量的水,加热可收集到溴乙烷。所涉及的有关物质的物理性质见下表:
、乙醇和适量的水,加热可收集到溴乙烷。所涉及的有关物质的物理性质见下表:

(1)写出有机化合物所含官能团名称。溴乙烷:_______ ;乙醇:_______ 。
(2)完成用此法制备溴乙烷的反应式:
① ;
;
②_______ 
_______ 。
其中反应②是一个可逆反应,在实验中采取的措施_______ (任写一种),以提高溴乙烷的产率。
(3)反应时若温度过高,可看到有红棕色气体产生,其成分为_______ (写分子式)。为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是_______ 。
(4)反应物中加入适量水,除了溶解NaBr使反应物接触更充分外,还可以_______ (双选)。
a.降低硫酸浓度,减少副反应 b.减少HBr的挥发
c.使反应混合物分层 d.防止反应体系温度过高
(5)烧瓶中除了加入反应物外,还需加入几片碎瓷片,目的是_______ 。实验进行的途中若发现未加入碎瓷片,正确的处理方法是_______ 。
(6)下列最适宜作为溴乙烷收集装置的是_______ 。
(7)制得的粗溴乙烷中会含有少量 而呈黄色,可先用
而呈黄色,可先用 溶液洗涤,再水洗干燥后
溶液洗涤,再水洗干燥后_______ (填操作名称)。洗涤过程用到的主要玻璃仪器是_______ 。
(8)完成 溶液洗涤时发生反应的离子方程式并标明电子转移方向和数目:
溶液洗涤时发生反应的离子方程式并标明电子转移方向和数目:_______ 。
 _______
_______
(9)能否改用NaOH溶液洗涤粗溴乙烷?说明原因_______ 。
(10)检验溴乙烷官能团的正确操作顺序是:取少量溴乙烷,然后_______ (填代号)。
①加热;②加入 溶液;③加入稀
溶液;③加入稀 酸化;④加入NaOH溶液;⑤冷却
酸化;④加入NaOH溶液;⑤冷却
 、乙醇和适量的水,加热可收集到溴乙烷。所涉及的有关物质的物理性质见下表:
、乙醇和适量的水,加热可收集到溴乙烷。所涉及的有关物质的物理性质见下表:
| 乙醇 | 溴乙烷 | |
| 沸点(℃) | 78 | 38.4 |
密度( ) ) | 0.79 | 1.45 |
| 水溶性 | 互溶 | 不溶 |
(2)完成用此法制备溴乙烷的反应式:
①
 ;
;②

其中反应②是一个可逆反应,在实验中采取的措施
(3)反应时若温度过高,可看到有红棕色气体产生,其成分为
(4)反应物中加入适量水,除了溶解NaBr使反应物接触更充分外,还可以
a.降低硫酸浓度,减少副反应 b.减少HBr的挥发
c.使反应混合物分层 d.防止反应体系温度过高
(5)烧瓶中除了加入反应物外,还需加入几片碎瓷片,目的是
(6)下列最适宜作为溴乙烷收集装置的是
 | 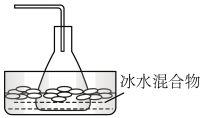 | 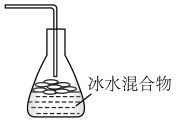 |  |
| a | b | c | d |
 而呈黄色,可先用
而呈黄色,可先用 溶液洗涤,再水洗干燥后
溶液洗涤,再水洗干燥后(8)完成
 溶液洗涤时发生反应的离子方程式并标明电子转移方向和数目:
溶液洗涤时发生反应的离子方程式并标明电子转移方向和数目: _______
_______
(9)能否改用NaOH溶液洗涤粗溴乙烷?说明原因
(10)检验溴乙烷官能团的正确操作顺序是:取少量溴乙烷,然后
①加热;②加入
 溶液;③加入稀
溶液;③加入稀 酸化;④加入NaOH溶液;⑤冷却
酸化;④加入NaOH溶液;⑤冷却
您最近一年使用:0次
2023-09-04更新
|
202次组卷
|
2卷引用:上海财经大学附属北郊高级中学2023-2024学年高三上学期开学摸底评估化学试题



