2017届江西师大附中高三12月月考化学试卷
江西
高三
阶段练习
2017-07-27
242次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、物质结构与性质、化学反应原理、常见无机物及其应用
2017届江西师大附中高三12月月考化学试卷
江西
高三
阶段练习
2017-07-27
242次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、物质结构与性质、化学反应原理、常见无机物及其应用
一、未知 添加题型下试题
未知-未知
|
容易(0.94)
1. 化学与生活密切相关,下列说法不正确的是
| A.煤、石油、天然气是不可再生能源,风能、生物质能、沼气是可再生能源 |
| B.“84消毒液”具有强氧化性,可做环境的消毒剂从而预防流感 |
| C.已知水热反应是指在高温高压下,将二氧化碳转化为有机物的技术,则水热反应可以降低自然界中碳的含量 |
| D.已知PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为“细颗粒物”,则PM2.5在空气中有可能形成胶体 |
【知识点】 化学与环境保护
您最近一年使用:0次
二、单选题 添加题型下试题
单选题
|
容易(0.94)
2. 某硫原子的质量是ag,一个12C原子的质量是bg,若NA只表示阿伏伽德罗常数的数值,则下列说法中正确的是
①该硫原子的相对原子质量为12a/b
②m g该硫原子的物质的量为m/aNAmol
③该硫原子的摩尔质量是aNAg/mol
④ag该硫原子所含的电子数为16
⑤cg 该硫原子所含质子数为4bcNA/3a
①该硫原子的相对原子质量为12a/b
②m g该硫原子的物质的量为m/aNAmol
③该硫原子的摩尔质量是aNAg/mol
④ag该硫原子所含的电子数为16
⑤cg 该硫原子所含质子数为4bcNA/3a
| A.①②③④⑤ | B.①②③④ | C.①②④⑤ | D.①③④⑤ |
【知识点】 化学计量
您最近一年使用:0次
单选题
|
较易(0.85)
名校
3. 元素周期律揭示了元素间的递变规律,下列递变规律正确的是
| A.ⅣA族元素氢化物沸点:SiH4>CH4,所以ⅤA族元素氢化物沸点:PH3>NH3 |
| B.第二周期元素氢化物稳定性:HF>H2O,所以第三周期元素氢化物稳定性:HCl>H2S |
| C.ⅦA族元素的非金属性:F>Cl,所以ⅦA族元素氢化物的酸性:HF>HCl |
| D.镁比铝活泼,工业上用电解熔融氧化铝制铝,所以工业上也用电解熔融氧化镁制镁 |
【知识点】 元素周期律的应用 类比预测在推断中的应用解读
您最近一年使用:0次
2017-01-05更新
|
311次组卷
|
3卷引用:2017届江西师大附中高三12月月考化学试卷
三、未知 添加题型下试题
未知-未知
|
容易(0.64)
4. 短周期主族元素X 、Y 、Z、W的原子序数依次增大,X原子核外最外层电子数是次外层的2倍,Y的氟化物YF3分子中各原子均达到8电子稳定结构,Z是同周期中原子半径最大的元素,W的最高正价为+7价.下列说法正确的是( )
| A.简单离子半径大小顺序:rW>rZ>rY |
| B.元素W的氧化物对应水化物的酸性比Y 的强 |
| C.X与Y形成的原子晶体X3Y4的熔点可能比金刚石高 |
| D.X与W形成的化合物和Z与W形成的化合物的化学键类型相同 |
【知识点】 元素周期表 元素周期律
您最近一年使用:0次
四、单选题 添加题型下试题
单选题
|
适中(0.64)
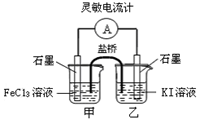
5. 控制适当的条件,将反应2Fe3++2I-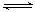 2Fe2++I2设计成如图所示的原电池。下列判断正确的是
2Fe2++I2设计成如图所示的原电池。下列判断正确的是
 2Fe2++I2设计成如图所示的原电池。下列判断正确的是
2Fe2++I2设计成如图所示的原电池。下列判断正确的是
| A.反应开始时,乙中电极反应为2I-+2e-="=" I2 |
| B.反应开始时,甲中石墨电极上发生氧化反应 |
| C.电流表指针为零时,两池溶液颜色相同 |
| D.平衡时甲中溶入FeCl2固体后,乙池的石墨电极为正极 |
【知识点】 原电池
您最近一年使用:0次
2016-12-09更新
|
482次组卷
|
3卷引用:2015届甘肃省天水市高三一轮复习基础知识检测化学试卷
单选题
|
容易(0.94)
名校
解题方法
6. 科学家用氮化镓材料与铜组装成如图所示的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4。下列关于该电池叙述错误的是
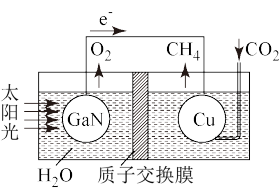

| A.电池工作时,是将太阳能转化为电能 |
| B.铜电极为正极,电极反应式为:CO2+8e-+8H+=CH4+2H2O |
| C.电池内部H+透过质子交换膜从左向右移动 |
| D.为提高该人工光合系统的工作效率,可向装置中加入少量硝酸溶液 |
您最近一年使用:0次
2017-01-05更新
|
511次组卷
|
3卷引用:2017届江西师大附中高三12月月考化学试卷
五、未知 添加题型下试题
未知-未知
|
较易(0.64)
7. 甲~辛等元素在周期表中的相对位置如下表。甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素。下列判断正确的是( )


| A.金属性:甲>乙>丁 |
| B.原子半径:己>辛>戊 |
| C.丙和庚的原子核外电子数相差13 |
| D.乙的单质在空气中燃烧生成只含离子键的化合物 |
【知识点】 元素周期表 元素周期律
您最近一年使用:0次
未知-未知
|
容易(0.4)
8. 下列说法正确的是
| A.甲烷的燃烧热为ΔH=-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
| B.已知H2O(l)=H2O(g) ΔH=+44kJ·mol-1,则2g H2(g)完全燃烧生成液态水比生成气态水多释放22kJ的能量 |
| C.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的ΔH<0 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的ΔH相同 |
【知识点】 反应热
您最近一年使用:0次
未知-未知
|
容易(0.4)
9. 某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2=2H2O,下列有关说法正确的是


| A.电子通过外电路从b极流向a极 |
| B.b极上的电极反应式为:O2+2H2O+4e--=4OH-- |
| C.每转移0.1mol电子,消耗1.12L的H2 |
| D.H+由a极通过固体酸电解质传递到b极 |
【知识点】 化学电源
您最近一年使用:0次
六、单选题 添加题型下试题
单选题
|
适中(0.64)
10. 通常人们把拆开1mol某化学键所消耗的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H),化学反应的△H等于反应物的总键能与生成物的总键能之差。工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g) Si(s)+4HCl(g),该反应的反应热△H为
Si(s)+4HCl(g),该反应的反应热△H为

 Si(s)+4HCl(g),该反应的反应热△H为
Si(s)+4HCl(g),该反应的反应热△H为
| A.+412kJ/mol | B.-412kJ/mol | C.+236kJ/mol | D.-236kJ/mol |
【知识点】 化学反应热的计算
您最近一年使用:0次



