浙江省2018版考前特训(2017年10月)加试30分特训:6 化学实验的测定、设计及评价
浙江
高三
专题练习
2017-08-14
102次
整体难度:
适中
考查范围:
常见无机物及其应用、化学实验基础、有机化学基础
浙江省2018版考前特训(2017年10月)加试30分特训:6 化学实验的测定、设计及评价
浙江
高三
专题练习
2017-08-14
102次
整体难度:
适中
考查范围:
常见无机物及其应用、化学实验基础、有机化学基础
一、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
1. ClO2是一种优良的消毒剂,浓度过高时易发生分解,常将其制成NaClO2固体,以便运输和贮存。过氧化氢法制备NaClO2固体的实验装置如图所示。请回答:
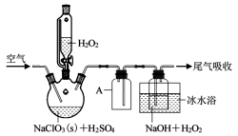
已知:2NaClO3+H2O2+H2SO4===2ClO2↑+O2↑+Na2SO4+2H2O
2ClO2+H2O2+2NaOH===2NaClO2+O2↑+2H2O
ClO2熔点-59℃、沸点11℃;H2O2沸点150℃
(1)仪器A的作用是______________________ ;
冰水浴冷却的目的是___________________ (写两种)。
(2)空气流速过快或过慢,均降低NaClO2产率,试解释其原因______________________ 。
(3)Clˉ存在时会催化ClO2的生成。反应开始时在三颈烧瓶中加入少量盐酸,ClO2的生成速率大大提高,并产生微量氯气。该过程可能经两步反应完成,将其补充完整:①____________________________ (用离子方程式表示),②H2O2+Cl2===2Clˉ+O2+2H+。(4)H2O2浓度对反应速率有影响。通过图所示装置将少量30%H2O2溶液浓缩至40%,B处应增加一个设备。该设备的作用是_________ ,馏出物是_________ 。
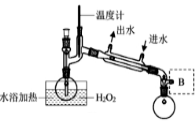
(5)抽滤法分离NaClO2过程中,下列操作不正确的是_______ 。
A.为防止滤纸被腐蚀,用玻璃纤维代替滤纸进行抽滤
B.先转移溶液至漏斗,待溶液快流尽时再转移沉淀
C.洗涤沉淀时,应使洗涤剂快速通过沉淀
D.抽滤完毕,断开水泵与吸滤瓶间的橡皮管后,关闭水龙头

已知:2NaClO3+H2O2+H2SO4===2ClO2↑+O2↑+Na2SO4+2H2O
2ClO2+H2O2+2NaOH===2NaClO2+O2↑+2H2O
ClO2熔点-59℃、沸点11℃;H2O2沸点150℃
(1)仪器A的作用是
冰水浴冷却的目的是
(2)空气流速过快或过慢,均降低NaClO2产率,试解释其原因
(3)Clˉ存在时会催化ClO2的生成。反应开始时在三颈烧瓶中加入少量盐酸,ClO2的生成速率大大提高,并产生微量氯气。该过程可能经两步反应完成,将其补充完整:①

(5)抽滤法分离NaClO2过程中,下列操作不正确的是
A.为防止滤纸被腐蚀,用玻璃纤维代替滤纸进行抽滤
B.先转移溶液至漏斗,待溶液快流尽时再转移沉淀
C.洗涤沉淀时,应使洗涤剂快速通过沉淀
D.抽滤完毕,断开水泵与吸滤瓶间的橡皮管后,关闭水龙头
您最近一年使用:0次
2017-08-13更新
|
633次组卷
|
3卷引用:浙江省2018版考前特训(2017年10月)加试30分特训:6 化学实验的测定、设计及评价
解答题-实验探究题
|
适中(0.65)
名校
2. 硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁。硫酸亚铁铵在500℃时隔绝空气加热完全分解。回答下列问题:
(1)硫酸亚铁铵隔绝空气加热完全分解,发生了氧化还原反应,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO 3、H2O、N2和
3、H2O、N2和__________ 。
(2)为检验分解产物的成分,设计如下实验装置进行实验,加热A中的硫酸亚铁铵至分解完全。
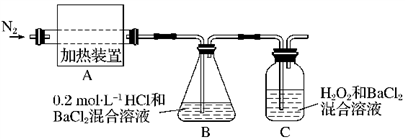
①A中固体充分加热较长时间后,通入氮气,目的是__________________________ 。
②为验证A中残留物是否含有FeO,需要选用的试剂有____________ (填字母)。
A.KSCN溶液B.稀硫酸
C.浓盐 酸D.KMnO4溶液
酸D.KMnO4溶液
③装置B中BaCl2溶液的作用是为了检验分解产物中是否有________ 气体生成,若含有该气体,观察到的现象为_______________________________________ 。
④若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为b mol,C中沉淀物质的量为a mol,则b________________ (填“大于”“小于”或“等于”)a。
⑤实验中,观察到C中有白色沉淀生成,则C中发生的反应为___________________________________________ (用离子方程式表示)。
(3)为测定某固体样品中(NH4)2Fe(SO4)2·6H2O的含量,某实验小组做了如下实验:
测定原理:MnO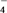 +Fe2++H+―→Mn2++Fe3++H2O(方程式未配平)
+Fe2++H+―→Mn2++Fe3++H2O(方程式未配平)
测定步骤:步骤一:准确称量20.00 g硫酸亚铁铵晶体,配制成100 mL溶液。
步骤二:取所配溶液25.00 mL于锥形瓶中,加稀H2SO4酸化,用0.100 0 mol·L-1KMnO4溶液滴定至终点,重复两次,平均消耗KMnO4溶液16.00 mL。
①如何判断滴定终点?________________________ ;
②产品中(NH4)2Fe(SO4)2·6H2O的质量分数为_________________ 。
(1)硫酸亚铁铵隔绝空气加热完全分解,发生了氧化还原反应,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO
 3、H2O、N2和
3、H2O、N2和(2)为检验分解产物的成分,设计如下实验装置进行实验,加热A中的硫酸亚铁铵至分解完全。

①A中固体充分加热较长时间后,通入氮气,目的是
②为验证A中残留物是否含有FeO,需要选用的试剂有
A.KSCN溶液B.稀硫酸
C.浓盐
 酸D.KMnO4溶液
酸D.KMnO4溶液③装置B中BaCl2溶液的作用是为了检验分解产物中是否有
④若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为b mol,C中沉淀物质的量为a mol,则b
⑤实验中,观察到C中有白色沉淀生成,则C中发生的反应为
(3)为测定某固体样品中(NH4)2Fe(SO4)2·6H2O的含量,某实验小组做了如下实验:
测定原理:MnO
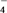 +Fe2++H+―→Mn2++Fe3++H2O(方程式未配平)
+Fe2++H+―→Mn2++Fe3++H2O(方程式未配平)测定步骤:步骤一:准确称量20.00 g硫酸亚铁铵晶体,配制成100 mL溶液。
步骤二:取所配溶液25.00 mL于锥形瓶中,加稀H2SO4酸化,用0.100 0 mol·L-1KMnO4溶液滴定至终点,重复两次,平均消耗KMnO4溶液16.00 mL。
①如何判断滴定终点?
②产品中(NH4)2Fe(SO4)2·6H2O的质量分数为
您最近一年使用:0次
2016-12-09更新
|
952次组卷
|
6卷引用:2017届浙江省温州中学高三上10月高考模拟化学试卷



