2018届高三一轮复习化学:微考点20-铁及其化合物的实验探究
全国
高三
学业考试
2017-09-25
64次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学反应原理、化学实验基础
2018届高三一轮复习化学:微考点20-铁及其化合物的实验探究
全国
高三
学业考试
2017-09-25
64次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、化学反应原理、化学实验基础
一、填空题 添加题型下试题
填空题
|
适中(0.65)
解题方法
1. 铁是目前人类使用量最大的金属,它能形成多种化合物。
(1)取5.6 g的生铁与足量的稀硫酸混合反应,无论怎样进行实验,最终收集的气体体积均小于2.24 L(标准状况),最主要的原因是_____________________ ;所得溶液在长时间放置过程中会慢慢出现浅黄色,试用离子方程式解释这一变化的原因:___________ 。
(2)ZnFe2Ox是一种新型纳米材料,可将工业废气中的某些元素转化为游离态,制取纳米ZnFe2Ox和用于除去废气的转化关系为ZnFe2O4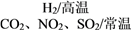 ZnFe2Ox。若上述转化反应中消耗的n(ZnFe2O4)∶n(H2)=2∶1,x的值为
ZnFe2Ox。若上述转化反应中消耗的n(ZnFe2O4)∶n(H2)=2∶1,x的值为________ 。请写出 ZnFe2Ox与NO2反应的化学方程式:_________________________ (x用前一问求出的具体值)。
(3)LiFePO4(难溶于水)材料被视为最有前途的锂离子电池材料之一。
①以 FePO4(难溶于水)、Li2CO3、单质碳为原料在高温下制备LiFePO4,该反应还生成一种可燃性气体,则反应的化学方程式为___________________________ 。
②磷酸铁锂动力电池有几种类型,其中一种(中间是锂离子聚合物的隔膜,它把正极与负极隔开)工作原理为FePO4+Li LiFePO4。则放电时正极上的电极反应式为
LiFePO4。则放电时正极上的电极反应式为___________________________________ 。
(4)已知25 ℃时Ksp[Fe(OH3)]=4.0×10-38,此温度下若在实验室中配制5 mol·L-1 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入______ mL 2 mol·L-1的盐酸(忽略加入盐酸时溶液体积的变化)。
(1)取5.6 g的生铁与足量的稀硫酸混合反应,无论怎样进行实验,最终收集的气体体积均小于2.24 L(标准状况),最主要的原因是
(2)ZnFe2Ox是一种新型纳米材料,可将工业废气中的某些元素转化为游离态,制取纳米ZnFe2Ox和用于除去废气的转化关系为ZnFe2O4
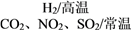 ZnFe2Ox。若上述转化反应中消耗的n(ZnFe2O4)∶n(H2)=2∶1,x的值为
ZnFe2Ox。若上述转化反应中消耗的n(ZnFe2O4)∶n(H2)=2∶1,x的值为(3)LiFePO4(难溶于水)材料被视为最有前途的锂离子电池材料之一。
①以 FePO4(难溶于水)、Li2CO3、单质碳为原料在高温下制备LiFePO4,该反应还生成一种可燃性气体,则反应的化学方程式为
②磷酸铁锂动力电池有几种类型,其中一种(中间是锂离子聚合物的隔膜,它把正极与负极隔开)工作原理为FePO4+Li
 LiFePO4。则放电时正极上的电极反应式为
LiFePO4。则放电时正极上的电极反应式为(4)已知25 ℃时Ksp[Fe(OH3)]=4.0×10-38,此温度下若在实验室中配制5 mol·L-1 100 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入
您最近一年使用:0次
填空题
|
适中(0.65)
2. 铁及其化合物在生产和生活中有广泛的应用。
(1)铁元素在元素周期表中的位置为________________ 。
(2)等物质的量的铁分别与足量的盐酸、水蒸气在一定条件下反应,产生相同条件下的气体体积比为__________ ;铁在高温条件下与水蒸气反应的化学方程式为______________________________________________________________ 。
(3)碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如图:
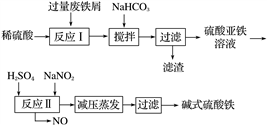
已知:常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
①加入少量NaHCO3的目的是调节pH,应控制pH的范围为____________ 。
②碱式硫酸铁溶于水后产生的[Fe(OH)]2+,可部分水解生成聚合离子[Fe2(OH)4]2+。该水解反应的离子方程式为_______________________________ 。
(4)高铁酸钾(K2FeO4)也是常用的水处理剂。它的制备方法有多种。
①熔融法又称为过氧化钠氧化法。先在高温熔融的条件下制备高铁酸钠:Fe+3Na2O2===Na2FeO4+2Na2O,再将高铁酸钠加入到氢氧化钾溶液里,发生反应:2KOH+Na2FeO4===K2FeO4+2NaOH,请根据复分解反应原理分析该反应发生的原因:_________________________________________________________________ 。
②电解法制备高铁酸钾。铁和石墨分别做两个电极的电极材料,氢氧化钠溶液做电解液实现电解制备。阴极的电极材料为__________ ,写出阳极的电极反应式为_______________________________________________________ 。
(1)铁元素在元素周期表中的位置为
(2)等物质的量的铁分别与足量的盐酸、水蒸气在一定条件下反应,产生相同条件下的气体体积比为
(3)碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如图:

已知:常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe3+ | Fe2+ | Al3+ |
| 开始沉淀(pH) | 2.3 | 7.5 | 3.4 |
| 完全沉淀(pH) | 3.2 | 9.7 | 4.4 |
①加入少量NaHCO3的目的是调节pH,应控制pH的范围为
②碱式硫酸铁溶于水后产生的[Fe(OH)]2+,可部分水解生成聚合离子[Fe2(OH)4]2+。该水解反应的离子方程式为
(4)高铁酸钾(K2FeO4)也是常用的水处理剂。它的制备方法有多种。
①熔融法又称为过氧化钠氧化法。先在高温熔融的条件下制备高铁酸钠:Fe+3Na2O2===Na2FeO4+2Na2O,再将高铁酸钠加入到氢氧化钾溶液里,发生反应:2KOH+Na2FeO4===K2FeO4+2NaOH,请根据复分解反应原理分析该反应发生的原因:
②电解法制备高铁酸钾。铁和石墨分别做两个电极的电极材料,氢氧化钠溶液做电解液实现电解制备。阴极的电极材料为
您最近一年使用:0次



