将2 mol/L A气体和1 mol/L B气体混合,并在一定条件下发生如下反应:2A(g)+B(g)  2C(g),若经2 s后测得C的浓度为0.6 mol•L-1,现有下列几种说法:
2C(g),若经2 s后测得C的浓度为0.6 mol•L-1,现有下列几种说法:
①用物质A表示的反应的平均速率为0.3 mol•L-1•s-1
②用物质B表示的反应的平均速率为0.6 mol•L-1•s-1
③2 s时物质A的转化率为70%
④2 s时物质B的浓度为0.7 mol•L-1
其中正确的是( )
 2C(g),若经2 s后测得C的浓度为0.6 mol•L-1,现有下列几种说法:
2C(g),若经2 s后测得C的浓度为0.6 mol•L-1,现有下列几种说法:①用物质A表示的反应的平均速率为0.3 mol•L-1•s-1
②用物质B表示的反应的平均速率为0.6 mol•L-1•s-1
③2 s时物质A的转化率为70%
④2 s时物质B的浓度为0.7 mol•L-1
其中正确的是( )
| A.①③ | B.②③ | C.①④ | D.②④ |
19-20高二上·江西南昌·期中 查看更多[1]
(已下线)【南昌新东方】2019 南昌十九中 高二上 期中.
更新时间:2020-04-17 00:25:07
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】某温度下,在2L恒容密闭容器中,加入3 molA 和2 mol B进行如下反应:3A(g)+2B(g) 4C(?)+2D(?)。反应5 min后达到平衡,测得反应前后的压强之比为25:26。下列说法不正确的是
4C(?)+2D(?)。反应5 min后达到平衡,测得反应前后的压强之比为25:26。下列说法不正确的是
 4C(?)+2D(?)。反应5 min后达到平衡,测得反应前后的压强之比为25:26。下列说法不正确的是
4C(?)+2D(?)。反应5 min后达到平衡,测得反应前后的压强之比为25:26。下列说法不正确的是A.该温度下,该反应的平衡常数表达式为K =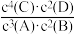 |
| B.该条件下反应到达平衡,v(A)=0.06mol/(L·min) |
| C.该条件下,在该容器中继续投入3 molA和2 mol B,反应物的转化率增大 |
| D.温度不变,增大压强,平衡向左移动,化学平衡常数K不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在容积不变的容器中充入CO和NO发生如下反应: ,其他条件不变时,分别探究温度和催化剂的比表面积对上述反应的影响。实验测得
,其他条件不变时,分别探究温度和催化剂的比表面积对上述反应的影响。实验测得 与时间的关系如图所示。
与时间的关系如图所示。

已知:ⅰ.起始投料比 均为2∶3;
均为2∶3;
ⅱ.比表面积:单位质量的物质具有的总面积。
下列说法不正确 的是
 ,其他条件不变时,分别探究温度和催化剂的比表面积对上述反应的影响。实验测得
,其他条件不变时,分别探究温度和催化剂的比表面积对上述反应的影响。实验测得 与时间的关系如图所示。
与时间的关系如图所示。
已知:ⅰ.起始投料比
 均为2∶3;
均为2∶3;ⅱ.比表面积:单位质量的物质具有的总面积。
下列说法
| A.Ⅰ、Ⅱ反应温度相同,催化剂的比表面积不同 |
| B.Ⅱ中NO的平衡转化率为75% |
C.在Ⅲ的条件下,该反应的平衡常数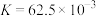 |
D.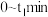 ,Ⅲ中平均反应速率 ,Ⅲ中平均反应速率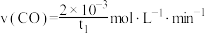 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】在恒温恒容的2L密闭容器中,充入4mol气体A和2mol气体B发生反应:3A(g)+2B(g) ⇌ 4C(?)+2D(?),反应5min后达到平衡,测得生成1.6molC,反应前后体系压强之比为5∶4。则下列说法正确的是
| A.气体A的平衡转化率大于气体B的平衡转化率 |
| B.物质D的聚集状态一定是气体 |
| C.平衡后C的物质的量浓度为0.8mol/L |
| D.从反应开始到平衡时用A表示的平均化学反应速率为0.24mol·L-1·min-1 |
您最近一年使用:0次
【推荐1】由γ˗羟基丁酸(HOCH2CH2CH2COOH)生成γ˗丁内酯( )的反应如下:HOCH2CH2CH2COOH
)的反应如下:HOCH2CH2CH2COOH
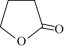 +H2O。在25°C时,溶液中γ˗羟基丁酸初始浓度为0.180mol/L,随着反应的进行,测得γ˗丁内酯的浓度随时间的变化如下表所示。下列说法中错误的是
+H2O。在25°C时,溶液中γ˗羟基丁酸初始浓度为0.180mol/L,随着反应的进行,测得γ˗丁内酯的浓度随时间的变化如下表所示。下列说法中错误的是
 )的反应如下:HOCH2CH2CH2COOH
)的反应如下:HOCH2CH2CH2COOH
 +H2O。在25°C时,溶液中γ˗羟基丁酸初始浓度为0.180mol/L,随着反应的进行,测得γ˗丁内酯的浓度随时间的变化如下表所示。下列说法中错误的是
+H2O。在25°C时,溶液中γ˗羟基丁酸初始浓度为0.180mol/L,随着反应的进行,测得γ˗丁内酯的浓度随时间的变化如下表所示。下列说法中错误的是| t/min | 21 | 50 | 80 | 100 | 120 | 160 | 220 | ∞ |
| c/(mol/L) | 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.116 | 0.132 |
| A.在120min时,γ˗羟基丁酸的转化率为50% |
| B.在50~80min内,以γ˗丁内酯的浓度变化表示的反应速率为0.0007mol/(L·min) |
| C.在25°C时,该反应的平衡常数为K=2.75 |
| D.为提高平衡时γ˗羟基丁酸的转化率,及时移出γ˗丁内酯平衡正向移动,加快反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】为了探究原电池工作原理,设计如图1装置,某离子浓度变化如图2所示(不考虑副反应)下列叙述错误的是
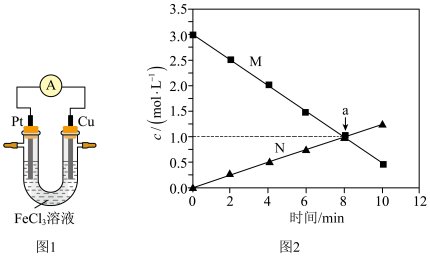
| A.图1中,铜极为负极,铂极发生还原反应 |
B.图2中,N代表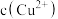 与时间的关系 与时间的关系 |
C.图1中,铂极电极反应式为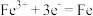 |
D.图2中,a点时 转化了约66.7% 转化了约66.7% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】t℃时,在恒容密闭容器中发生反应:X(g)+3Y(g) 2Z(g)ΔH,不同温度下容器中各组分浓度如下:
2Z(g)ΔH,不同温度下容器中各组分浓度如下:
已知:350℃时,反应经5min达到平衡状态。
下列说法不正确 的是
 2Z(g)ΔH,不同温度下容器中各组分浓度如下:
2Z(g)ΔH,不同温度下容器中各组分浓度如下:| 物质 | X | Y | Z | |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 | |
| 平衡浓度/mol·L-1 | 350℃ | 0.05 | 0.05 | 0.1 |
| 400℃ | 0.08 | 0.14 | 0.04 | |
下列说法
| A.该反应的ΔH<0 |
| B.350℃时,5min内该反应平均速率v(Y)=0.03mol·L-1·min-1 |
| C.350℃达到平衡后再通入少量Y(g),达到新平衡时,X转化率增大 |
| D.350℃时,该反应的平衡常数K=40 |
您最近一年使用:0次



