已知有A、B、C、D、E五种短周期的主族元素,它们的原子序数依次递增,A是所有元素中原子半径最小的元素,B、C组成的某一种化合物能引起温室效应。常温下,金属D单质投入水中能与水剧烈反应。常温下E单质是常见的气体。请按要求回答下列几个问题:
(1)B、D的元素名称分别为:________ 、________ 。
(2)E在周期表中的位置为:________ 。
(3)C离子的结构示意图为:________ 。
(4)B、C、D三种元素的原子半径从大到小的顺序为________ (用元素符号表示)。
(5)B、E的最高价氧化物对应水化物的酸性从强到弱的顺序为:________ (用对应的化学式表示)。
(6)写出C、D两种元素组成的阴、阳离子个数比为1:2且只含离子键的化合物的电子式:________ 。
(1)B、D的元素名称分别为:
(2)E在周期表中的位置为:
(3)C离子的结构示意图为:
(4)B、C、D三种元素的原子半径从大到小的顺序为
(5)B、E的最高价氧化物对应水化物的酸性从强到弱的顺序为:
(6)写出C、D两种元素组成的阴、阳离子个数比为1:2且只含离子键的化合物的电子式:
更新时间:2020-04-27 22:27:03
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】A、B、C、D、E为原子序数依次增大的短周期元素。已知A、B、E三原子最外层共有11个电子,且这三种元素的最高价氧化物对应水化物之间两两皆能反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。回答:
(1)写出元素符号:A___________ 、B___________ 、C___________ 、D___________ 、E___________ 。
(2)写出A、B两元素最高价氧化物对应水化物相互反应的化学方程式___________ 。A、E两元素最高价氧化物对应水化物相互反应的化学方程式___________ 。
(3)比较C、D最高价氧化物对应水化物的酸性___________ (用化学式表示)。
(1)写出元素符号:A
(2)写出A、B两元素最高价氧化物对应水化物相互反应的化学方程式
(3)比较C、D最高价氧化物对应水化物的酸性
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】某研究性学习小组设计实验探究元素周期律,如图所示。

(1)仪器a的名称是____________ ,加入的药品为稀硝酸;仪器b的名称是____________ ,加入的药品为碳酸钠固体;b中反应现象为___________ ,验证氮的非金属性比碳的___ (填“强”或“弱”)。
(2)c中装有硅酸钠溶液,c中反应现象为____ ,验证硅的非金属性比碳的___ (填“强”或“弱”)。
(3)结论:同一周期从左到右元素非金属性逐渐____ (填“增强”或“减弱”);同一主族从上到下元素非金属性逐渐_______ (填“增强”或“减弱”)。
(4)某同学考虑到稀硝酸的挥发,则应在装置b和c之间增加一个盛有_______ 试剂的洗气瓶。

(1)仪器a的名称是
(2)c中装有硅酸钠溶液,c中反应现象为
(3)结论:同一周期从左到右元素非金属性逐渐
(4)某同学考虑到稀硝酸的挥发,则应在装置b和c之间增加一个盛有
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】如图所示标出的是元素周期表的一部分元素,据图回答下列问题(用元素符号表示)。
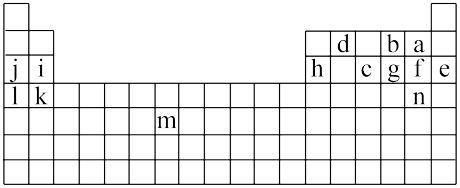
(1)图中用字母标出的14种元素中,金属性最强的是___ ,非金属性最强的是__ ,其单质的电子式___ 。
(2)b在周期表中的位置___ ,b、g气态氢化物中热稳定性最强的是___ ,结构式为___ 。
(3)j的最高价氧化物的水化物化学式___ ,该化合物中含有___ 键、___ 键,h与j的最高价氧化物的水化物反应的离子方程式___ 。

(1)图中用字母标出的14种元素中,金属性最强的是
(2)b在周期表中的位置
(3)j的最高价氧化物的水化物化学式
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D、E是周期表中五种常见的短周期元素,原子序数依次增大。C、D、E最高价氧化物对应的水化物两两均可以相互反应生成盐和水;A的原子序数与C的最外层电子数相同:B的氢化物水溶液显碱性;E的氢化物水溶液为强酸。回答下列问题:
(1) D在周期表中的位置是__________ ,写出D的氧化物与强酸反应的离子方程式:____________________
(2) B的氢化物呈碱性的原因:______________________________ (用方程式表示)
(3) 用电子式来表示化合物CE的形成过程:______________________________
(4) E的单质与A的一种氧化物反应生成具有漂白性的物质。有关反应的化学方程式为:________________________________________
(1) D在周期表中的位置是
(2) B的氢化物呈碱性的原因:
(3) 用电子式来表示化合物CE的形成过程:
(4) E的单质与A的一种氧化物反应生成具有漂白性的物质。有关反应的化学方程式为:
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】有A、B、C、D、E5种短周期元素,A与B可形成BA型化合物,A元素的单质常用于自来水消毒;金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8;C元素有3种同位素C1、C2、C3,自然界里含量最多的是C1,C3原子的质量数是C1的3倍,C2原子的质量数是C1的2倍;D的气态氢化物的水溶液呈碱性,而其最高价氧化物对应的水化物为强酸;E元素原子的最外层电子数比次外层电子数多4。
(1)写出下列元素的元素名称:A_________ ,B_________ 。
(2)写出C1、C3两种原子的符号:C1____________ ,C3___________ 。
(3)A、B、E形成的一种化合物是某种家用消毒液的有效成分,其电子式是___________ 。
(4)D的最高价氧化物的水化物与其氢化物反应形成化合物的化学式是___________ ,其所含化学键的类型是____________ ,由最常见的E原子与C2原子形成的最简单分子0.5mol中,所含中子的数目是___________ 。
(5)C、E的单质在碱性(KOH溶液)条件下可设计成一种燃料电池,其正极的电极反应式为_________ 。
(1)写出下列元素的元素名称:A
(2)写出C1、C3两种原子的符号:C1
(3)A、B、E形成的一种化合物是某种家用消毒液的有效成分,其电子式是
(4)D的最高价氧化物的水化物与其氢化物反应形成化合物的化学式是
(5)C、E的单质在碱性(KOH溶液)条件下可设计成一种燃料电池,其正极的电极反应式为
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】短周期元素A、B、C、D四种元素,它们的原子序数由A到D依次增大。在周期表中,A的原子半径最小。B元素的原子最外层电子数是内层电子数的两倍,C为地壳中含量最多的元素,D是第IA族元素,D单质燃烧时呈现黄色火焰,D的单质在加热下与C的单质充分反应生成E。试根据以上叙述回答:
(1)写出元素的符号:A___________ 、B___________ 、C___________ 、D___________ 。
(2)C在元素周期表中的位置:___________ 。
(3)写出E与CO2反应的化学方程式___________ 。
(1)写出元素的符号:A
(2)C在元素周期表中的位置:
(3)写出E与CO2反应的化学方程式
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】A、B、C、D 四种元素,原子序数依次增大,A 原子的最外层上有4个电子;B的阴离子和 C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)C离子的结构示意图为_____ 。D在周期表中位置_____ 。
(2)A、D两元素形成的化合物属_____ (填“离子”或“共价”)化合物。
(3)写出D的最高价氧化物的水化物和A单质反应的化学方程式:_____ 。
(4)B原子与氢原子形成的粒子中,与NH3具有相同电子数的阴离子为_____ (填化学式),阳离子为_____ (填化学式),其中阴离子的电子式为_____ 。
(5)写出B与氯元素和氢元素形成的氯水中含有的具有漂白性物质的结构式_____________
(1)C离子的结构示意图为
(2)A、D两元素形成的化合物属
(3)写出D的最高价氧化物的水化物和A单质反应的化学方程式:
(4)B原子与氢原子形成的粒子中,与NH3具有相同电子数的阴离子为
(5)写出B与氯元素和氢元素形成的氯水中含有的具有漂白性物质的结构式
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】A、B、C、D均为短周期元素,他们的原子序数依次增大,B是构成物质种类最多的元素,B和A组成的化合物 B6 A 6 是一种无色透明的液体,不溶于水,密度比水小,C 是地壳中含量最高的非金属元素,D 在同周期元素中原子半径最大。
(1)A、B、D 的元素名称分别为___________ 、____________ 、___________
(2)C 在元素周期表中位置为___________________ 。
(3)A、C、D 能组成多种不同的化合物,这些化合物中既含有极性共价键又含有离子键的化合物为_______________ (写电子式,下同),既含有非极性共价键又含有离子键的化合物为_________________ 。
(4)A 和 D 能组成一种化学活性很高的离子化合物 DA,DA 能和C的单质 C2反应生成一种强碱,请写出 DA 和 C2反应的化学方程式_________________________ 。
(1)A、B、D 的元素名称分别为
(2)C 在元素周期表中位置为
(3)A、C、D 能组成多种不同的化合物,这些化合物中既含有极性共价键又含有离子键的化合物为
(4)A 和 D 能组成一种化学活性很高的离子化合物 DA,DA 能和C的单质 C2反应生成一种强碱,请写出 DA 和 C2反应的化学方程式
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】短周期主族元素A、B、C、D、E的原子序数依次增大。已知:
①A原子最外层电子数是次外层电子数的两倍;B的阴离子与C的阳离子跟氖原于的电子层结构相同; B 与 D 同主族;
②常温下B2是气体,相同条件下它相对氢气的密度是16;
③C的单质能在B2中燃烧,生成淡黄色固体甲;
回答下列问题:
(1)A在元素周期表中的位置为___________ ;C的离子结构示意图为 ___________ ;E的最高价氧化物对应的水化物是 ___________ (填化学式);
(2)五种元素中,原子半径最大的是___________ (填元素符号);D、E的简单氢化物中热稳定性较差的是 ___________ (填化学式);
①A原子最外层电子数是次外层电子数的两倍;B的阴离子与C的阳离子跟氖原于的电子层结构相同; B 与 D 同主族;
②常温下B2是气体,相同条件下它相对氢气的密度是16;
③C的单质能在B2中燃烧,生成淡黄色固体甲;
回答下列问题:
(1)A在元素周期表中的位置为
(2)五种元素中,原子半径最大的是
您最近半年使用:0次



