汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3→K2O+5Na2O+16N2↑。若氧化物比还原物多1.75mol,则下列判断正确的是
| A.生成40.0LN2(标准状况) |
| B.有0.250molKNO3被氧化 |
| C.转移电子的物质的量为1.25mol |
| D.被氧化的N原子的物质的量为3.75mol |
更新时间:2020-04-30 15:28:19
|
【知识点】 氧化还原反应有关计算
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】做实验时不小心粘了一些高锰酸钾,皮肤上的斑很久才能消除,如果用草酸的稀溶液洗涤马上可以复原,其离子方程式为:2 +5
+5 +
+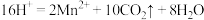 ,关于此反应的叙述正确的是
,关于此反应的叙述正确的是
 +5
+5 +
+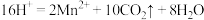 ,关于此反应的叙述正确的是
,关于此反应的叙述正确的是A.该反应的氧化剂是 |
B. 被还原, 被还原,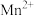 为氧化产物 为氧化产物 |
C.该反应电子转移总数是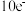 |
D.标准状况下生成11.2L的 ,电子转移了0.5mol ,电子转移了0.5mol |
您最近半年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】工业上从海水中制溴的步骤为:(I)先把盐卤加热到363K后控制pH为3.5,通入氯气把溴置换出来;(II)再用空气把溴吹出并用碳酸钠溶液吸收;(III)最后再用硫酸酸化,单质溴又从溶液中析出。其中,碳酸钠溶液吸收溴单质的反应可以分三步进行,其反应的机理如图所示。下列说法正确的是
第一步: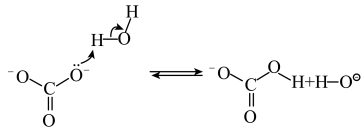
第二步: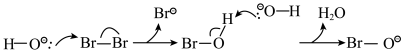
第三步: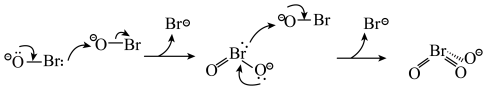
第一步:

第二步:
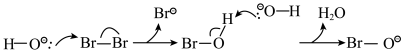
第三步:

A.1molH-O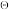 中含有的电子数为9NA 中含有的电子数为9NA |
| B.第二步反应为Br2在OH-中歧化,产生Br-和BrO- |
| C.当第(III)步产生1molBr2时则转移的电子数为2NA |
| D.该反应机理说明BrO-的稳定性较差 |
您最近半年使用:0次

 (C为
(C为 价)会与酸性
价)会与酸性 溶液发生如下反应:
溶液发生如下反应: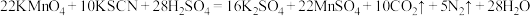 ,下列说法不正确的是
,下列说法不正确的是
 ,转移
,转移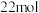 电子
电子 氧化为
氧化为 ,再加稍过量的
,再加稍过量的

