下列措施能加快Fe与0.1mol/L的稀H2SO4反应产生H2的反应速率的是( )
| A.增加Fe的用量 | B.降低温度 |
| C.将稀硫酸改为98%的浓硫酸 | D.滴加少量的CuSO4溶液 |
更新时间:2020-04-26 14:25:11
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快是
| A.不用稀硫酸,改用同浓度醋酸 | B.加热 |
| C.滴加少量CuSO4溶液 | D.不用铁片,改用铁粉 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】反应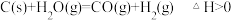 在一可变容积的密闭容器中进行,下列条件的改变能够增大其反应速率的是
在一可变容积的密闭容器中进行,下列条件的改变能够增大其反应速率的是
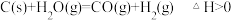 在一可变容积的密闭容器中进行,下列条件的改变能够增大其反应速率的是
在一可变容积的密闭容器中进行,下列条件的改变能够增大其反应速率的是| A.增加C(s)的物质的量 | B.保持体积不变,分离出部分CO和H2 |
| C.将容器的体积缩小一半 | D.保持容器体积不变,向其内充入一定量氦气 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】在铁和稀硫酸的反应中,下列方法可以加快其反应速率的是
| A.用铁钉代替铁粉 | B.加入少量氯化钠溶液 |
| C.用98%的浓硫酸代替稀硫酸 | D.适当升高反应温度 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】变量控制是科学研究的重要方法。相同质量的碳酸钙与足量不同浓度的酸分别在下列条件下发生反应,化学反应速率最大的是
| 选项 | 碳酸钙的状态 | 实验温度/℃ | 酸的浓度 |
| A | 块状 | 10 | 0.2mol·L-1H2SO4 |
| B | 粉末 | 30 | 0.2mol·L-1H2SO4 |
| C | 粉末 | 10 | 0.1mol·L-1HCl |
| D | 粉末 | 30 | 0.1mol·L-1HCl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】以海水为电解质溶液的水激活电池结构如图所示。下列说法不正确的是
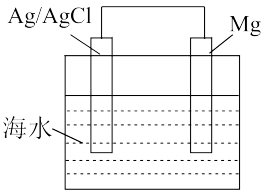

A.正极反应式是 |
B.海水中的 向镁电极移动 向镁电极移动 |
C.镁电极会发生副反应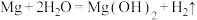 |
D.电池总反应是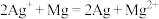 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。
锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s),
下列说法错误的是( )
锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s),
下列说法错误的是( )
| A.电池工作时,锌失去电子 |
| B.电池工作时,电子由负极通过外电路流向正极 |
| C.电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e-=Mn2O3(s)+2OH-(aq) |
| D.外电路中每通过0.4mol电子,锌的质量理论上减小6.5g |
您最近一年使用:0次



