某学习小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验,根据实验流程回答相关问题:
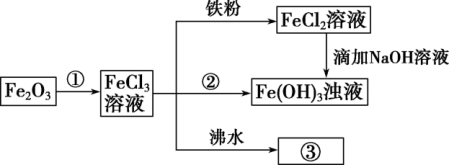
(1)请写出 Fe2O3与物质①反应的离子方程式:_____ 。
(2)检验溶液中 Fe3+是否存在的试剂是_____ (只写一种即可)。
(3)写出铁与 FeCl3溶液反应的离子方程式:_____ 。
(4)向FeCl2溶液中滴加NaOH 溶液最终生成Fe(OH)3浊液,该过程的现象为_____ ,此过程中 Fe(OH)2转化为 Fe(OH)3的反应为(用化学方程式表示)_____ 。

(1)请写出 Fe2O3与物质①反应的离子方程式:
(2)检验溶液中 Fe3+是否存在的试剂是
(3)写出铁与 FeCl3溶液反应的离子方程式:
(4)向FeCl2溶液中滴加NaOH 溶液最终生成Fe(OH)3浊液,该过程的现象为
更新时间:2020-05-11 08:27:56
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某同学利用某一金属元素不同价态间的相互转化,设计如图转化关系(部分物质未写出)。
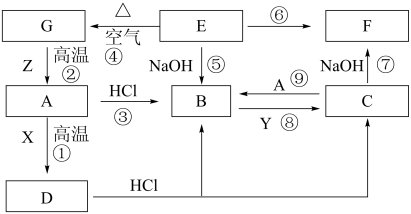
已知:①A是生活中应用最广泛的一种金属单质,A、B、C、D、E、F、G中均含有同一种元素;
②常温下,X是一种常见的液体,其分子是10e-分子;
③常温下,Y是一种黄绿色有毒气体,可用于自来水消毒;
④Z为地壳中含量最多的金属元素的单质。
请回答下列问题:
(1)A、B、F、X的化学式分别为A_______ , B_______ ,F_______ ,X_______ 。
(2)铸造工业上,液态A在注入模具前,必须将模具充分干燥,原因是_______ 。(用文字描述)
(3)上述反应中属于氧化还原反应的有_______ 个。
(4)由上述转化关系,分析实验室保存B的水溶液时通常加入少量A的目的是_______ ,若 B的水溶液因发生氧化还原反应而变质,加入KSCN溶液后,可观察到的现象为_______ 。
(5)选用下列装置_______ (填标号)能较长时间观察到E的颜色,不选用的装置中可观察到沉淀颜色变化情况为_______ 。


已知:①A是生活中应用最广泛的一种金属单质,A、B、C、D、E、F、G中均含有同一种元素;
②常温下,X是一种常见的液体,其分子是10e-分子;
③常温下,Y是一种黄绿色有毒气体,可用于自来水消毒;
④Z为地壳中含量最多的金属元素的单质。
请回答下列问题:
(1)A、B、F、X的化学式分别为A
(2)铸造工业上,液态A在注入模具前,必须将模具充分干燥,原因是
(3)上述反应中属于氧化还原反应的有
(4)由上述转化关系,分析实验室保存B的水溶液时通常加入少量A的目的是
(5)选用下列装置

您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下图表示各物质之间的转化关系,已知A、D、F、H均为单质,X常温下为无色液体,B为淡黄色固体,J溶于酸得到黄色溶液。
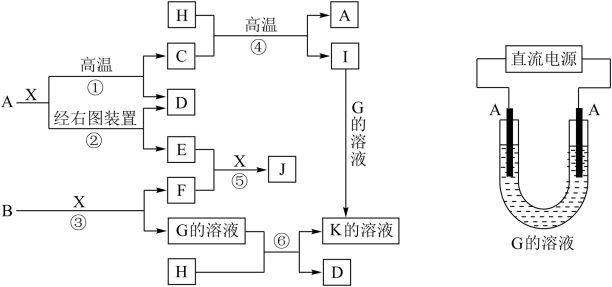
请按要求填空:
(1)写出B的电子式__________________________ 。
(2)写出生成E的电极反应式:___________________________________ 。
反应⑤的现象是_______________________________ 。
(3)反应①的化学方程式是__________________________ 。
在实验室中引发反应④的操作是______________________ 。
(4)反应⑥中若转移1 mol电子,则被还原的X是_____________ mol。

请按要求填空:
(1)写出B的电子式
(2)写出生成E的电极反应式:
反应⑤的现象是
(3)反应①的化学方程式是
在实验室中引发反应④的操作是
(4)反应⑥中若转移1 mol电子,则被还原的X是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】部分铁的化合物“价—类”二维关系如图所示。
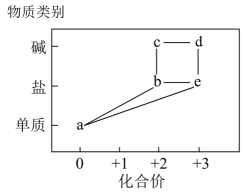
回答下列问题:
(1)c的化学式为___________ ,c放置在空气中可观察到现象有___________ 。
(2)硫酸盐b的溶液中含少量硫酸盐e,除去杂质的方法是___________ 。
(3)a→b的离子方程式为___________ 。
(4)在b中加入盐酸,产生无色无味气体,将该气体通入澄清石灰水中,溶液变浑浊。如果在空气中高温灼烧b,可得到红色粉末,写出b在空气中灼烧的化学方程式:___________ 。
(5)工业上,常用一氧化碳在高温下还原赤铁矿制备a,制备112kga时至少需要___________ LCO(标准状况),该反应中转移___________ mol电子。

回答下列问题:
(1)c的化学式为
(2)硫酸盐b的溶液中含少量硫酸盐e,除去杂质的方法是
(3)a→b的离子方程式为
(4)在b中加入盐酸,产生无色无味气体,将该气体通入澄清石灰水中,溶液变浑浊。如果在空气中高温灼烧b,可得到红色粉末,写出b在空气中灼烧的化学方程式:
(5)工业上,常用一氧化碳在高温下还原赤铁矿制备a,制备112kga时至少需要
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】磷酸亚铁锂是锂离子电池中常用的正极材料, (磷酸铁)是制备磷酸亚铁锂的前驱体。用磷铁渣(含Fe、FeP、
(磷酸铁)是制备磷酸亚铁锂的前驱体。用磷铁渣(含Fe、FeP、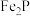 及
及 )制备
)制备 的工艺流程如下:
的工艺流程如下:
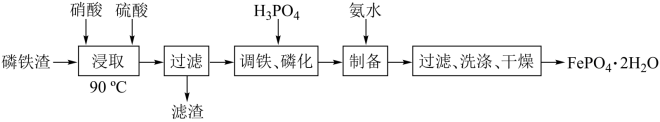
已知 溶于强酸。
溶于强酸。
(1)锂在元素周期表中的位置为___________ 。 的电离方程式为
的电离方程式为___________ 。
(2)“浸取”时,在密闭反应器中依次加入硝酸、硫酸,硝酸首先分解生成 和
和 ,
, 将铁和磷分别氧化为
将铁和磷分别氧化为 、
、 。
。
①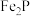 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
②加入硫酸的目的是___________ 。
(3)“制备”时发生反应的离子方程式为___________ ;上述流程制得的 中含有的杂质是
中含有的杂质是___________ 。
(4) 与
与 及C在高温条件下生成
及C在高温条件下生成 和等物质的量的
和等物质的量的 、CO,该反应中还原剂与氧化剂的物质的量之比为
、CO,该反应中还原剂与氧化剂的物质的量之比为___________ 。
 (磷酸铁)是制备磷酸亚铁锂的前驱体。用磷铁渣(含Fe、FeP、
(磷酸铁)是制备磷酸亚铁锂的前驱体。用磷铁渣(含Fe、FeP、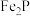 及
及 )制备
)制备 的工艺流程如下:
的工艺流程如下:
已知
 溶于强酸。
溶于强酸。(1)锂在元素周期表中的位置为
 的电离方程式为
的电离方程式为(2)“浸取”时,在密闭反应器中依次加入硝酸、硫酸,硝酸首先分解生成
 和
和 ,
, 将铁和磷分别氧化为
将铁和磷分别氧化为 、
、 。
。①
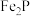 与
与 反应的化学方程式为
反应的化学方程式为②加入硫酸的目的是
(3)“制备”时发生反应的离子方程式为
 中含有的杂质是
中含有的杂质是(4)
 与
与 及C在高温条件下生成
及C在高温条件下生成 和等物质的量的
和等物质的量的 、CO,该反应中还原剂与氧化剂的物质的量之比为
、CO,该反应中还原剂与氧化剂的物质的量之比为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】金属镓被称为“电子工业脊梁”,今年8月1日,国家商务部开始对镓和锗两种金属进行出口管制,这一举措是对美国等国家对中国进行芯片技术封锁与5G技术打压的有力回应,展示了我国的自信和决心。GaN作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,GaN商用进入快车道。综合利用炼锌矿渣[主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4]获得3种金属盐,并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如下:

已知:常温下,浸出液中各离子形成氢氧化物沉淀的pH和金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表:
(1)GaN属于_____ 晶体;Ga2(Fe2O4)3中Fe的化合价为_____ 。
(2)处理浸出液时,将溶液的pH调节至5.4的主要目的是_____ 。
(3)“溶解还原”步骤中需要加入一定量的铁粉,进行该操作的主要目的是_____ 。
(4)Ga的化学性质与Al非常相似,“反萃取”后水溶液中镓元素主要以_____ (用离子符号表示)形式存在。
(5)“高温合成”操作中Ga(CH3)3与NH3反应生成GaN的化学方程式为_____ 。
(6)利用炼锌矿渣所获得的三种金属盐,分别为镓盐、FeCl2和_____ (用化学式表示)。

已知:常温下,浸出液中各离子形成氢氧化物沉淀的pH和金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表:
| 金属离子 |  |  |  |  |
| 开始沉淀pH | 8.0 | 1.7 | 5.5 | 3.0 |
| 沉淀完全pH | 9.6 | 3.2 | 8.0 | 4.9 |
| 萃取率(%) | 0 | 99 | 0 | 97~98.5 |
(1)GaN属于
(2)处理浸出液时,将溶液的pH调节至5.4的主要目的是
(3)“溶解还原”步骤中需要加入一定量的铁粉,进行该操作的主要目的是
(4)Ga的化学性质与Al非常相似,“反萃取”后水溶液中镓元素主要以
(5)“高温合成”操作中Ga(CH3)3与NH3反应生成GaN的化学方程式为
(6)利用炼锌矿渣所获得的三种金属盐,分别为镓盐、FeCl2和
您最近半年使用:0次
【推荐3】硫酸渣是黄铁矿制备硫酸过程中得到的焙烧渣,其主要成分为 、
、 、
、 等。工业上可用硫酸渣生产绿矾(
等。工业上可用硫酸渣生产绿矾( ),其工艺流程如下。
),其工艺流程如下。 能溶于NaOH溶液。
能溶于NaOH溶液。
回答下列问题:
(1)硫酸渣在加入NaOH溶液浸取前需进行粉磨处理,目的是___________ 。
(2)操作Ⅰ所需的玻璃仪器有烧杯、___________ 。
(3)浸渣与稀 反应的离子方程式为
反应的离子方程式为___________ 。
(4)物质甲可选择下列物质中的___________。
(5)由溶液Ⅲ获取 时,
时, 易被
易被 氧化,请完成并配平该离子方程式
氧化,请完成并配平该离子方程式_______ 。
□ □
□ □________=□
□________=□ □
□
(6)已知硫酸渣中 (
(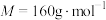 )的质量分数为w,某工厂用m吨该硫酸渣生产出了n吨
)的质量分数为w,某工厂用m吨该硫酸渣生产出了n吨 (
(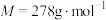 ),产率为
),产率为___________ (列出计算式即可,产率 )。
)。
 、
、 、
、 等。工业上可用硫酸渣生产绿矾(
等。工业上可用硫酸渣生产绿矾( ),其工艺流程如下。
),其工艺流程如下。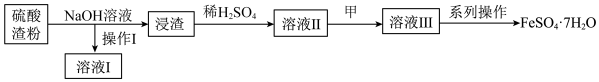
 能溶于NaOH溶液。
能溶于NaOH溶液。回答下列问题:
(1)硫酸渣在加入NaOH溶液浸取前需进行粉磨处理,目的是
(2)操作Ⅰ所需的玻璃仪器有烧杯、
(3)浸渣与稀
 反应的离子方程式为
反应的离子方程式为(4)物质甲可选择下列物质中的___________。
| A.氯气 | B.铁粉 | C.氨水 | D.双氧水 |
(5)由溶液Ⅲ获取
 时,
时, 易被
易被 氧化,请完成并配平该离子方程式
氧化,请完成并配平该离子方程式□
 □
□ □________=□
□________=□ □
□
(6)已知硫酸渣中
 (
(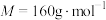 )的质量分数为w,某工厂用m吨该硫酸渣生产出了n吨
)的质量分数为w,某工厂用m吨该硫酸渣生产出了n吨 (
(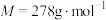 ),产率为
),产率为 )。
)。
您最近半年使用:0次
【推荐1】为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验。
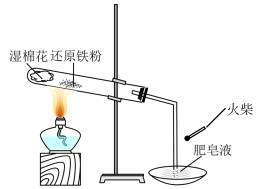
(1)高温下,让铁粉与水蒸气反应,见题图。试管中发生反应的化学方程式是___________ ,其中___________ 为氧化剂。
(2)根据图回答问题

①往A、B溶液中分别滴入几滴KSCN溶液,溶液的颜色A___________ 、B___________ 。
②写出上述过程中有关反应的化学方程式:
Fe2O3→A___________ ;A→B___________ 。
③B→C可看到的现象是___________ 。
④将A的饱和溶液滴入沸水中并不断加热,可制得___________ 胶体;当光束通过该胶体时,可看到一条光亮的“通路”,这种现象称为___________ 效应。

(1)高温下,让铁粉与水蒸气反应,见题图。试管中发生反应的化学方程式是
(2)根据图回答问题

①往A、B溶液中分别滴入几滴KSCN溶液,溶液的颜色A
②写出上述过程中有关反应的化学方程式:
Fe2O3→A
③B→C可看到的现象是
④将A的饱和溶液滴入沸水中并不断加热,可制得
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。
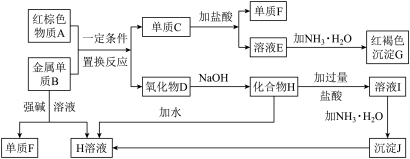
(1)单质F的化学式是_______________ 。
(2)写出单质B与强碱溶液反应的离子方程式___________________________ ,写出由沉淀J生成H溶液的离子方程式______________________________________ 。
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式:____________________________________________ ,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式______________________________ 。
(4)溶液I中所含金属离子是__________________ 。

(1)单质F的化学式是
(2)写出单质B与强碱溶液反应的离子方程式
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式:
(4)溶液I中所含金属离子是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾[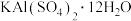 ]有如下两条途径。
]有如下两条途径。
途径I
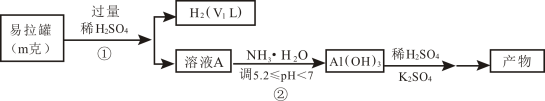
途径II
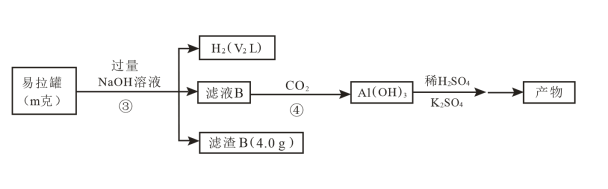
回答下列问题:
(1)Al元素在周期表中的位置为_______ 。
(2)溶液A中的金属离子有_______ 、_______ 、 。
。
(3)过程②生成 的离子方程式为
的离子方程式为_______ 。
(4)过程③发生反应的离子方程式为_______ 。
(5)下列关于产物的说法中,错误的是_______ (填标号)。
A.用KSCN溶液可以检验产物中是否含有
B.向明矾中加入 ,发生反应的离子方程式为
,发生反应的离子方程式为
C.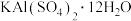 属于混合物
属于混合物
(6)途径II与途径I比较,优点有_______ (写出一点即可)。
(7)若V1与V2之差为2.24L(已折算成标准状况),则m克易拉罐样品中含Fe_______ g。
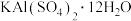 ]有如下两条途径。
]有如下两条途径。途径I

途径II

回答下列问题:
(1)Al元素在周期表中的位置为
(2)溶液A中的金属离子有
 。
。(3)过程②生成
 的离子方程式为
的离子方程式为(4)过程③发生反应的离子方程式为
(5)下列关于产物的说法中,错误的是
A.用KSCN溶液可以检验产物中是否含有

B.向明矾中加入
 ,发生反应的离子方程式为
,发生反应的离子方程式为
C.
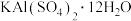 属于混合物
属于混合物(6)途径II与途径I比较,优点有
(7)若V1与V2之差为2.24L(已折算成标准状况),则m克易拉罐样品中含Fe
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】碳酸亚铁可用于治疗缺铁性贫血。实验室里先制得硫酸亚铁,后将硫酸亚铁与碳酸氢钠反应制得碳酸亚铁(FeSO4+2NaHCO3 Na2SO4+FeCO3↓+CO2↑+H2O)。实验装置如下图所示(部分夹持仪器略去)。
Na2SO4+FeCO3↓+CO2↑+H2O)。实验装置如下图所示(部分夹持仪器略去)。
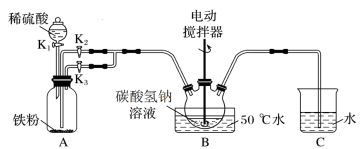
回答下列问题:
(1)A装置中发生反应的化学方程式是________ 。
(2)实验过程中,将生成的FeSO4溶液和NaHCO3溶液混合的操作是________ 。
(3)装置B发生反应生成FeCO3的离子方程式是______ 。
(4)碳酸亚铁在潮湿的空气中逐渐被氧化生成氢氧化铁和一种气体,反应的化学方程式为_________ 。
(5)配制溶液所用的蒸馏水必须先除去溶解的氧气,具体方法是_______ 。
(6)设计实验检验制得的产品中是否含Fe3+:________ 。
 Na2SO4+FeCO3↓+CO2↑+H2O)。实验装置如下图所示(部分夹持仪器略去)。
Na2SO4+FeCO3↓+CO2↑+H2O)。实验装置如下图所示(部分夹持仪器略去)。
回答下列问题:
(1)A装置中发生反应的化学方程式是
(2)实验过程中,将生成的FeSO4溶液和NaHCO3溶液混合的操作是
(3)装置B发生反应生成FeCO3的离子方程式是
(4)碳酸亚铁在潮湿的空气中逐渐被氧化生成氢氧化铁和一种气体,反应的化学方程式为
(5)配制溶液所用的蒸馏水必须先除去溶解的氧气,具体方法是
(6)设计实验检验制得的产品中是否含Fe3+:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】该课外活动小组为了粗略测定过氧化钠的纯度,他们称取ag样品,并设计用下图装置来测定过氧化钠的质量分数。
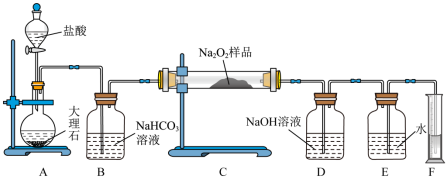
(1)将仪器连接好以后,必须进行的第一步操作是___________ 。
(2)B装置出来的气体是否需要干燥___________ 。(填“是”或“否”)
(3)写出装置C中发生的所有反应的化学方程式___________ ,___________ 。
(4)实验结束时,读取实验中生成气体的体积时,合理的是___________ (填字母序号)。
a.直接读取气体体积,不需要冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中的水的体积
(5)读取量筒内水的体积后,折算成标准状况下氧气的体积为VmL,则样品中过氧化钠的质量分数为___________ 。

(1)将仪器连接好以后,必须进行的第一步操作是
(2)B装置出来的气体是否需要干燥
(3)写出装置C中发生的所有反应的化学方程式
(4)实验结束时,读取实验中生成气体的体积时,合理的是
a.直接读取气体体积,不需要冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中的水的体积
(5)读取量筒内水的体积后,折算成标准状况下氧气的体积为VmL,则样品中过氧化钠的质量分数为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氮化铝(AlN)是一种新型无机非金属材料。为了分析某AlN样品(样品中的杂质不与氢氧化钠溶液反应)中 AlN的含量,某实验小组设计了如下两种实验方案。
已知:AlN+NaOH+H2O=NaAlO2+NH3↑
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。
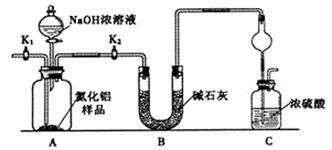
(1)上图C装置中球形干燥管的作用是_______________________ 。
(2)完成以下实验步骤:组装好实验装置,首先______________ ,再加入实验药品。接下来的实验操作是_______ ,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是______________ 。
(3)若去掉装置B,则导致测定结果________ (填“偏高”、“偏低”或“无影响”)。由于上述装置还存在缺陷,导致测定结果偏高,请提出改进意见________________ 。
【方案2】按以下步骤测定样品中A1N的纯度:
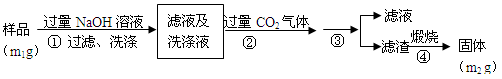
(4)步骤②生成沉淀的离子方程式为___________________ 。
(5)步骤③的操作是_________ 。A1N的纯度是__________ (用m1、m2表示)。
已知:AlN+NaOH+H2O=NaAlO2+NH3↑
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。

(1)上图C装置中球形干燥管的作用是
(2)完成以下实验步骤:组装好实验装置,首先
(3)若去掉装置B,则导致测定结果
【方案2】按以下步骤测定样品中A1N的纯度:

(4)步骤②生成沉淀的离子方程式为
(5)步骤③的操作是
您最近半年使用:0次



