某小组探究酸化条件对0.1mol/LKI溶液氧化反应的影响。
(1)溶液变蓝,说明溶液中含有____________ 。结合实验1和实验2,该小组同学认为酸化能够加快I-氧化反应的速率。
(2)同学甲对滴加稀硫酸后溶液变蓝速率不同的原因提出猜想:放置一段时间后的0.1mol/LKI溶液成分与新制0.1mol/LKI溶液可能存在差异,并继续进行探究。
实验3:取新制0.1mol/LKI溶液在空气中放置,测得pH如下:
资料:
ⅰ.pH<11.7时,I-能被O2氧化为I。
ⅱ.一定碱性条件下,I2容易发生歧化,产物中氧化产物与还原产物的物质的量之比为1∶5。
①用化学用语,解释0.1mol/LKI溶液放置初期pH升高的原因:_________________________________________________________ 。
②对比实验1和实验2,结合化学用语和必要的文字,分析实验1中加稀硫酸后“溶液立即变蓝”的主要原因可能是_____________________________________________________________________________________ 。
(3)同学甲进一步设计实验验证分析的合理性。
(4)该组同学想进一步探究pH对I2发生歧化反应的影响,进行了如下实验。
实验5:用20mL 4种不同浓度的KOH溶液与2mL淀粉溶液进行混合,测量混合液的pH后,向其中加入2滴饱和碘水,观察现象。记录如下:
从实验5可以看出pH越大,歧化反应速率越_______________ (填“快”或“慢”)。
解释pH=8.4时,“产生蓝色,30s后蓝色消失”的原因:_________________________ 。
| 序号 | 操作及现象 |
| 实验1 | 取放置一段时间后依然无色的0.1mol/LKI溶液,加入淀粉溶液,溶液不变蓝;向溶液中继续加入2滴6mol/L的稀硫酸,溶液立即变蓝 |
| 实验2 | 取新制的0.1mol/LKI溶液,加入淀粉溶液,溶液不变蓝;向溶液中继续加入2滴6mol/L的稀硫酸,溶液10s后微弱变蓝 |
(1)溶液变蓝,说明溶液中含有
(2)同学甲对滴加稀硫酸后溶液变蓝速率不同的原因提出猜想:放置一段时间后的0.1mol/LKI溶液成分与新制0.1mol/LKI溶液可能存在差异,并继续进行探究。
实验3:取新制0.1mol/LKI溶液在空气中放置,测得pH如下:
| 时间 | 5分钟 | 1天 | 3天 | 10天 |
| pH | 7.2 | 7.4 | 7.8 | 8.7 |
资料:
ⅰ.pH<11.7时,I-能被O2氧化为I。
ⅱ.一定碱性条件下,I2容易发生歧化,产物中氧化产物与还原产物的物质的量之比为1∶5。
①用化学用语,解释0.1mol/LKI溶液放置初期pH升高的原因:
②对比实验1和实验2,结合化学用语和必要的文字,分析实验1中加稀硫酸后“溶液立即变蓝”的主要原因可能是
(3)同学甲进一步设计实验验证分析的合理性。
| 序号 | 操作 | 现象 |
| 实验4 | 重复实验2操作后,继续向溶液中加入 | 溶液立即变蓝 |
(4)该组同学想进一步探究pH对I2发生歧化反应的影响,进行了如下实验。
实验5:用20mL 4种不同浓度的KOH溶液与2mL淀粉溶液进行混合,测量混合液的pH后,向其中加入2滴饱和碘水,观察现象。记录如下:
| 实验组 | A | B | C | D |
| pH | 11.4 | 10.6 | 9.5 | 8.4 |
| 现象 | 无颜色变化 | 产生蓝色后瞬间消失 | 产生蓝色,30s后蓝色消失 | |
从实验5可以看出pH越大,歧化反应速率越
解释pH=8.4时,“产生蓝色,30s后蓝色消失”的原因:
2020·北京丰台·一模 查看更多[4]
北京市丰台区2020届高三第一次模拟考试化学试题(已下线)北京市2019-2020学年高三各区一模化学考试分类汇编:科学探究北京市北京交通大学附属中学2020-2021学年高二上学期期末练习化学试题天津市河北区2021-2022学年高三上学期期末考试化学试题
更新时间:2020-05-11 19:31:38
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】海水中溴含量约为65mg·L-1,从海水中提取溴的工艺流程如下:
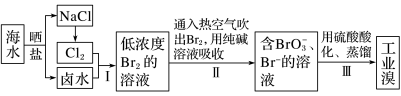
(1)以上步骤I中已获得游离态的溴,步骤II又将之转变成化合态的溴,其目的是_______ 。
(2)步骤II通入热空气吹出Br2,利用了溴的_______。
(3)步骤II中涉及的离子反应如下,请在下面横线上填入适当的化学计量数:_______ 。
_______Br2+_______ =_______
=_______ +_______Br-+_______CO2↑
+_______Br-+_______CO2↑
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的化学方程式:_______ 。
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是_______。
(6)某同学在进行蒸馏操作时,采用如图所示装置:
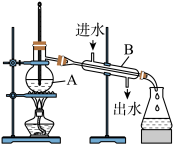
①写出图中两处明显的错误:_______ 、_______ 。
②实验时A中除加入混合溶液外还需加入少量_______ ,其作用是_______ 。

(1)以上步骤I中已获得游离态的溴,步骤II又将之转变成化合态的溴,其目的是
(2)步骤II通入热空气吹出Br2,利用了溴的_______。
| A.氧化性 | B.还原性 | C.挥发性 | D.腐蚀性 |
_______Br2+_______
 =_______
=_______ +_______Br-+_______CO2↑
+_______Br-+_______CO2↑(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的化学方程式:
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是_______。
| A.乙醇 | B.四氯化碳 | C.烧碱溶液 | D.苯 |

①写出图中两处明显的错误:
②实验时A中除加入混合溶液外还需加入少量
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】我国有广阔的海岸线,海水综合利用大有可为.海水中Br﹣含量为65mg•L﹣1,从海水中提取溴的工业流程如下:

(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是:_______ .
(2)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的___(填序号).
(3)以上流程Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数:
___ Br2+___  ═
═___  +
+___ Br﹣+___ CO2↑
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.写出溴蒸气与二氧化硫水溶液反应的离子方程式:___________ .
(5)实验室从溴水中分离出溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是____(填序号).
(6)用上述流程制得含Br265%的工业溴1t,至少需要海水_____ m3.
(7)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.写出溴与二氧化硫水溶液反应的离子方程式:__________________ .

(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是:
(2)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的___(填序号).
| A.氧化性 | B.还原性 | C.挥发性 | D.腐蚀性 |
 ═
═ +
+(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.写出溴蒸气与二氧化硫水溶液反应的离子方程式:
(5)实验室从溴水中分离出溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是____(填序号).
| A.乙醇 | B.四氯化碳 | C.裂化汽油 | D.苯 |
(7)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.写出溴与二氧化硫水溶液反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】锑(Sb)及其化合物在工业上有许多用途。以辉锑矿(主要成分为 ,还含有PbS、
,还含有PbS、 、CuO、
、CuO、 等)为原料制备金属锑的工艺流程如图所示:
等)为原料制备金属锑的工艺流程如图所示: 之外,还含有
之外,还含有 、
、 、
、 、
、 等;
等;
②常温下: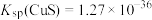 ,
,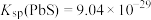 ;
;
③溶液中离子浓度小于或等于 mol/L时,认为该离子沉淀完全。
mol/L时,认为该离子沉淀完全。
(1)滤渣1中除了S之外,还有_______ (填化学式)。
(2)“浸出”时, 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(3)该生产流程能实现循环利用的物质是_______ (填化学式)。
(4)常温下,“除铜、铅”时, 和
和 均沉淀完全,此时溶液中的
均沉淀完全,此时溶液中的 不低于
不低于_______ 。所加 也不宜过多,其原因为
也不宜过多,其原因为_______ 。
(5)“除砷”时有 生成,该反应的离子方程式为
生成,该反应的离子方程式为_______ 。
 ,还含有PbS、
,还含有PbS、 、CuO、
、CuO、 等)为原料制备金属锑的工艺流程如图所示:
等)为原料制备金属锑的工艺流程如图所示:
 之外,还含有
之外,还含有 、
、 、
、 、
、 等;
等;②常温下:
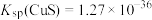 ,
,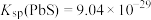 ;
;③溶液中离子浓度小于或等于
 mol/L时,认为该离子沉淀完全。
mol/L时,认为该离子沉淀完全。(1)滤渣1中除了S之外,还有
(2)“浸出”时,
 发生反应的化学方程式为
发生反应的化学方程式为(3)该生产流程能实现循环利用的物质是
(4)常温下,“除铜、铅”时,
 和
和 均沉淀完全,此时溶液中的
均沉淀完全,此时溶液中的 不低于
不低于 也不宜过多,其原因为
也不宜过多,其原因为(5)“除砷”时有
 生成,该反应的离子方程式为
生成,该反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学课外小组用如图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)。
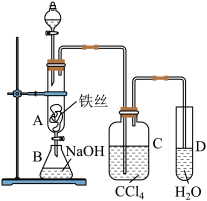
(1)写出A中反应的化学方程式_____ 。
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是____ 。
(3)C中盛放CCl4的作用是___ 。
(4)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入___ ,现象是__ 。

(1)写出A中反应的化学方程式
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是
(3)C中盛放CCl4的作用是
(4)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】“消洗灵”是一种广谱、高效、低毒的消毒洗涤剂,消毒原理与“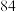 消毒液”相似,但更稳定、易保存。某“消洗灵”产品化学组成可以表示为Na10P3O13Cl·5H2O,实验室制备装置和过程如下:
消毒液”相似,但更稳定、易保存。某“消洗灵”产品化学组成可以表示为Na10P3O13Cl·5H2O,实验室制备装置和过程如下:
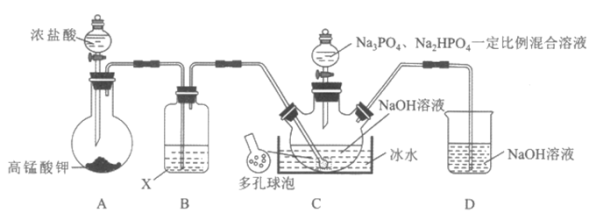
回答下列问题:
Ⅰ.打开 中分液漏斗活塞,制备
中分液漏斗活塞,制备 碱性溶液。
碱性溶液。
(1)C中盛装氢氧化钠的仪器名称是___________ 。
(2) 试剂的名称为
试剂的名称为___________ 。
(3)C中采用多孔球泡的目的是___________ 。
(4)D装置的作用是___________ 。
Ⅱ.关闭 中分液漏斗活塞,打开
中分液漏斗活塞,打开 中分液漏斗活塞,一段时间后
中分液漏斗活塞,一段时间后 中溶液经蒸发浓缩、冷却结晶、过滤得到粗产品。
中溶液经蒸发浓缩、冷却结晶、过滤得到粗产品。
(5)产品中氯元素的化合价为___________ 。
Ⅲ.产品纯度测定Na10P3O13Cl·5H2O的摩尔质量为 )
)
①取 待测试样溶于蒸馏水配成
待测试样溶于蒸馏水配成 溶液;
溶液;
②取 待测液于锥形瓶中,加入
待测液于锥形瓶中,加入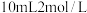 稀硫酸、
稀硫酸、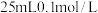 碘化钾溶液(过量),此时溶液出现棕色;
碘化钾溶液(过量),此时溶液出现棕色;
③滴入 滴
滴 淀粉溶液,用
淀粉溶液,用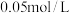 硫代硫酸钠溶液滴定至终点,平行滴定三次,平均消耗
硫代硫酸钠溶液滴定至终点,平行滴定三次,平均消耗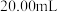 。
。
已知: 2S2O +I2=S4O
+I2=S4O + 2I-
+ 2I-
(6)产品的纯度为___________ (用含 、
、 的代数式表示)。
的代数式表示)。
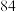 消毒液”相似,但更稳定、易保存。某“消洗灵”产品化学组成可以表示为Na10P3O13Cl·5H2O,实验室制备装置和过程如下:
消毒液”相似,但更稳定、易保存。某“消洗灵”产品化学组成可以表示为Na10P3O13Cl·5H2O,实验室制备装置和过程如下:
回答下列问题:
Ⅰ.打开
 中分液漏斗活塞,制备
中分液漏斗活塞,制备 碱性溶液。
碱性溶液。(1)C中盛装氢氧化钠的仪器名称是
(2)
 试剂的名称为
试剂的名称为(3)C中采用多孔球泡的目的是
(4)D装置的作用是
Ⅱ.关闭
 中分液漏斗活塞,打开
中分液漏斗活塞,打开 中分液漏斗活塞,一段时间后
中分液漏斗活塞,一段时间后 中溶液经蒸发浓缩、冷却结晶、过滤得到粗产品。
中溶液经蒸发浓缩、冷却结晶、过滤得到粗产品。(5)产品中氯元素的化合价为
Ⅲ.产品纯度测定Na10P3O13Cl·5H2O的摩尔质量为
 )
)①取
 待测试样溶于蒸馏水配成
待测试样溶于蒸馏水配成 溶液;
溶液;②取
 待测液于锥形瓶中,加入
待测液于锥形瓶中,加入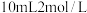 稀硫酸、
稀硫酸、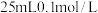 碘化钾溶液(过量),此时溶液出现棕色;
碘化钾溶液(过量),此时溶液出现棕色;③滴入
 滴
滴 淀粉溶液,用
淀粉溶液,用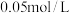 硫代硫酸钠溶液滴定至终点,平行滴定三次,平均消耗
硫代硫酸钠溶液滴定至终点,平行滴定三次,平均消耗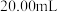 。
。已知: 2S2O
 +I2=S4O
+I2=S4O + 2I-
+ 2I-(6)产品的纯度为
 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需经处理后才能排放。某校兴趣小组欲测定硫酸工业尾气中二氧化硫含量,采用以下方案:
甲方案:如下图所示,图中气体流量计B用于准确测量通过尾气的体积。将尾气通入一定体积已知浓度的碘水中测定二氧化硫的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。
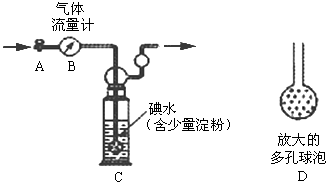
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验准确度,其理由是:______ 。
(2)洗气瓶C中的溶液可以用其他试剂替代,请你举出一种:______ 。
(3)洗气瓶C溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量______ (填“偏高”、“偏低”或“无影响”)。
乙方案:实验步骤如以下流程图所示:
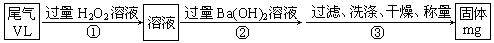
(4)写出步骤②中反应的化学方程式______ 。
(5)步骤③中洗涤沉淀的方法是______ 。
(6)通过的尾气体积为VL(已换算成标准状况)时,该尾气中二氧化硫含量(体积分数)为______ (用含有V、m的代数式表示)。
丙方案:将乙方案中步骤①省略,直接将尾气通入过量Ba(OH)2溶液,其余步骤与方案乙相同。
(7)你认为丙方案是否合理,说明理由:______ 。
甲方案:如下图所示,图中气体流量计B用于准确测量通过尾气的体积。将尾气通入一定体积已知浓度的碘水中测定二氧化硫的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。

(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验准确度,其理由是:
(2)洗气瓶C中的溶液可以用其他试剂替代,请你举出一种:
(3)洗气瓶C溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量
乙方案:实验步骤如以下流程图所示:
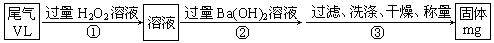
(4)写出步骤②中反应的化学方程式
(5)步骤③中洗涤沉淀的方法是
(6)通过的尾气体积为VL(已换算成标准状况)时,该尾气中二氧化硫含量(体积分数)为
丙方案:将乙方案中步骤①省略,直接将尾气通入过量Ba(OH)2溶液,其余步骤与方案乙相同。
(7)你认为丙方案是否合理,说明理由:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某学习小组查阅资料可知高温下, 与
与 反应一定生成
反应一定生成 ,可能生成
,可能生成 或
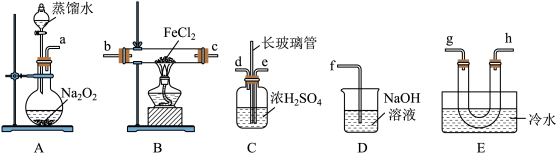
或 。该小组同学利用如下装置对该反应进行探究。回答下列问题:
。该小组同学利用如下装置对该反应进行探究。回答下列问题:
已知: 固体呈绿色,熔点为
固体呈绿色,熔点为 ,沸点为
,沸点为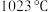 ;
; 在
在 左右升华。
左右升华。
(1)装置A中盛放蒸馏水的仪器名称为_______ 。
(2)按气流从左到右的顺序,上述装置合理的连接顺序为_______ (填仪器接口的小写字母)。
 与
与 反应一定生成
反应一定生成 ,可能生成
,可能生成 或
或 。该小组同学利用如下装置对该反应进行探究。回答下列问题:
。该小组同学利用如下装置对该反应进行探究。回答下列问题:
已知:
 固体呈绿色,熔点为
固体呈绿色,熔点为 ,沸点为
,沸点为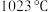 ;
; 在
在 左右升华。
左右升华。(1)装置A中盛放蒸馏水的仪器名称为
(2)按气流从左到右的顺序,上述装置合理的连接顺序为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组设计如下实验方案,将浓硫酸与铜片反应制备SO2并进行相关实验探究,实验装置如图所示:
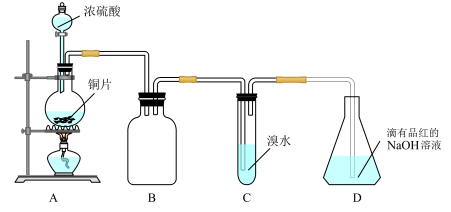
请回答下列问题:
(1)装置B的作用是______ 。
(2)设计装置C的目的是验证SO2的______ 性,装置C中发生反应的离子方程式是______ 装置D中NaOH全部转化为NaHSO3的标志是______ 。
(3)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能的情况:
I.HSO3-与ClO-恰好反应
Ⅱ.NaClO不足
Ⅲ.NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请完成下表:(已知酸性:H2SO3>H2CO3>HClO)
(4)请设计简单实验证明:室温下HSO3-的电离平衡常数Ka与水解平衡常数Kb,的相对大小:___ 。

请回答下列问题:
(1)装置B的作用是
(2)设计装置C的目的是验证SO2的
(3)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能的情况:
I.HSO3-与ClO-恰好反应
Ⅱ.NaClO不足
Ⅲ.NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请完成下表:(已知酸性:H2SO3>H2CO3>HClO)
| 序号 | 实验操作 | 现象 | 结论 |
| ① | 加几小块CaCO3固体 | 有气泡产生 | I或Ⅱ |
| ② | 滴加少量淀粉KI溶液,振荡 | Ⅲ | |
| ③ | 滴加少量溴水,振荡 | Ⅱ | |
| ④ | 滴加少量酸性KMnO4溶液、振荡 | 溶液为紫色 |
您最近一年使用:0次




