原子序数依次增大的短周期主族元素X、Y、Z、W、R,其中X、Y两种元素的核电荷数之差等于它们的原子最外层电子数之和;Y、Z位于相邻主族;Z是地壳中含量最高的元素。X、W是同主族元素。上述五种元素两两间能形成四种常见的化合物甲、乙、丙、丁,这四种化合物中原子个数比如下表:
(1)写出下列元素符号:Y:___ ;W:___ ;R:___ 。
(2)写出下列化合物的电子式:乙:___ ;丙:___ 。
(3)向甲的水溶液中加入丁,有淡黄色沉淀生成,请写出反应的化学方程式为:___ 。
(4)甲和乙反应能放出大量的热,同时生成两种无污染的物质, 请写出该反应的化学方程式::___ 。
| 甲 | 乙 | 丙 | 丁 | |
| 化合物中元素原子个数比 | X∶Z=1∶1 | Y∶X=1∶2 | W∶Z=1∶1 | W∶R=2∶1 |
(1)写出下列元素符号:Y:
(2)写出下列化合物的电子式:乙:
(3)向甲的水溶液中加入丁,有淡黄色沉淀生成,请写出反应的化学方程式为:
(4)甲和乙反应能放出大量的热,同时生成两种无污染的物质, 请写出该反应的化学方程式::
更新时间:2020-05-12 09:45:25
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】氢能源是一种重要的清洁能源。现有两种可产生H2的固体化合物甲和乙。将6.00 g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72 LH2(已折算成标准状况)。甲与水反应也能产生H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状态下的密度为1.25 g·L-1。请回答下列问题:
(1)乙的电子式是_______ 。
(2)甲可在加热时将二氧化碳还原为甲烷,其化学方程式是_______ 。
(3)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式_______ 。
(4)甲与乙之间能发生反应产生H2,判断理由是_______ 。
(1)乙的电子式是
(2)甲可在加热时将二氧化碳还原为甲烷,其化学方程式是
(3)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式
(4)甲与乙之间能发生反应产生H2,判断理由是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,表中所列序号分别代表短周期中的一种元素:
(1)元素④的原子结构示意图是_______ 。
(2)元素⑤在周期表中的位置是_______ 。
(3)②⑥⑦最高价氧化物对应水化物中的碱性最强的是(用电子式表示)_______ 。
(4)⑤⑧⑨的氢化物中稳定性最好的是(用电子式表示)_______ 。
(5)⑧⑩的最高价氧化物对应水化物的酸性顺序(用化学式表示)_______ 。
(6)化合物X由①⑤⑥三种元素组成,化合物Y是元素③的最高价氧化物,将标准状况下11.2LY通入到200mL3mol/L的X溶液中完全被吸收。通过计算判断所得溶液组成的化学式及质量(不用写出计算过程):_______ 。
| ① | |||||||
| ② | ③ | ④ | ⑤ | ||||
| ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)元素⑤在周期表中的位置是
(3)②⑥⑦最高价氧化物对应水化物中的碱性最强的是(用电子式表示)
(4)⑤⑧⑨的氢化物中稳定性最好的是(用电子式表示)
(5)⑧⑩的最高价氧化物对应水化物的酸性顺序(用化学式表示)
(6)化合物X由①⑤⑥三种元素组成,化合物Y是元素③的最高价氧化物,将标准状况下11.2LY通入到200mL3mol/L的X溶液中完全被吸收。通过计算判断所得溶液组成的化学式及质量(不用写出计算过程):
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知A、B、C、D、E、F 均为短周期主族元素,原子序数依次增大。C为地壳中含量最高的元素,E原子的次外层电子数是最外层的2倍,F最高价氧化物对应的水化物酸性比H2SO4强。A、D同主族,B、C同周期,气态化合物甲由A、B两种元素组成,其原子个数比为4∶1。
(1)化合物甲的空间结构_______ 。
(2)F在周期表中的位置_______ 。
(3)B、D、E 3种元素原子半径由大到小顺序_______ (用元素符号表示)。
(4)用电子式表示D和F形成化合物的过程_______ 。
(5)B的最高价氧化物和D的一种氧化物能发生反应生成C单质,写出该反应的化学方程式_______ 。
(1)化合物甲的空间结构
(2)F在周期表中的位置
(3)B、D、E 3种元素原子半径由大到小顺序
(4)用电子式表示D和F形成化合物的过程
(5)B的最高价氧化物和D的一种氧化物能发生反应生成C单质,写出该反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】利用化学原理可以对工厂排放的废水、废渣等进行有效检测。某工厂对制铬工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸液中金属离子主要是Cr3+,其次是Fe3+, Fe2+, Al3+, Ca2+, Mg2+)

常温下部分阳离子的氢氧化物形成沉淀时溶液的pH见下表:
(1)酸浸时,为了提高浸取率可采取的措施是_____________________________ (至少一条)
(2)调pH=4.0是为了除去______________________ (填Fe3+, Al3+, Ca2+, Mg2+)
(3)钠离子交换树脂的原理为Mn++ n NaR → MRn+nNa+,被交换的杂质离子是___________________________ (填Fe3+, Al3+, Ca2+, Mg2+)
(4)试配平下列氧化还原反应方程式:
____ Na2Cr2O7+__ SO2+____ H2O =____ Cr(OH)(H2O)5SO4+___ Na2SO4

常温下部分阳离子的氢氧化物形成沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Ca2+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | 9.6 | 4.2 | 9.7 | — |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8.0 | 11.7 | 9.0(>9.0溶解) |
(1)酸浸时,为了提高浸取率可采取的措施是
(2)调pH=4.0是为了除去
(3)钠离子交换树脂的原理为Mn++ n NaR → MRn+nNa+,被交换的杂质离子是
(4)试配平下列氧化还原反应方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】肼(N2H4)可作火箭发射的燃料,具有强还原性,实验室用NH3与Cl2合成N2H4的装置如图所示,请回答下列问题:

(1)仪器c的名称为__________ ,按图连接装置,盛放试剂前,首先要进行________ 的操作。
(2)装置A试管中盛放的药品为_______ (填化学式),装置中仪器a的作用除了导气还有_______ 。
(3)导管b的作用是______________ 。装置C中的试剂是_________ (填名称)。
(4)装置D中制备 的化学方程式为
的化学方程式为________________________ 。
(5)装置B中制备 的离子方程式为
的离子方程式为________________________________ 。
(6)实验室对产品中肼的质量分数进行测定。已知: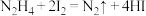 。取装置B中的溶液
。取装置B中的溶液 ,调节溶液
,调节溶液 为6.5左右,加水配成
为6.5左右,加水配成 溶液,取
溶液,取 于锥形瓶中,滴加
于锥形瓶中,滴加 滴淀粉溶液,用
滴淀粉溶液,用 的
的 溶液滴定(杂质不参与反应),测得消耗
溶液滴定(杂质不参与反应),测得消耗 溶液的体积为
溶液的体积为 ,则该产品中
,则该产品中 的质量分数为
的质量分数为_____ 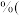 保留3位有效数字),若加水配制溶液时,俯视容量瓶刻度线,则测定的质量分数
保留3位有效数字),若加水配制溶液时,俯视容量瓶刻度线,则测定的质量分数______ (填“偏大”“偏小”“不影响”)。

(1)仪器c的名称为
(2)装置A试管中盛放的药品为
(3)导管b的作用是
(4)装置D中制备
 的化学方程式为
的化学方程式为(5)装置B中制备
 的离子方程式为
的离子方程式为(6)实验室对产品中肼的质量分数进行测定。已知:
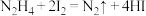 。取装置B中的溶液
。取装置B中的溶液 ,调节溶液
,调节溶液 为6.5左右,加水配成
为6.5左右,加水配成 溶液,取
溶液,取 于锥形瓶中,滴加
于锥形瓶中,滴加 滴淀粉溶液,用
滴淀粉溶液,用 的
的 溶液滴定(杂质不参与反应),测得消耗
溶液滴定(杂质不参与反应),测得消耗 溶液的体积为
溶液的体积为 ,则该产品中
,则该产品中 的质量分数为
的质量分数为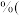 保留3位有效数字),若加水配制溶液时,俯视容量瓶刻度线,则测定的质量分数
保留3位有效数字),若加水配制溶液时,俯视容量瓶刻度线,则测定的质量分数
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】从分银渣(主要成分SnO2、Sb2O3、Ag、PbCl2)中提取金属的工艺流程如下:

已知:①“浆化熔炼”时,SnO2、Sb2O3转化为可溶性Na2SnS3和Na3SbS3、PbCl2转化为更难溶的PbS;②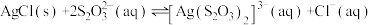 ;③滤液3中含大量[PbCl4]2-。
;③滤液3中含大量[PbCl4]2-。
回答下列问题:
(1)“溶浸”时为提高浸取速率,可以采取的方法有___________ (写出一种即可)。
(2)“沉锡”时调节pH过低,除导致沉淀不完全,还可能产生的问题有___________ ;证明“沉锡”后所得粗Sn(OH)4洗涤干净的具体操作为___________ 。
(3)“氧化分银”时,含Pb微粒转化的离子方程式为___________ ;向滤渣1中加入饱和NaCl的目的是___________ 。
(4)碱性环境下,加入足量甲醛得到粗Ag的离子方程式为___________ 。
(5)废液2经除杂、双氧水氧化处理后所得物质可循环入上述___________ 操作(填操作单元名称)。

已知:①“浆化熔炼”时,SnO2、Sb2O3转化为可溶性Na2SnS3和Na3SbS3、PbCl2转化为更难溶的PbS;②
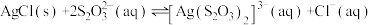 ;③滤液3中含大量[PbCl4]2-。
;③滤液3中含大量[PbCl4]2-。回答下列问题:
(1)“溶浸”时为提高浸取速率,可以采取的方法有
(2)“沉锡”时调节pH过低,除导致沉淀不完全,还可能产生的问题有
(3)“氧化分银”时,含Pb微粒转化的离子方程式为
(4)碱性环境下,加入足量甲醛得到粗Ag的离子方程式为
(5)废液2经除杂、双氧水氧化处理后所得物质可循环入上述
您最近一年使用:0次
【推荐1】A、B、C、D均为周期表中前四周期元素,其原子序数依次增大,其中A、B、C为短周期非金属 元素。A是形成化合物种类最多的元素;B原子基态电子排布中只有一个未成对电子;C是同周期元素中原子半径最小的元素;D的基态原子在前四周期元素的基态原子中单电子数最多;回答下列问题(相关回答均用元素符号表示):
(1)D的基态原子的核外电子排布式是_____ 。
(2)B的氢化物的沸点比C的氢化物的沸点___________ (填“高”或“低”),原因是______ 。
(3)A的电负性______ (填“大于”或“小于”)C的电负性,A与C形成的化合物的电子式_________ 。
(1)D的基态原子的核外电子排布式是
(2)B的氢化物的沸点比C的氢化物的沸点
(3)A的电负性
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知五种元素为短周期元素,其原子序数的大小顺序为C>A>B>D>E;A、C同周期,B、C同主族;A与B形成离子化合物,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子分子。试回答下列问题:
(1)写出五种元素名称A________ ,B________ ,C________ ,D________ ,E________ ;
(2)用电子式表示A2C的形成过程________________________________ ;
(3)D与E形成常见离子的空间构型为________________ ;
(4)A、B两元素形成的化合物A2B2属于__________ 晶体(填类型),晶体内存在的化学键有___________ ;A2B晶体的熔点_______ (填“>”“=”“<”)A2C晶体的熔点;
(5)由A、B、C、E四种元素,可以共同形成两种不同化合物,它们的水溶液可以反应生成一种气体,请写出离子方程式:___________________________________ 。
(1)写出五种元素名称A
(2)用电子式表示A2C的形成过程
(3)D与E形成常见离子的空间构型为
(4)A、B两元素形成的化合物A2B2属于
(5)由A、B、C、E四种元素,可以共同形成两种不同化合物,它们的水溶液可以反应生成一种气体,请写出离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有A、B、C、D、E五种元素,它们的质子数依次增多。
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+离子比B3+离子多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于D的下一个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为2:1。试回答:
(1)A元素在周期表中的位置为________ 、E是________ (填元素名称)。
(2)D的单质分子的结构式_______ ,C元素最高价氧化物的水化物的电子式____ 。
(3)写出工业上冶炼B单质的化学方程式_______________ 。
(4)写出CD的溶液中通入氯气的离子方程式________________ 。
(5)比较B、C、E三种元素形成的简单离子氧化性的强弱:(B、C、E离子用实际离子符号表示)氧化性_________ 。
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+离子比B3+离子多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于D的下一个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质的量之比为2:1。试回答:
(1)A元素在周期表中的位置为
(2)D的单质分子的结构式
(3)写出工业上冶炼B单质的化学方程式
(4)写出CD的溶液中通入氯气的离子方程式
(5)比较B、C、E三种元素形成的简单离子氧化性的强弱:(B、C、E离子用实际离子符号表示)氧化性
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】联合国大会称2019年定为“化学元素周期表国际年”,表明了元素周期律的重要性。几种主族元素在周期表中的位置如下:
根据上表回答下列问题:
(1)①⑤⑥三种元素原子半径由大到小的顺序是___________ (用元素符号表示)。
(2)表中某元素原子的电子层数是最外层电子数的3倍,该元素的原子结构示意图为___________ ,该元素在周期表中的位置是___________ ,写出该元素的单质与④的简单氧化物反应的化学方程式___________ 。
(3)①②③三种元素最高价氧化物对应的水化物的碱性最强的是___________ 。(填化学式)。
(4)⑦的非金属性强于⑧,下列表述中不能证明这一事实的是___________(填字母)。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ④ | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ⑦ | |||||
| 4 | ② | ⑧ | ||||||
(1)①⑤⑥三种元素原子半径由大到小的顺序是
(2)表中某元素原子的电子层数是最外层电子数的3倍,该元素的原子结构示意图为
(3)①②③三种元素最高价氧化物对应的水化物的碱性最强的是
(4)⑦的非金属性强于⑧,下列表述中不能证明这一事实的是___________(填字母)。
| A.⑦的氢化物比⑧的氢化物稳定 |
| B.⑦最高价氧化物对应的水化物的酸性强于⑧最高价氧化物对应的水化物的酸性 |
| C.⑦的单质能将⑧从其钠盐溶液中置换出来 |
| D.⑦的氢化物酸性比⑧的氢化物酸性 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知有原子序数依次增大的A、B、C、D、E五种短周期元素和过渡元素F,其相关信息如表所示:
(1)上述六种元素中,金属性最强的元素在周期表中的位置是_______ 。
(2)分子式为B5Al2且其一氯代物只有一种的有机物的名称为_______ 。
(3)C元素的气态氢化物与其最高价氧化物对应的水化物化合生成M,M的水溶液呈_______ 性;将M的浓溶液滴加到Mg(OH)2悬浊液中,描述现象并解释产生该现象的原因_______ 。
(4)D元素的最高价氧化物对应的水化物与E元素的单质反应的离子方程式为_______ 。
(5)F与B形成的合金在潮湿的空气中易发生电化学腐蚀形成红棕色固体,腐蚀过程中正极的电极反应式为_______ 。
1 | A与C形成化合物的水溶液呈碱性 |
2 | B的最高正价与最低负价的代数和为0 |
3 | D的常见化合物的焰色反应为黄色 |
4 | E是同周期中简单离子半径最小的元素 |
(2)分子式为B5Al2且其一氯代物只有一种的有机物的名称为
(3)C元素的气态氢化物与其最高价氧化物对应的水化物化合生成M,M的水溶液呈
(4)D元素的最高价氧化物对应的水化物与E元素的单质反应的离子方程式为
(5)F与B形成的合金在潮湿的空气中易发生电化学腐蚀形成红棕色固体,腐蚀过程中正极的电极反应式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】有A、B、C、D四种短周期元素, 它们的原子序数由A到D依次增大, 已知A和B原子有相同的电子层数, 且A的L层电子数是K层电子数的两倍, C在空气中燃烧时呈现黄色火焰, C的单质在加热下与B的单质充分反应, 可以得到与D单质颜色相同的淡黄色固态化合物, 试根据以上叙述回答:
(1)元素名称: A______ B _____ C _____ D ______
(2)D元素位于周期表中_____________________ 族,AB2的结构式为______________
(3)写出AB2与C2B2反应的化学方程式:________________________________________ 。
(4)电子式表示化合物 C2D 的形成过程:_____________________________________ 。
(1)元素名称: A
(2)D元素位于周期表中
(3)写出AB2与C2B2反应的化学方程式:
(4)电子式表示化合物 C2D 的形成过程:
您最近一年使用:0次



