几种短周期元素的原子半径及主要化合价见下表:
根据表中信息,判断以下说法正确的是( )
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.160 | 0.186 | 0.102 | 0.143 | 0.074 |
| 主要化合价 | +2 | +1 | -2,+4,+6 | +3 | -2 |
| A.单质与稀硫酸反应的速率快慢:R>X>Y |
| B.离子半径:T2->X2+ |
| C.元素最高价氧化物的水化物的碱性:Y>R>X |
| D.单质与氢气化合由易到难:Z>T |
更新时间:2020-05-18 16:50:48
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】我国科学家最近发现一种可用于制造半导体材料的新物质,其结构如图所示,X、Y、Z、W为原子序数依次增大的短周期主族元素,Z、Y处于同一主族。下列说法正确的是
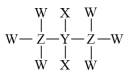
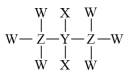
A.原子半径: |
B.电负性: |
| C.W、Z形成的化合物各原子最外层满足8电子稳定结构 |
| D.W的氧化物对应的水化物为强电解质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为3:8,X与W同族,Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是
| A.金属性:Y>Z | B.氢化物的沸点:X<W |
| C.离子的还原性:X>W | D.离子半径:X>Z>Y |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验过程中的现象及结论均正确,且存在因果关系的是
| A | B | C | D | |
| 实验装置 |  | 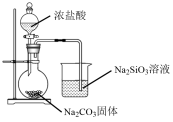 | 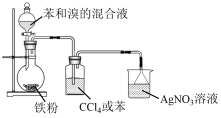 |  |
| 实验现象 | 试管内有白烟生成,内壁上有油状液滴生成 | 烧杯中出现白色沉淀 | 烧杯中出现淡黄色沉淀 | 有红热状的液珠落入蒸发皿内的细沙上,液珠冷却后变为黑色固体 |
| 实验结论 |  与 与 发生取代反应 发生取代反应 | 非金属性:Cl>C>Si | 苯与液溴在 催化下发生取代反应 催化下发生取代反应 | 黑色固体是 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
①活性炭、SO2和HClO都具有漂白作用,且漂白的化学原理相同
②第IA族元素铯的两种同位素137Cs比133Cs多4个质子
③因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S
④泥水、淀粉溶液、盐酸分别属于悬浊液、胶体、溶液
⑤碳酸氢根离子的电离方程式:HCO3-+H2O H3O++CO32-
H3O++CO32-
⑥从上到下,卤族元素的非金属性逐渐减弱,故氢卤酸的酸性依次减弱
⑦500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
①活性炭、SO2和HClO都具有漂白作用,且漂白的化学原理相同
②第IA族元素铯的两种同位素137Cs比133Cs多4个质子
③因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S
④泥水、淀粉溶液、盐酸分别属于悬浊液、胶体、溶液
⑤碳酸氢根离子的电离方程式:HCO3-+H2O
 H3O++CO32-
H3O++CO32-⑥从上到下,卤族元素的非金属性逐渐减弱,故氢卤酸的酸性依次减弱
⑦500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)
 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1| A.全部 | B.④⑤ | C.②③④⑦ | D.②④⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列叙述不正确的是
| A.碱性:LiOH>NaOH | B.沸点:C2H5OH>C2H6 |
| C.热稳定性:H2O>NH3 | D.溶解度:Na2CO3>NaHCO3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】化合物甲[YW(XV4)2]和化合物乙(ZXV4)常用于游泳池的净水和消毒。V、W、X、Y、Z原子序数依次增大,V、X在元素周期表中同族且相邻,其中V元素在地壳中含量最高;基态W原子有7种空间运动状态不同的电子,基态Y原子的价层电子排布式为4s1,Z位于元素周期表第四周期ds区,基态时有1个单电子。下列说法正确的是
| A.简单离子半径:X>Y | B.简单氢化物稳定性:V<X |
| C.单质的沸点:Z>V>X | D.最高价氧化物对应水化物碱性最强的是W |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】W、X、Y、Z、M为原子序数依次增大的短周期主族元素,其原子半径和最外层电子数的关系如图所示。下列说法正确的是


| A.简单离子半径:M>Y>Z |
| B.W2X2与Y2X2的化学键类型完全相同 |
| C.简单氢化物的沸点:M>X |
| D.最高价氧化物对应水化物的碱性:Z>Y |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是
| A.物质A由Z与Y两种元素组成,则0.5mol物质A中含有的离子数约为9.03×1023 |
| B.元素Y、Z、W形成的离子具有相同电子层结构,其离子半径依次增大 |
| C.元素Z、R的氧化物的水化物之间相互反应生成的盐溶液呈中性或碱性 |
| D.元素Y、R分别与元素X形成的化合物的沸点:XmY<XmR |
您最近一年使用:0次



