化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①哪一时间段反应速率最大________ min(填“0~1”,“1~2”,“2~3”,“3~4”或“4~5”),原因是______________________________ 。
②求3~4min时间段以盐酸的浓度变化来表示的该反应速率________ (设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是________ (填字母)。
A.蒸馏水 B.KCl溶液
C.KNO3溶液 D.Na2SO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
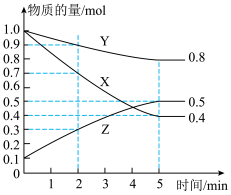
①该反应的化学方程式是_______________ 。
②该反应达到平衡状态的标志是________ (填字母)。
A.Y的体积分数在混合气体中保持不变
B.X、Y的反应速率比为3∶1
C.容器内气体压强保持不变
D.容器内气体的总质量保持不变
E.生成1molY的同时消耗2molZ
③2min内Y的转化率为________ 。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL(标准状况) | 100 | 240 | 464 | 576 | 620 |
②求3~4min时间段以盐酸的浓度变化来表示的该反应速率
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是
A.蒸馏水 B.KCl溶液
C.KNO3溶液 D.Na2SO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。

①该反应的化学方程式是
②该反应达到平衡状态的标志是
A.Y的体积分数在混合气体中保持不变
B.X、Y的反应速率比为3∶1
C.容器内气体压强保持不变
D.容器内气体的总质量保持不变
E.生成1molY的同时消耗2molZ
③2min内Y的转化率为
17-18高一下·江苏南通·期中 查看更多[18]
黑龙江省黑河市五校2021-2022学年高一下学期期末联考化学试题甘肃省永昌县第一高级中学2021-2022学年高一下学期期末考试化学试题辽宁省重点高中沈阳市联合体2021-2022高一下学期期中考试化学试题安徽省滁州市定远县育才学校2020-2021学年高一下学期期末考试化学试题吉林省延边朝鲜族自治州延边二中北校区2020-2021学年高一下学期第一次月考化学试题江苏省盱眙县都梁中学2020-2021学年高一下学期第一次学情检测化学试题四川省成都市简阳市阳安中学2020-2021学年高二上学期期中考试化学试题广西壮族自治区南宁市第三十六中学2019-2020学年高一上学期6月月考化学试题四川省眉山市仁寿第二中学2020-2021学年高二上学期10月月考理综化学试题吉林省长春外国语学校2019-2020学年高一下学期期末考试化学(理)试题陕西省西安中学2019-2020学年高一下学期期中考试化学试题(实验班)湖南省邵阳市第二中学2019-2020学年高一下学期5月考试化学试题辽宁省锦州市黑山县黑山中学2019-2020学年高一下学期线上教学检测化学试题湖北省武汉市第三十九中学2019-2020学年高一下学期线上期中考试化学试题苏教版高中化学必修2专题二《化学反应与能量转化》测试卷2020年春季苏教版高中化学必修2专题二《化学反应与能量转化》测试卷【校级联考】辽宁省六校协作体2018-2019学年高一下学期期中考试化学试题【全国百强校】江苏省海安中学2017-2018学年高一下学期期中考试化学试题(普通班)
更新时间:2020-05-29 22:42:10
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】一定温度下,反应3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g),在一密闭容器中进行,达平衡后,试回答:(A.变快 B.不变 C变慢,填字母代号)。
Fe3O4(s)+4H2(g),在一密闭容器中进行,达平衡后,试回答:(A.变快 B.不变 C变慢,填字母代号)。
(1)增加Fe的物质的量,其正反应速率__________ ,逆反应速率__________ 。
(2)将容器的体积缩小一半,其正反应速率________ ,逆反应速率_________ 。
(3)若保持体积不变,充入Ar,其逆反应速率________ ,逆反应速率_________ 。
(4)保持压强不变,充入Ar,其正反应速率__________ ,逆反应速率_________ 。
(5)使用催化剂,其正反应速率__________ ,逆反应速率_________ 。
 Fe3O4(s)+4H2(g),在一密闭容器中进行,达平衡后,试回答:(A.变快 B.不变 C变慢,填字母代号)。
Fe3O4(s)+4H2(g),在一密闭容器中进行,达平衡后,试回答:(A.变快 B.不变 C变慢,填字母代号)。(1)增加Fe的物质的量,其正反应速率
(2)将容器的体积缩小一半,其正反应速率
(3)若保持体积不变,充入Ar,其逆反应速率
(4)保持压强不变,充入Ar,其正反应速率
(5)使用催化剂,其正反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】填空题
(1)下列五种物质中,①H2O ②O2 ③Na2O2 ④NaOH ⑤NaBr,只存在共价键的是__________ ,只存在离子键的是__________ ,既存在离子键又存在共价键的是_________ ,含有极性键的是__________ ,是非极性分子的是________ 。(填编号)
(2)对于Fe+2HCl=FeCl2+H2↑,改变下列条件对生成氢气的速率有何影响?(填“增大”“减小”或“不变”)
①降低温度:________ ;
②增大盐酸浓度:________ ;
③增加铁丝的用量:________ 。
④加入催化剂:________ 。
(1)下列五种物质中,①H2O ②O2 ③Na2O2 ④NaOH ⑤NaBr,只存在共价键的是
(2)对于Fe+2HCl=FeCl2+H2↑,改变下列条件对生成氢气的速率有何影响?(填“增大”“减小”或“不变”)
①降低温度:
②增大盐酸浓度:
③增加铁丝的用量:
④加入催化剂:
您最近一年使用:0次
【推荐3】根据以下叙述,回答(1)~(2)小题。
大气中的臭氧层可滤除大量的紫外光,保护地球上的生物。氟利昂(如CCl2F2)可在光的作用下分解,产生Cl原子,Cl原子会对臭氧层产生长久的破坏作用,臭氧的分子式为O3。有关反应为:
O3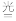 O2+O
O2+O
Cl+O3荣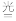 ClO+O2
ClO+O2
O+ClO=Cl+O2
总反应为2O3=3O2。
(1)在上述臭氧变成氧气的过程中,Cl原子是__ 。
A.反应物 B.生成物
C.中间产物 D.催化剂
(2)O3和O2是__ 。
A.同一种物质 B.同素异形体
C.氧的同位素 D.同一种元素
大气中的臭氧层可滤除大量的紫外光,保护地球上的生物。氟利昂(如CCl2F2)可在光的作用下分解,产生Cl原子,Cl原子会对臭氧层产生长久的破坏作用,臭氧的分子式为O3。有关反应为:
O3
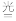 O2+O
O2+OCl+O3荣
 ClO+O2
ClO+O2O+ClO=Cl+O2
总反应为2O3=3O2。
(1)在上述臭氧变成氧气的过程中,Cl原子是
A.反应物 B.生成物
C.中间产物 D.催化剂
(2)O3和O2是
A.同一种物质 B.同素异形体
C.氧的同位素 D.同一种元素
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】某温度时,在2L容器中,某一反应中A、B的物质的量随时间变化的曲线如图所示,由图中数据分析得:
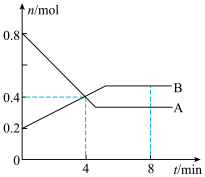
(1)在4min末时,A.B的物质的量浓度c(A)___ c(B);在该温度下达到化学平衡时c(A)___ c(B)(以上填“>”“<”或“=”);
(2)从反应开始至4min时,A的平均反应速率为___ ;
(3)该反应的化学方程式为___ 。

(1)在4min末时,A.B的物质的量浓度c(A)
(2)从反应开始至4min时,A的平均反应速率为
(3)该反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】为减弱温室效应,除了减少CO2的排放、植树造林、将液态CO2注入深海等措施外,还有一种思路是将CO2转化成其它可燃物质。如工业上已实现CO2和H2反应生成甲醇的转化。已知:在一恒温、恒容密闭容器中充入l mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H= -49.0 kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。请回答:
CH3OH(g)+H2O(g) △H= -49.0 kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。请回答:
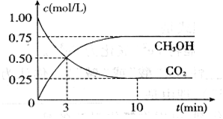
(1)达到平衡的时刻是____________ min(填“3”或“10”)。在前10min内,用CO2表示的反应速率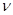 (CO2)=
(CO2)=________
(2)能判断该反应达到化学平衡状态的依据是____________ 。
a.容器压强不变 b.混合气体中c(CO2)不变
c.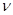 (CH3OH)=
(CH3OH)=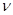 (H2O) d.c(CH3OH)=c(H2O)
(H2O) d.c(CH3OH)=c(H2O)
(3)为了提高H2的转化率,可采取__________ (填“增大”或“减小”)CO2浓度的措施。
(4)达平衡后,H2的转化率是_____________ 。平衡常数K=____________ 。(计算结果保留一位小数)
 CH3OH(g)+H2O(g) △H= -49.0 kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。请回答:
CH3OH(g)+H2O(g) △H= -49.0 kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如下图所示。请回答:
(1)达到平衡的时刻是
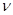 (CO2)=
(CO2)=(2)能判断该反应达到化学平衡状态的依据是
a.容器压强不变 b.混合气体中c(CO2)不变
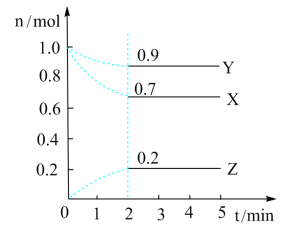
c.
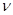 (CH3OH)=
(CH3OH)=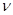 (H2O) d.c(CH3OH)=c(H2O)
(H2O) d.c(CH3OH)=c(H2O)(3)为了提高H2的转化率,可采取
(4)达平衡后,H2的转化率是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】某温度时,在一个 2 L 的密闭容器中,X、Y、Z 三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
(1)该反应在_____________ min 时达到平衡状态。
(2)该反应的化学方程式为___________________________________________ 。
(3)从开始至 2min,Z 的平均反应速率为____________________________________ 。

(1)该反应在
(2)该反应的化学方程式为
(3)从开始至 2min,Z 的平均反应速率为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】一定条件下,体积为1L的密闭容器中存在如下反应:
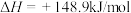 。
。
(1)下列各项中能说明该反应已达化学平衡状态的是_______ (填序号)。
a.v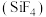 消耗=v
消耗=v 生成 b.容器内气体压强不再变化
生成 b.容器内气体压强不再变化
c.容器内气体的总质量不再变化 d.容器内HF体积分数不再变化
(2)反应过程中测定的部分数据如下表(表中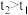 ):
):
通过计算a或b的值判断t1时刻反应是否达到化学平衡状态:_______ 。
(3)若只改变一个条件使上述反应的化学平衡常数变大,该反应_______ (填序号)。
a.一定向正反应方向移动 b.一定是增大压强造成的
c.一定是升高温度造成的 d.SiF4的平衡转化率一定增大
(4)反应进行到2min时,容器内气体的密度减小了0.03g/L,则这2min内: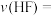
_______ 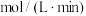 。
。

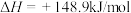 。
。(1)下列各项中能说明该反应已达化学平衡状态的是
a.v
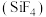 消耗=v
消耗=v 生成 b.容器内气体压强不再变化
生成 b.容器内气体压强不再变化c.容器内气体的总质量不再变化 d.容器内HF体积分数不再变化
(2)反应过程中测定的部分数据如下表(表中
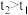 ):
):| 反应时间/min | n(SiF4)/mol | n(H2O)/mol |
| 0 | 1.20 | 2.40 |
| t1 | 0.80 | a |
| t2 | b | 1.60 |
(3)若只改变一个条件使上述反应的化学平衡常数变大,该反应
a.一定向正反应方向移动 b.一定是增大压强造成的
c.一定是升高温度造成的 d.SiF4的平衡转化率一定增大
(4)反应进行到2min时,容器内气体的密度减小了0.03g/L,则这2min内:
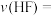
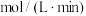 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
Ⅰ.脱硝:
已知:H2的燃烧热为285.8kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ·mol-1
H2O(g)=H2O(l) ΔH=-44kJ·mol-1
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为:____________ 。
Ⅱ.脱碳:
(1)向2L密闭容器中加入2molCO2和6molH2,在适当的催化剂作用下,发生反应:
CO2(g)+3H2(g) CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)
①该反应自发进行的条件是_____________ (填“低温”、“高温”或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是____________ 。(填字母)
a.混合气体的平均式量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1molCO2生成的同时有3mol H—H键断裂
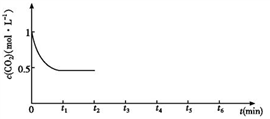
③CO2的浓度随时间(0~t2)变化如下图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t6 CO2浓度随时间的变化。_____________
⑵改变温度,使反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
①达到平衡时,反应Ⅰ、Ⅱ对比:平衡常数K(I)______ K(II)(填“﹥”“﹤”或“=”下同);平衡时CH3OH的浓度c(I)____ c(II)。
②对反应Ⅰ,前10min内的平均反应速率v(CH3OH)=_______ 。在其他条件不变的情况下,若30min时只改变温度T2℃,此时H2的物质的量为3.2mol,则T1___ T2(填“>”、“<”或“=”)。若30min时只向容器中再充入1molCO2(g)和1molH2O(g),则平衡_____ 移动(填“正向”“逆向”或“不”)。
⑶利用人工光合作用可将CO2转化为甲酸,反应原理为2CO2+2H2O=2HCOOH+O2,
装置如图所示:
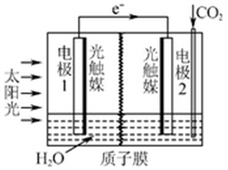
①电极2的电极反应式是____________ ;
②在标准状况下,当电极2室有11.2L CO2反应。 理论上电极1室液体质量_____ (填“增加”或“减少”______ g。
Ⅰ.脱硝:
已知:H2的燃烧热为285.8kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ·mol-1
H2O(g)=H2O(l) ΔH=-44kJ·mol-1
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为:
Ⅱ.脱碳:
(1)向2L密闭容器中加入2molCO2和6molH2,在适当的催化剂作用下,发生反应:
CO2(g)+3H2(g)
 CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)①该反应自发进行的条件是
②下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均式量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1molCO2生成的同时有3mol H—H键断裂
③CO2的浓度随时间(0~t2)变化如下图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t6 CO2浓度随时间的变化。

⑵改变温度,使反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应Ⅰ:恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应Ⅱ:绝热恒容 | 0min | 0 | 0 | 2 | 2 |
①达到平衡时,反应Ⅰ、Ⅱ对比:平衡常数K(I)
②对反应Ⅰ,前10min内的平均反应速率v(CH3OH)=
⑶利用人工光合作用可将CO2转化为甲酸,反应原理为2CO2+2H2O=2HCOOH+O2,
装置如图所示:

①电极2的电极反应式是
②在标准状况下,当电极2室有11.2L CO2反应。 理论上电极1室液体质量
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】氮循环与人类生活、社会发展息息相关。回答下列问题:
(1)用化学方程式表示实验室制备 的原理:
的原理:___________ 。
(2) 是一种重要的化工原料,工业上利用
是一种重要的化工原料,工业上利用 制备
制备 的流程如图所示:
的流程如图所示:

上述反应中,气体颜色发生变化的是___________ ,反应后分子数增加的是___________ (均填序号)。
(3)在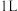 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,在不同温度(
,在不同温度( )下发生反应
)下发生反应 ,测得
,测得 的浓度(
的浓度( ,单位:
,单位: )随反应时间(
)随反应时间( )的变化情况如表所示:
)的变化情况如表所示:
①下列说法中,不能说明反应 达到平衡状态的是
达到平衡状态的是___________ (填标号)。
a.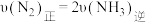 b.断裂
b.断裂 时断裂
时断裂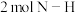
c.混合气体的密度保持不变 d.混合气体的压强保持不变
② 时,在
时,在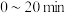 内,
内, 的平均反应速率为
的平均反应速率为___________  ,
,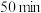 时,
时, 的转化率为
的转化率为___________ %( 的转化率是指已被转化的
的转化率是指已被转化的 的物质的量与其初始的物质的量之比)。
的物质的量与其初始的物质的量之比)。
③由表格中的数据可知, 时,反应达到平衡所需要的时间
时,反应达到平衡所需要的时间
___________ (填“ ”“
”“ ”或“
”或“ ”)
”)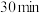 ,说明理由:
,说明理由:___________ 。
(1)用化学方程式表示实验室制备
 的原理:
的原理:(2)
 是一种重要的化工原料,工业上利用
是一种重要的化工原料,工业上利用 制备
制备 的流程如图所示:
的流程如图所示:
上述反应中,气体颜色发生变化的是
(3)在
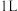 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,在不同温度(
,在不同温度( )下发生反应
)下发生反应 ,测得
,测得 的浓度(
的浓度( ,单位:
,单位: )随反应时间(
)随反应时间( )的变化情况如表所示:
)的变化情况如表所示:| 实验序号 |  |  | |||||
| 0 | 10 | 20 | 30 | 40 | 50 | ||
| 1 | 400 | 0 | 0.20 | 0.34 | 0.43 | 0.50 | 0.50 |
| 2 | 500 | 0 | 0.25 | 0.40 | 0.48 | 0.48 | 0.48 |
| 3 | 600 | 0 | 0.28 | 0.45 | 0.45 | ||
 达到平衡状态的是
达到平衡状态的是a.
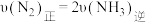 b.断裂
b.断裂 时断裂
时断裂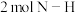
c.混合气体的密度保持不变 d.混合气体的压强保持不变
②
 时,在
时,在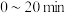 内,
内, 的平均反应速率为
的平均反应速率为 ,
,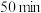 时,
时, 的转化率为
的转化率为 的转化率是指已被转化的
的转化率是指已被转化的 的物质的量与其初始的物质的量之比)。
的物质的量与其初始的物质的量之比)。③由表格中的数据可知,
 时,反应达到平衡所需要的时间
时,反应达到平衡所需要的时间
 ”“
”“ ”或“
”或“ ”)
”)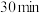 ,说明理由:
,说明理由:
您最近一年使用:0次



