(1)M能层上有________ 个能级,有________ 个轨道,作为内层最多可容纳________ 个电子,作为最外层时,最多可含有________ 个未成对电子。
(2)E原子核外电子占有9个轨道,且具有1个未成对电子,E离子结构示意图是____________ 。
(3)F、G都是短周期元素,F2-与G3+的电子层结构相同,则G元素的原子序数是________ ,F2-的电子排布式是______________ 。
(2)E原子核外电子占有9个轨道,且具有1个未成对电子,E离子结构示意图是
(3)F、G都是短周期元素,F2-与G3+的电子层结构相同,则G元素的原子序数是
更新时间:2020-06-09 15:05:11
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】现有A、B、C、D、E五种元素,均为前四周期元素、它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1)写出下列元素的元素符号:B:___________ C:___________ D:___________
(2)用元素符号表示A2B2的电子式为___________ 。
(3)E元素在元素周期表的位置为:___________ ,属于___________ 区,它有___________ 个能层。
(4)D原子核外电子排布式为___________ , 离子价层电子轨道表示式为
离子价层电子轨道表示式为___________ , 价层电子排布式的特点是
价层电子排布式的特点是___________ 。
(5)检验某溶液中是否含有 ,通常所用的试剂是
,通常所用的试剂是___________ 和___________ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都低于同周期相邻元素 |
| C元素基态原子核外有17个不同运动状态的电子 |
| D元素位于元素周期表中的第八列,在地壳中的含量居前四位 |
| E元素基态原子的M层全充满,N层没有成对电子,只有1个未成对电子 |
(2)用元素符号表示A2B2的电子式为
(3)E元素在元素周期表的位置为:
(4)D原子核外电子排布式为
 离子价层电子轨道表示式为
离子价层电子轨道表示式为 价层电子排布式的特点是
价层电子排布式的特点是(5)检验某溶液中是否含有
 ,通常所用的试剂是
,通常所用的试剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】根据表中提供的部分短周期元素原子半径及主要化合价的信息,回答下列问题
(1)A在元素周期表中位置是____ 。
(2)B的离子结构示意图:_____ ,
(3)C单质与A的最高价氧化物对应的水化物反应的离子方程式:____ 。
(4)元素最高价氧化物对应的水化物酸性最强的是:____ (写化学式)。
(5)A元素与F元素形成的化合物的电子式_____ 。
| 元素代号 | A | B | C | D | E | F | G |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.112 | 0.104 | 0.099 | 0.066 |
| 主要化合价 | +1 | +2 | +3 | +2 | +6、-2 | +7、-1 | -2 |
(1)A在元素周期表中位置是
(2)B的离子结构示意图:
(3)C单质与A的最高价氧化物对应的水化物反应的离子方程式:
(4)元素最高价氧化物对应的水化物酸性最强的是:
(5)A元素与F元素形成的化合物的电子式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】已知A、B、C、D、E五种元素的原子序数依次增大,其中A、B、C、D为短周期元素,且只有A、D为非金属元素。A的氢化物溶于水得到的溶液能使酚酞溶液变红。B、C、D的最高价氧化物对应水化物相互之间能够两两反应,且D原子最外层电子数是C原子最外层电子数的2倍。B、E元素同主族,且原子序数相差8。
(1)E在元素周期表中的位置:___________ ,写出E的最高价氧化物对应水化物与C的单质反应的化学方程式:___________ 。
(2)A的氢化物溶于水后的电离方程式为___________ ;实验室制备A的氢化物的化学方程式为___________ 。
(3)B单质在空气中燃烧后的产物为___________ ,写出该产物和水反应的离子方程式:___________ 。
(1)E在元素周期表中的位置:
(2)A的氢化物溶于水后的电离方程式为
(3)B单质在空气中燃烧后的产物为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】按所示格式填写下表。
| 微粒符号 | 原子序数 | 电子排布式 | 外围电子排布式 |
 | |||
 | |||
 | |||
 | 30 | ||
 | 26 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。某FexNy的制备需铁、氮气、丙酮和乙醇参与。
(1)Fe3+基态核外电子排布式为____________________ 。Fe与N相比,第一电离能较大的是_______________ 。
(2)丙酮( )分子中碳原子轨道的杂化类型为
)分子中碳原子轨道的杂化类型为_______________ 和_______________ 。
(3)C、N、O三种元素形成的氢化物沸点从高到低的顺序为:_____________ ,原因是________________ 。
(4)1molN2分子中含有σ键____________ mol,含π键______________ mol。
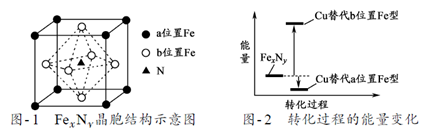
(5)某FexNy的晶胞如图−1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x−n) CunNy。FexNy转化为两种Cu替代型产物的能量变化如图−2所示,其中更稳定的Cu替代型产物的化学式为___________ 。
(1)Fe3+基态核外电子排布式为
(2)丙酮(
 )分子中碳原子轨道的杂化类型为
)分子中碳原子轨道的杂化类型为(3)C、N、O三种元素形成的氢化物沸点从高到低的顺序为:
(4)1molN2分子中含有σ键
(5)某FexNy的晶胞如图−1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物Fe(x−n) CunNy。FexNy转化为两种Cu替代型产物的能量变化如图−2所示,其中更稳定的Cu替代型产物的化学式为

您最近一年使用:0次
【推荐3】根据已学知识,请回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是L,占据该能层电子的原子轨道形状为_______ 。
(2)写出3p轨道上有2个未成对电子的元素的符号:_______ 。
(3)已知铬是24号元素,画出Cr的价层电子排布图:_______ 。
(4)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为_______ ,电负性由大到小的顺序是_______ 。
(5)Zn2+的核外电子排布式为_______ 。
(1)基态N原子中,核外电子占据的最高能层的符号是L,占据该能层电子的原子轨道形状为
(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)已知铬是24号元素,画出Cr的价层电子排布图:
(4)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为
(5)Zn2+的核外电子排布式为
您最近一年使用:0次



