五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性。回答下列问题:
(1)五种元素中,原子半径最大的是__________ ,非金属性最强的是__________ (填元素符号);
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是__________ (用化学式表示);
(3)A和E形成的化合物与A和B形成的化合物反应,产物的电子式为_______________ 。
(1)五种元素中,原子半径最大的是
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是
(3)A和E形成的化合物与A和B形成的化合物反应,产物的电子式为
18-19高一下·江西南昌·阶段练习 查看更多[1]
(已下线)【南昌新东方】2019-2020 南大附中 高一下 第三次月考
更新时间:2020-06-16 16:48:26
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】短周期主族元素A、B、C、D、E、G的原子序数依次增大,在元素周期表中A的原子半径最小(稀有气体元素除外),B与C相邻且C的最外层电子数是次外层的3倍,C、D的最外层电子数之和与G的最外层电子数相等,E是地壳中含量最多的金属元素。回答下列问题:
(1)C在元素周期表中的位置是__________ ;由C和D组成既含离子键又含共价键的化合物的电子式__________ 。
(2)分别由C、D、E、G元素形成的简单离子的半径由大到小的顺序为__________ (用相应的离子符号表示)。
(3)写出实验室中制备G元素的单质的离子方程式______________________________
(4)E单质能写D的最高价氧化物的水化物浓溶液反应放出氢气,反应的离子方程式是:__________ 由上述六种元素中的三种组成的某种盐,是漂白液的主要成分,将该盐溶液滴入硫酸酸化的KI淀粉溶液中,溶液变为蓝色,则反应的化学方程式为________________________________________ .
(1)C在元素周期表中的位置是
(2)分别由C、D、E、G元素形成的简单离子的半径由大到小的顺序为
(3)写出实验室中制备G元素的单质的离子方程式
(4)E单质能写D的最高价氧化物的水化物浓溶液反应放出氢气,反应的离子方程式是:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】有A、B、C、D四种元素,A元素的原子有三个电子层,最外层上有一个电子:B元素-2价阴离子的电子层结构与氩原子相同;C元素的原子核内无中子:D原子核外电子数比A原子核外电子总数多6个。
(1)写出A、B、C、D四种元素的符号:A________ 、B________ 、C________ 、D________ 。
(2)写出与A的电子层结构相同的两种离子的离子符号________ 、________ 。
(3)写出B离子的电子式________________ ,D原子的结构示意图________________ 。
(1)写出A、B、C、D四种元素的符号:A
(2)写出与A的电子层结构相同的两种离子的离子符号
(3)写出B离子的电子式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】硼氢化钠( )是一种常用的络合金属氢化物还原剂,在化学反应中有很高的选择性。以硼氢化钠反应后生成的副产物偏硼酸钠(
)是一种常用的络合金属氢化物还原剂,在化学反应中有很高的选择性。以硼氢化钠反应后生成的副产物偏硼酸钠( )为原料,结合改进后的Bayer法制备硼氢化钠的工艺流程如下:
)为原料,结合改进后的Bayer法制备硼氢化钠的工艺流程如下:
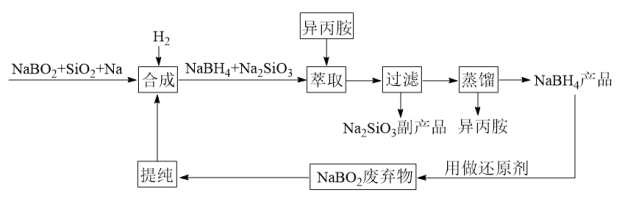
回答下列问题
(1)写出 的电子式
的电子式_______ 。
(2)合成时,需要将石英晶体粉碎,其目的是_______ 。
(3)实验室完成过滤时,需要用到的玻璃仪器有漏斗、烧杯和_______ 。
(4)从煤油中取出金属钠后,需要先_______ (简述操作),再用石油醚洗涤。
(5)合成反应中氧化剂与还原剂的质量比为_______ 。
(6)流程中可以循环利用的物质除 外,还有
外,还有_______ 。
(7) 做还原剂时需控制溶液为弱碱性.若酸性较强,
做还原剂时需控制溶液为弱碱性.若酸性较强, 易与水反应放出
易与水反应放出 ,写出反应的离子方程式
,写出反应的离子方程式_______ 。
 )是一种常用的络合金属氢化物还原剂,在化学反应中有很高的选择性。以硼氢化钠反应后生成的副产物偏硼酸钠(
)是一种常用的络合金属氢化物还原剂,在化学反应中有很高的选择性。以硼氢化钠反应后生成的副产物偏硼酸钠( )为原料,结合改进后的Bayer法制备硼氢化钠的工艺流程如下:
)为原料,结合改进后的Bayer法制备硼氢化钠的工艺流程如下:
回答下列问题
(1)写出
 的电子式
的电子式(2)合成时,需要将石英晶体粉碎,其目的是
(3)实验室完成过滤时,需要用到的玻璃仪器有漏斗、烧杯和
(4)从煤油中取出金属钠后,需要先
(5)合成反应中氧化剂与还原剂的质量比为
(6)流程中可以循环利用的物质除
 外,还有
外,还有(7)
 做还原剂时需控制溶液为弱碱性.若酸性较强,
做还原剂时需控制溶液为弱碱性.若酸性较强, 易与水反应放出
易与水反应放出 ,写出反应的离子方程式
,写出反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】(1)现有A、B、X、Y、Z五种短周期元素,原子序数依次增大。它们的性质或原子结构如下表:
请回答:
①X元素在元素周期表中的位置是______________ ;
②Z单质通入Y的最高价氧化物对应水化物的溶液中,可以得到漂白液,相应反应的离子方程式为___________________________________________________ ;
③化合物甲由A和B两种元素组成且质量比为3:14,甲与X单质在催化剂、加热条件下发生的反应是工业上制取硝酸的基础,写出该反应的化学方程式____________ 。
(2)短周期元素X、Y、Z在周期表中的位置关系如图所示
①X元素单质的化学式是_________ ,若X核内中子数与质子数相等,则X单质的摩尔质量为________ ;
②Y单质的电子式是_________ ;Z与钙形成的化合物的电子式是__________ 。
| 元素 | 性质或原子结构 |
| A | 原子核内只有一个质子 |
| B | 单质是空气中含量最多的气体 |
| X | 原子的最外层电子数是次外层电子数的3倍 |
| Y | 短周期元素中原子半径最大的元素 |
| Z | 最高正化合价与最低负化合价的代数和为6 |
①X元素在元素周期表中的位置是
②Z单质通入Y的最高价氧化物对应水化物的溶液中,可以得到漂白液,相应反应的离子方程式为
③化合物甲由A和B两种元素组成且质量比为3:14,甲与X单质在催化剂、加热条件下发生的反应是工业上制取硝酸的基础,写出该反应的化学方程式
(2)短周期元素X、Y、Z在周期表中的位置关系如图所示
| X | ||
| Y | ||
| Z |
②Y单质的电子式是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】元素X、Y、Z、M、R均为短周期主族元素,且原子序数依次增大。已知:Y为地壳中含量最多的元素,M原子的最外层电子数与次外层电数之比为3:4;R-、Z+、X+离子半径逐渐减小;化合物XR常温下为气体,请回答下列问题:
(1)M在元素周期表中的位置__ ;Z+离子的结构示意图为__ 。
(2)写出X、Y、R按原子个数之比1:1:1形成的化合物的电子式__ 。
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式__ 。
(4)实验室制备R的单质,该反应的离子方程式为__ 。
(5)R非金属性强于M,下列选项中能证明这一事实的是__ (填字母序号)。
A.常温下的R单质熔沸点比M单质的高
B.R的氢化物比M的氢化物更稳定
C.一定条件下R和M的单质都能与NaOH溶液反应
D.最高价氧化物对应水化物的酸性强弱:R>M
(6)由X、Y、Z、M四种元素组成的一种弱酸酸式盐A。向A溶液中通入氯气,得到无色溶液,写出该反应的离子方程式__ 。
(1)M在元素周期表中的位置
(2)写出X、Y、R按原子个数之比1:1:1形成的化合物的电子式
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式
(4)实验室制备R的单质,该反应的离子方程式为
(5)R非金属性强于M,下列选项中能证明这一事实的是
A.常温下的R单质熔沸点比M单质的高
B.R的氢化物比M的氢化物更稳定
C.一定条件下R和M的单质都能与NaOH溶液反应
D.最高价氧化物对应水化物的酸性强弱:R>M
(6)由X、Y、Z、M四种元素组成的一种弱酸酸式盐A。向A溶液中通入氯气,得到无色溶液,写出该反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】有A、B、C、D、E5种元素,已知:
①A原子最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子第三层上的电子比第一层多5个。
②常温下B2是气体,相同条件下,它的密度是氢气的16倍。
③C的单质在B2中燃烧,生成淡黄色固体F。F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2。D在DB2中的含量为50%。根据以上情况回答:
(1)D是____________ ,其在周期表中的位置为______________ 。
(2)E的原子结构示意图为____________ ,C的离子结构示意图为___________ 。
(3)F和AB2反应的化学方程式为________________________________________ 。
(4)F中含有的化学键为__________________ 。
①A原子最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子第三层上的电子比第一层多5个。
②常温下B2是气体,相同条件下,它的密度是氢气的16倍。
③C的单质在B2中燃烧,生成淡黄色固体F。F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2。D在DB2中的含量为50%。根据以上情况回答:
(1)D是
(2)E的原子结构示意图为
(3)F和AB2反应的化学方程式为
(4)F中含有的化学键为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】下表列出了9种元素在元素周期表中的位置。

请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是_______
(2)画出元素⑧形成的简单离子的结构示意图_______
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为_______
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是_______
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是_______ (填化学式)
(6)写出元素⑥的单质与水反应的离子反应方程式_______
(7)写出一个能证明元素⑧比元素⑨非金属性强的反应事实的离子方程式_______

请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是
(2)画出元素⑧形成的简单离子的结构示意图
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是
(6)写出元素⑥的单质与水反应的离子反应方程式
(7)写出一个能证明元素⑧比元素⑨非金属性强的反应事实的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】已知 、
、 、
、 、
、 四种元素的核电荷数依次增大,
四种元素的核电荷数依次增大, 原子最外层电子数是次外层电子数的2倍;
原子最外层电子数是次外层电子数的2倍; 元素在地壳中含量最多;
元素在地壳中含量最多; 原子最外层电子数与
原子最外层电子数与 原子最外层电子数相等,且
原子最外层电子数相等,且 原子比
原子比 原子多一个电子层;
原子多一个电子层; 原子与
原子与 原子具有相同的电子层数,且
原子具有相同的电子层数,且 原子内层电子总数比最外层电子数多3。试回答下列问题:
原子内层电子总数比最外层电子数多3。试回答下列问题:
(1)写出四种元素的名称:
____________ ;
____________ ;
____________ ;
____________ 。
(2) 原子的结构示意图为
原子的结构示意图为________________________ 。
(3) 的阴离子的结构示意图为
的阴离子的结构示意图为________________________ 。
 、
、 、
、 、
、 四种元素的核电荷数依次增大,
四种元素的核电荷数依次增大, 原子最外层电子数是次外层电子数的2倍;
原子最外层电子数是次外层电子数的2倍; 元素在地壳中含量最多;
元素在地壳中含量最多; 原子最外层电子数与
原子最外层电子数与 原子最外层电子数相等,且
原子最外层电子数相等,且 原子比
原子比 原子多一个电子层;
原子多一个电子层; 原子与
原子与 原子具有相同的电子层数,且
原子具有相同的电子层数,且 原子内层电子总数比最外层电子数多3。试回答下列问题:
原子内层电子总数比最外层电子数多3。试回答下列问题:(1)写出四种元素的名称:




(2)
 原子的结构示意图为
原子的结构示意图为(3)
 的阴离子的结构示意图为
的阴离子的结构示意图为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】A、B、C、D都是短周期元素,原子半径D>C>A>B,其中A、B处于同一周期,A 的最外层电子数是次外层电子数的2倍,A、C处于同一主族。C原子核内的质子数等于A、B原子核内的质子数之和,C原子最外层电子数是D原子最外层电子数的4倍。试回答下列问题。
(1)元素分别是:A_______ ,D_______ (填元素名称)。
(2)A、B2种元素分别形成的气态氢化物的稳定性由小到大的顺序是_______ 。(填化学式)
(3)A与B形成的三原子分子的电子式是_______ 。组成的化合物属于_______ (填“离子化合物”或“共价化合物”),B与D形成的原子个数之比为1∶1的化合物的电子式是_______ ,含有的化学键是_______ 和_______ 。
(4)用电子式表示化合物D2B的形成过程_______ 。
(1)元素分别是:A
(2)A、B2种元素分别形成的气态氢化物的稳定性由小到大的顺序是
(3)A与B形成的三原子分子的电子式是
(4)用电子式表示化合物D2B的形成过程
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】已知X、Y、Z、M、G、Q是六种短周期主族元素,原子序数依次增大。X、Z、Q的单质在常温下呈气态:Y的原子最外层电子数是其电子层数的2倍:X与M同主族;Z、G分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)Z在元素周期表中的位置为__________ 。
(2)M、G的阳离子氧化性更强的是(写化学式)________ 。
(3)Z和Q的最低价氢化物沸点更高的是(写化学式)_________ 。
(4)上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式)________ 。
(5) M2Z2的电子式为________ 。
(6)常温下,能与G的单质发生反应的是(填字母序号)________ 。
A. CuSO4溶液 B.浓硫酸 C. NaOH溶液 D.Na2CO3固体
请回答下列问题:
(1)Z在元素周期表中的位置为
(2)M、G的阳离子氧化性更强的是(写化学式)
(3)Z和Q的最低价氢化物沸点更高的是(写化学式)
(4)上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式)
(5) M2Z2的电子式为
(6)常温下,能与G的单质发生反应的是(填字母序号)
A. CuSO4溶液 B.浓硫酸 C. NaOH溶液 D.Na2CO3固体
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】Ⅰ. 元素X、Y、Z、W、Q在元素周期表中的相对位置如下图所示。
(1)元素X在周期表中的位置是第_______ 周期,第_______ 族。
(2)五种元素中离子半径最小的是_______ 。
Ⅱ. 下图是部分短周期主族元素原子半径与原子序数的关系。

(3)X的元素符号:_______ 。
(4)Y与Z形成的是_______ 化合物。(填“离子”或“共价”)
(5)上述元素的最高价含氧酸中酸性最强的是_______ (填化学式)。
Ⅲ.(6)下列关于元素及其化合物性质的判断中,正确的是_______ (填序号)
A. 元素甲的氢氧化物只有碱性,而元素乙的氢氧化物具有两性,所以金属性:甲>乙
B. 元素甲最外层只有一个电子,而乙最外层有两个电子,所以金属性:甲>乙
C. 金属元素 、
、 能分别形成+2、+3价离子,所以氧化性:
能分别形成+2、+3价离子,所以氧化性: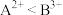
D. 因为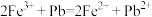 ,所以金属性:
,所以金属性:
E. 因为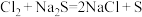 ,所以非金属性:
,所以非金属性:
F. 因为水溶液的酸性: ,所以非金属性:
,所以非金属性:
G. 是一元酸,而
是一元酸,而 是二元酸,所以酸性:
是二元酸,所以酸性: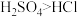
Ⅳ.(7)甲同学查阅资料知:氨气( )的分解温度在850℃以上,甲烷(
)的分解温度在850℃以上,甲烷( )的分解温度是655℃,据此得出结论:N元素的非金属性强于C元素。乙同学对此结论持怀疑态度,甲同学通过实验间接证明了自己的结论。你认为甲同学的实验方案是(请结合离子方程式简要说明):
)的分解温度是655℃,据此得出结论:N元素的非金属性强于C元素。乙同学对此结论持怀疑态度,甲同学通过实验间接证明了自己的结论。你认为甲同学的实验方案是(请结合离子方程式简要说明):_______ 。
| X | Y | ||||
| Z | W | Q |
(2)五种元素中离子半径最小的是
Ⅱ. 下图是部分短周期主族元素原子半径与原子序数的关系。

(3)X的元素符号:
(4)Y与Z形成的是
(5)上述元素的最高价含氧酸中酸性最强的是
Ⅲ.(6)下列关于元素及其化合物性质的判断中,正确的是
A. 元素甲的氢氧化物只有碱性,而元素乙的氢氧化物具有两性,所以金属性:甲>乙
B. 元素甲最外层只有一个电子,而乙最外层有两个电子,所以金属性:甲>乙
C. 金属元素
 、
、 能分别形成+2、+3价离子,所以氧化性:
能分别形成+2、+3价离子,所以氧化性: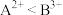
D. 因为
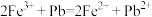 ,所以金属性:
,所以金属性:
E. 因为
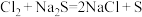 ,所以非金属性:
,所以非金属性:
F. 因为水溶液的酸性:
 ,所以非金属性:
,所以非金属性:
G.
 是一元酸,而
是一元酸,而 是二元酸,所以酸性:
是二元酸,所以酸性: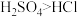
Ⅳ.(7)甲同学查阅资料知:氨气(
 )的分解温度在850℃以上,甲烷(
)的分解温度在850℃以上,甲烷( )的分解温度是655℃,据此得出结论:N元素的非金属性强于C元素。乙同学对此结论持怀疑态度,甲同学通过实验间接证明了自己的结论。你认为甲同学的实验方案是(请结合离子方程式简要说明):
)的分解温度是655℃,据此得出结论:N元素的非金属性强于C元素。乙同学对此结论持怀疑态度,甲同学通过实验间接证明了自己的结论。你认为甲同学的实验方案是(请结合离子方程式简要说明):
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】元素周期表的一部分如下表,根据该表回答下列问题:
(1)②③④分别与①形成含有10个电子的分子的化学式依次为___________ 、___________ 、___________ 。
(2)上述元素中,非金属性最强的元素是___________ (填元素符号),最高价氧化物对应水化物的酸性最强的是___________ (填酸的化学式)。
(3)⑤的单质着火时不能用水来灭火,原因之一是其燃烧的产物能与水反应,该反应的化学方程式为___________ ,该反应中产生标准状况下22.4L的气体时,转移的电子的数目为___________ (用含NA的代数式表示)。
(4)在加热条件下,⑥的氢化物的浓溶液与MnO2反应可制得⑥的单质,该反应中,氧化剂与还原剂的物质的量之比为___________ ,将①的单质在⑥的单质中点燃,可观察到的现象为___________ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ |
(2)上述元素中,非金属性最强的元素是
(3)⑤的单质着火时不能用水来灭火,原因之一是其燃烧的产物能与水反应,该反应的化学方程式为
(4)在加热条件下,⑥的氢化物的浓溶液与MnO2反应可制得⑥的单质,该反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次



