(1)原电池中发生的化学反应属于________ ,原电池将________ 能转化成________ 能。
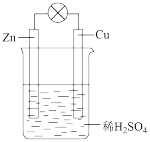
(2)如图为铜锌原电池:此电池中锌做________ (填:正或负)极,发生________ (填:氧化或还原)反应;铜极的电极方程式为________ ,电子流动的方向是:________ (填:铜→锌或锌→铜)。
(3)工业上冶炼金属钠的方程式为:________ ,冶炼方法是:________ ;氧化铁和铝粉发生铝热反应的化学方程式为:________ 。铝热反应的用途:________ (写出一种);工业上常用乙烯和水在一定条件下制取乙醇,其化学方程式为:________ 。
(2)如图为铜锌原电池:此电池中锌做

(3)工业上冶炼金属钠的方程式为:
更新时间:2020/06/18 21:35:45
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】化学与人类生活、生产密切相关。请根据题意填空:
(1)高温下铝粉与氧化铁的反应可用来焊接钢轨。该反应的化学方程式为2Al+Fe2O3 =Al2O3+2Fe,其中还原剂是
=Al2O3+2Fe,其中还原剂是____ ;
(2)可净化水中悬浮物使水变澄清的是____ (填“NaCl”或“明矾”)。
(3)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装___ (填“浓硫酸”或“浓盐酸”)。
(1)高温下铝粉与氧化铁的反应可用来焊接钢轨。该反应的化学方程式为2Al+Fe2O3
 =Al2O3+2Fe,其中还原剂是
=Al2O3+2Fe,其中还原剂是(2)可净化水中悬浮物使水变澄清的是
(3)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应,如图所示。

(1)写出图中铝热反应的化学方程式:_______ 。
(2)下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是_______。

(1)写出图中铝热反应的化学方程式:
(2)下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是_______。
A.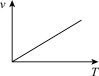 | B.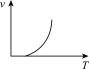 | C.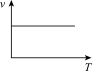 | D.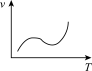 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】(1)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6mol电子时,所得还原产物的物质的量为___________ mol。
(2)用铝粉和 做铝热反应实验,需要的试剂还有
做铝热反应实验,需要的试剂还有___________ (填序号)。
a.KCl b.KClO3 c. d.Mg
d.Mg
取少量铝热反应所得的固体混合物,将其溶于足量稀 ,滴加KSCN溶液无明显现象,
,滴加KSCN溶液无明显现象,______ (填“能”或“不能”)说明固体混合物中无 ,理由是
,理由是_________ (用离子方程式说明)。
(2)用铝粉和
 做铝热反应实验,需要的试剂还有
做铝热反应实验,需要的试剂还有a.KCl b.KClO3 c.
 d.Mg
d.Mg取少量铝热反应所得的固体混合物,将其溶于足量稀
 ,滴加KSCN溶液无明显现象,
,滴加KSCN溶液无明显现象, ,理由是
,理由是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)把一块纯净的锌片插入盛有稀硫酸的烧杯里,可观察到锌片逐渐溶解,并有气体产生,再平行地插入一块铜片(如图甲所示),可观察到铜片上____ (填“有”或“没有”)气泡产生,再用导线把锌片和铜片连接起来(如图乙所示),可观察到铜片上_________ (填“有”或“没有”)气泡产生。
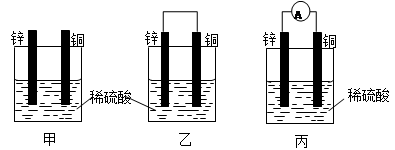
(2)用导线连接灵敏电流表的两端后,再与溶液中的锌片和铜片相连(如图丙所示),观察到灵敏电流表的指针发生了偏转,说明了导线中有电流通过。从上述现象中可以归纳出构成原电池的一些条件是___________________________ 和 _________________________________ ,
有关的电极反应式:锌片_________________________ ;铜片___________________________ 。
(3)图乙、图丙是一个将___________ 能转化为 _________ 能的装置,人们把它叫做原电池。

(2)用导线连接灵敏电流表的两端后,再与溶液中的锌片和铜片相连(如图丙所示),观察到灵敏电流表的指针发生了偏转,说明了导线中有电流通过。从上述现象中可以归纳出构成原电池的一些条件是
有关的电极反应式:锌片
(3)图乙、图丙是一个将
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】某实验室备有如下实验用品:铁片、铜片、锌片、碳棒、FeCl3溶液、ZnCl2溶液、CuSO4溶液、AgNO3溶液以及导线。试回答下列问题:
(1)若选用铁片、铜片、AgNO3溶液及导线,_______ (填“能”或“不能”)构成原电池。
(2)判断该电池的正极材料是_______ ,负极材料是_______ ,正极反应式是_______ ,负极反应式是 _______ ,电池总反应式是_______ 。
(1)若选用铁片、铜片、AgNO3溶液及导线,
(2)判断该电池的正极材料是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】甲醇(CH3OH)—空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如下图:
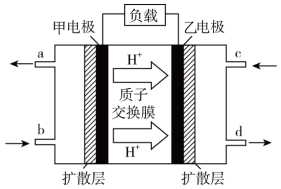
(1)图中左侧电极为电源_______ 极,该电极的电极反应式为:__________ 。
(2)当电池消耗甲醇6.4g时,消耗的O2的体积为___________ L(标况下)。

(1)图中左侧电极为电源
(2)当电池消耗甲醇6.4g时,消耗的O2的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】为解决化石能源面临的困境,人们大力开发新能源。
(1)氢气是未来非常理想能源,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作激光用使海水分解得到氢气的新技术:2H2O 2H2+O2。制得的氢气可用于燃料电池、合成氨工业。分解海水时,
2H2+O2。制得的氢气可用于燃料电池、合成氨工业。分解海水时,
(2)利用下列反应:Fe+2Fe3+=3Fe2+设计一个原电池,请选择适当的材料和试剂。
①在方框中画出设计的原电池示意图

②负极反应式:
③溶液中Fe3+向
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】通过化学方法可使能量按人们所期望的形式转化,从而开辟新能源和提高能量转化率。回答下列问题:
(1)根据构成原电池本质判断,如下反应可以设计成原电池的是_______(填标号)。
(2)如图是甲烷燃料电池的工作原理示意图。
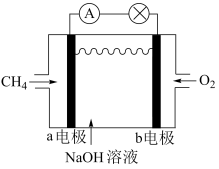
①电池的负极是_______ 电极(填“a”或“b”),该极的电极反应为_______ 。
②工作一段时间后,当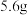 甲烷完全反应后,外电路中通过的电子数目为
甲烷完全反应后,外电路中通过的电子数目为_______ 。
③反应一段时间后,溶液的
_______ (填“增大”、“不变”或“减小”)。
(1)根据构成原电池本质判断,如下反应可以设计成原电池的是_______(填标号)。
A.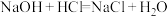 | B.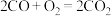 |
C.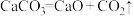 | D.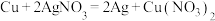 |

①电池的负极是
②工作一段时间后,当
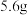 甲烷完全反应后,外电路中通过的电子数目为
甲烷完全反应后,外电路中通过的电子数目为③反应一段时间后,溶液的

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】已知有关物质的熔沸点数据如下表:
请参考上述数据回答问题:
(1)工业上常用电解熔融MgCl2的方法生产金属镁;用电解Al2O3与冰晶石熔融混合物的方法生产铝。不用电解MgO的方法生产镁的原因是:______ ;不用电解AlCl3的方法生产铝的原因是:______ 。
(2)请设计可靠的实验证明MgCl2、AlCl3所属化合物的类型,其实验方法是______ 。
(3)AlCl3具有以下______ 性质(请填序号)
①液化 ②挥发 ③升华
| MgO | Al2O3 | MgCl2 | AlCl3 | |
| 熔点(℃) | 2852 | 2045 | 714 | 190(2.5×105Pa) |
| 沸点(℃) | 3600 | 2980 | 1412 | 177.8 |
请参考上述数据回答问题:
(1)工业上常用电解熔融MgCl2的方法生产金属镁;用电解Al2O3与冰晶石熔融混合物的方法生产铝。不用电解MgO的方法生产镁的原因是:
(2)请设计可靠的实验证明MgCl2、AlCl3所属化合物的类型,其实验方法是
(3)AlCl3具有以下
①液化 ②挥发 ③升华
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】以惰性电极分别电解熔融氯化钠和氯化钠溶液时,电极反应有何差异_______ ?写出有关电极反应和总反应方程式_______ 。
您最近一年使用:0次
【推荐3】铝和氢氧化钠都是重要的工业产品。请回答:
(1)工业冶炼铝的化学方程式是___________________________________________ 。
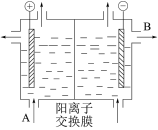
(2)可用阳离子交换膜法电解饱和食盐水制NaOH,其工作原理如左下图所示。

①请写出A、B两处物质的名称或化学式:A___________________ 、B____________________
②请写出电解食盐水的离子方程式__________________________________________
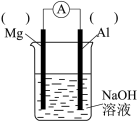
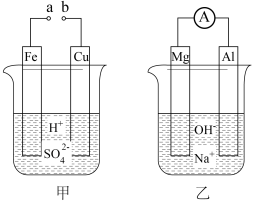
(3)以镁条、铝片为电极,以NaOH溶液为电解质溶液设计的原电池如上中图。
①负极材料为________ (填Mg或Al)。
②该原电池的总反应式为____________________________________________
(4)铝—空气燃料电池可用于电动汽车,通常以NaOH溶液为电解液,铝合金为负极,通入空气的极为正极(如右上图),则
负极的电极反应式为__________________________________ ;
正极的电极反应式为___________________________________ 。
(1)工业冶炼铝的化学方程式是
(2)可用阳离子交换膜法电解饱和食盐水制NaOH,其工作原理如左下图所示。



①请写出A、B两处物质的名称或化学式:A
②请写出电解食盐水的离子方程式
(3)以镁条、铝片为电极,以NaOH溶液为电解质溶液设计的原电池如上中图。
①负极材料为
②该原电池的总反应式为
(4)铝—空气燃料电池可用于电动汽车,通常以NaOH溶液为电解液,铝合金为负极,通入空气的极为正极(如右上图),则
负极的电极反应式为
正极的电极反应式为
您最近一年使用:0次

 移向
移向

