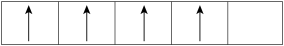
在d轨道中电子排布成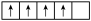 ,而不排布成
,而不排布成 ,其直接的依据是( )
,其直接的依据是( )
 ,而不排布成
,而不排布成 ,其直接的依据是( )
,其直接的依据是( )| A.能量最低原理 | B.泡利原理 | C.原子轨道能级图 | D.洪特规则 |
更新时间:2020-06-23 16:13:32
|
相似题推荐
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】一种合金钢主要是铬和镍。这两种元素在元素周期表中位于
| A.s区 | B.p区 | C.d区 | D.ds区 |
您最近一年使用:0次
单选题
|
容易
(0.94)
解题方法
【推荐2】基态铬(原子序数24)原子的电子排布式是
| A.1s22s22p63s23p64s14p5 | B.1s22s22p63s23p63d6 |
| C.1s22s22p63s23p64s13d4 | D.1s22s22p63s23p63d54s1 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐1】下列对电子排布式或轨道表示式书写的评价错误的是
| 选项 | 电子排布式或轨道表示式 | 评价 |
| A | Br-的电子排布式:[Ar]3dl0 4s2 4p6 | 错误;违反能量最低原理 |
| B | O原子的轨道表示式: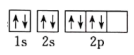 | 错误;违反洪特规则 |
| C | K原子的电子排布式:1s22s2 2p6 3s323p6 3d1 | 错误;违反能量最低原理 |
| D | F原子的轨道表示式: | 错误;违反泡利不相容原理 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】下列对电子排布式或轨道表示式书写的评价错误的是
| A.若Mn元素的基态原子核外电子排布式为1s22s22p63s23p63d7 ,则违反了构造原理 |
B.若基态硫原子的价层电子轨道表示式为 ,则违反了泡利原理 ,则违反了泡利原理 |
C.基态氮原子的核外电子轨道表示式为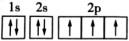 ,符合洪特规则和泡利原理 ,符合洪特规则和泡利原理 |
D.电子排布式(   )违反了洪特规则 )违反了洪特规则 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】若将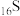 原子的电子排布式写成
原子的电子排布式写成 ,则违背了
,则违背了
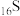 原子的电子排布式写成
原子的电子排布式写成 ,则违背了
,则违背了| A.能量守恒原理 | B.泡利不相容原理 | C.能量最低原理 | D.洪特规则 |
您最近一年使用:0次
单选题
|
容易
(0.94)
解题方法
【推荐2】以下列出的是一些基态原子的2p轨道和3d轨道中电子排布的情况,违反洪特规则的有
①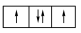 ②
②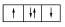 ③
③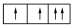 ④
④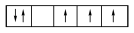 ⑤
⑤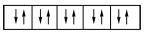 ⑥
⑥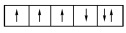
| A.①②③ | B.④⑤⑥ | C.②④⑥ | D.③④⑥ |
您最近一年使用:0次