世界上最早发现并使用锌的是中国,明朝末年《天工开物》一书中有世界上最早的关于炼锌技术的记载。回答下列问题:
(1)基态Zn原子的核外电子所占据的最高能层符号为___ 。
(2)硫酸锌溶于过量的氨水可形成[Zn(NH3)4]SO4溶液。
①[Zn(NH3)4]SO4中阴离子的空间构型为_______ 。
② 中,中心原子的轨道杂化类型为
中,中心原子的轨道杂化类型为________ 。
③写出一种与 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:________ 。
④NH3极易溶于水,除因为它们都是极性分子外,还因为________
(1)基态Zn原子的核外电子所占据的最高能层符号为
(2)硫酸锌溶于过量的氨水可形成[Zn(NH3)4]SO4溶液。
①[Zn(NH3)4]SO4中阴离子的空间构型为
②
 中,中心原子的轨道杂化类型为
中,中心原子的轨道杂化类型为③写出一种与
 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:④NH3极易溶于水,除因为它们都是极性分子外,还因为
19-20高二下·贵州铜仁·期中 查看更多[2]
更新时间:2020-06-24 00:30:19
|
相似题推荐
【推荐1】Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧的黄光是一种______ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是______ (填序号)。
a.1s22s22p43s13p 3p
3p 3p
3p b.1s22s22p33s23p
b.1s22s22p33s23p 3p
3p 3p
3p
c.1s22s22p63s13p d.1s22s22p63s2
d.1s22s22p63s2
(3)Ti原子位于元素周期表中的______ 区,其价电子排布式为_____ 。与Ti同周期的过渡元素中,未成对电子数最多的基态原子的外围电子的轨道表示式______ 。
(4)Fe3+与Fe2+的离子半径大小关系为Fe3+______ Fe2+(填“大于”或“小于”)。
(5)下列各组多电子原子的能级能量比较不正确的是______ 。
①2p=3p ②4s>2s ③4p>4f ④ 4d>3d
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.1s22s22p43s13p
 3p
3p 3p
3p b.1s22s22p33s23p
b.1s22s22p33s23p 3p
3p 3p
3p
c.1s22s22p63s13p
 d.1s22s22p63s2
d.1s22s22p63s2(3)Ti原子位于元素周期表中的
(4)Fe3+与Fe2+的离子半径大小关系为Fe3+
(5)下列各组多电子原子的能级能量比较不正确的是
①2p=3p ②4s>2s ③4p>4f ④ 4d>3d
| A.①④ | B.①③ | C.③④ | D.②③ |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】立方砷化硼具有高载流子迁移率,超越硅的导热、导电性能,有望成为硅基元器件的替代方案,其晶胞结构如图所示,请回答下列问题:
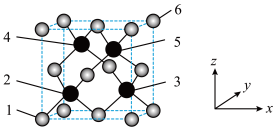
(1)As在元素周期表中的位置是_______ 。As属于_______ 区元素。
(2)该晶胞的化学式为_______ 。2、3、4、5四个原子所围成的空间结构为_______ 形。
(3)晶胞有两个基本要素。
①原子坐标参数,表示晶胞内部各原子的相对位置,图中1号原子的坐标参数为 ,6号原子的坐标参数为
,6号原子的坐标参数为 ,则2号原子的坐标参数为
,则2号原子的坐标参数为_______ 。
②晶胞参数是用来描述晶胞大小和形状的,设该晶胞的晶胞参数为a pm,阿伏加德罗常数为 ,则B、As原子之间的最短距离为
,则B、As原子之间的最短距离为_______ pm,该晶胞的密度为_______  。
。

(1)As在元素周期表中的位置是
(2)该晶胞的化学式为
(3)晶胞有两个基本要素。
①原子坐标参数,表示晶胞内部各原子的相对位置,图中1号原子的坐标参数为
 ,6号原子的坐标参数为
,6号原子的坐标参数为 ,则2号原子的坐标参数为
,则2号原子的坐标参数为②晶胞参数是用来描述晶胞大小和形状的,设该晶胞的晶胞参数为a pm,阿伏加德罗常数为
 ,则B、As原子之间的最短距离为
,则B、As原子之间的最短距离为 。
。
您最近一年使用:0次
【推荐3】已知元素 是组成物质
是组成物质 的其中一种元素。元素
的其中一种元素。元素 的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号
的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号 至
至 表示)如表所示:
表示)如表所示:
(1)元素 是
是___________ (填元素符号)。
(2)基态氮原子核外有___________ 种不同运动状态的电子,有___________ 种能量不同的电子。
(3) 中,电负性最大的元素是
中,电负性最大的元素是___________ (填元素符号), 的
的___________ 杂化轨道与 的
的 轨道形成
轨道形成___________ 键。
 是组成物质
是组成物质 的其中一种元素。元素
的其中一种元素。元素 的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号
的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号 至
至 表示)如表所示:
表示)如表所示: |  |  |  | |
电离能 | 578 | 1817 | 2745 | 11578 |
 是
是(2)基态氮原子核外有
(3)
 中,电负性最大的元素是
中,电负性最大的元素是 的
的 的
的 轨道形成
轨道形成
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】请回答下列问题:
(1) 中含有化学键的类型为
中含有化学键的类型为_______ 。
(2) 由
由 和
和 构成,
构成, 的空间结构是
的空间结构是_______ ,根据化合物 判断,
判断, 、B、H的电负性由大到小的顺序为
、B、H的电负性由大到小的顺序为_______ 。
(1)
 中含有化学键的类型为
中含有化学键的类型为(2)
 由
由 和
和 构成,
构成, 的空间结构是
的空间结构是 判断,
判断, 、B、H的电负性由大到小的顺序为
、B、H的电负性由大到小的顺序为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】回答下列问题:
(1)氨气通入盐酸中发生反应: 。
。
①NH3分子的VSEPR模型名称为_______ ,略去N原子上的_______ 个孤电子对,使得NH3分子的空间结构名称为_______ 。转化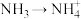 中,氮原子的杂化类型是否改变?
中,氮原子的杂化类型是否改变?_______ (填“改变”或“未变”)。
②转化H3O+→H2O涉及的两种微粒中,H2O、H3O+的空间结构名称分别为_______ 、_______ ,中心原子的杂化类型分别为_______ 、_______ 。
(2)分子的结构往往决定了物质的有关性质,特别是物质的溶解性、熔沸点等物理性质。
①基团间的相互影响可决定物质的结构与性质,如乙烷为_______ 分子(填“极性”或“非极性”,下同),而乙烷中一个氢原子被羟基(—OH)取代后所得的乙醇分子为_______ 分子,这决定了乙烷_______ 溶于水,而乙醇_______ 溶于水。
②氧、硫、硒(Se)元素同为第VIA族元素,三者的简单氢化物结构相似,但H2S的沸点低于H2O,原因是_______ ,H2S的沸点低于H2Se的原因是_______ 。
(1)氨气通入盐酸中发生反应:
 。
。①NH3分子的VSEPR模型名称为
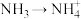 中,氮原子的杂化类型是否改变?
中,氮原子的杂化类型是否改变?②转化H3O+→H2O涉及的两种微粒中,H2O、H3O+的空间结构名称分别为
(2)分子的结构往往决定了物质的有关性质,特别是物质的溶解性、熔沸点等物理性质。
①基团间的相互影响可决定物质的结构与性质,如乙烷为
②氧、硫、硒(Se)元素同为第VIA族元素,三者的简单氢化物结构相似,但H2S的沸点低于H2O,原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】铁、铝、铜、硫、氮、磷、砷都是日常生活中常见的元素,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途。请回答以下问题:
(1)Cu+的基态价电子排布图_______ ;Cu(NH3)4SO4中N、S、O三种元素的第一电离能由大到小的顺序为_______ (元素符号表示)。
(2)SO 中心原子的杂化方式为
中心原子的杂化方式为_______ ,SO 的立体构型为
的立体构型为_______ 。
(3)某种磁性氮化铁的晶胞结构如图所示,该化合物的化学式为_______ 。
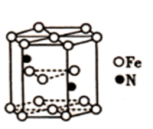
(1)Cu+的基态价电子排布图
(2)SO
 中心原子的杂化方式为
中心原子的杂化方式为 的立体构型为
的立体构型为(3)某种磁性氮化铁的晶胞结构如图所示,该化合物的化学式为

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】解释乙烯分子中π键是如何形成的?预测乙炔分子中π键是如何形成的?_______
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】C、O、S、 、
、 、
、 等元素的单质及化合物在诸多领域都有广泛应用。回答下列问题:
等元素的单质及化合物在诸多领域都有广泛应用。回答下列问题:
(1) 元素在元素周期表的位置是
元素在元素周期表的位置是_______ ,基态 原子能量最高的电子占据的原子轨道的形状是
原子能量最高的电子占据的原子轨道的形状是_______ ,基态 原子的简化电子排布式为
原子的简化电子排布式为_______ 。
(2)基态S原子的价层电子轨道表示式为_______ , 属于
属于_______ 分子(填“极性”或“非极性”)。
(3) 的键角
的键角_______  的键角(填“>”、“<”或“=”),理由是
的键角(填“>”、“<”或“=”),理由是_______
(4)琥珀酸亚铁片是预防和治疗缺铁性贫血的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是_______ 。 比
比 的离子半径小,原因是
的离子半径小,原因是_______ 。
 、
、 、
、 等元素的单质及化合物在诸多领域都有广泛应用。回答下列问题:
等元素的单质及化合物在诸多领域都有广泛应用。回答下列问题:(1)
 元素在元素周期表的位置是
元素在元素周期表的位置是 原子能量最高的电子占据的原子轨道的形状是
原子能量最高的电子占据的原子轨道的形状是 原子的简化电子排布式为
原子的简化电子排布式为(2)基态S原子的价层电子轨道表示式为
 属于
属于(3)
 的键角
的键角 的键角(填“>”、“<”或“=”),理由是
的键角(填“>”、“<”或“=”),理由是(4)琥珀酸亚铁片是预防和治疗缺铁性贫血的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成
 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是 比
比 的离子半径小,原因是
的离子半径小,原因是
您最近一年使用:0次



