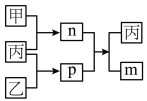
在如图所示的转化关系中(反应条件略去),常温下X为气体,a、b、c是中学化学中常见物质,均由常见元素组成。下列说法正确的是( )


A.若X为 ,a为一种固态单质,则c可能为 ,a为一种固态单质,则c可能为 或 或 |
| B.若a、b、c的焰色反应均呈黄色,水溶液均呈碱性,则a中可能含有非极性共价键 |
| C.若b为固态非金属单质,b与X所含元素同主族,则c与X不能反应 |
| D.若b为气态非金属单质,X与b所含元素同周期,则a与c在一定条件下可以反应生成b |
更新时间:2020-05-09 15:55:29
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】现有易溶强电解质的混合溶液10L,溶液中可能含K+、Ba2+、Na+、NH 、Cl-、SO
、Cl-、SO 、AlO
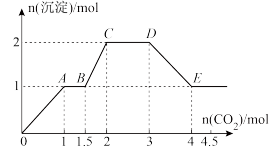
、AlO 、OH-中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如图所示,下列说法正确的是( )
、OH-中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如图所示,下列说法正确的是( )
 、Cl-、SO
、Cl-、SO 、AlO
、AlO 、OH-中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如图所示,下列说法正确的是( )
、OH-中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如图所示,下列说法正确的是( )
A.该溶液中能确定存在的离子是Ba2+、Na+、Cl-、NH |
| B.肯定不存在的离子是Cl-、OH- |
| C.若不能确定的离子中至少还存在一种阳离子,则该离子的最小浓度为0.2mol/L |
D.OA段反应的离子方程式:2AlO +CO2+3H2O═2Al(OH)3↓+CO +CO2+3H2O═2Al(OH)3↓+CO |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】有一包白色粉末,可能由BaCl2、Na2SO4、K2CO3、KOH、AgNO3和无水硫酸铜中的一种或几种组成。为了探究它的组成,进行了如下实验:
①将白色粉末加入足量水中充分溶解,过滤得到滤渣A和溶液B;
②在滤渣A中加入足量稀盐酸,A全部溶解并产生气体C;
③将气体C通入溶液B中产生沉淀D。
下列判断不正确的是
①将白色粉末加入足量水中充分溶解,过滤得到滤渣A和溶液B;
②在滤渣A中加入足量稀盐酸,A全部溶解并产生气体C;
③将气体C通入溶液B中产生沉淀D。
下列判断不正确的是
| A.滤渣A和沉淀D的成分相同 |
| B.白色粉末中一定有KOH |
| C.取少量溶液B,加入足量稀盐酸,有气泡产生 |
| D.③中若继续通入过量气体C,最终无固体剩余 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】某研究小组为了探究固体甲(二元化合物)和固体乙(无机矿物盐,含五种元素)的组成和性质,设计并完成了如下实验:
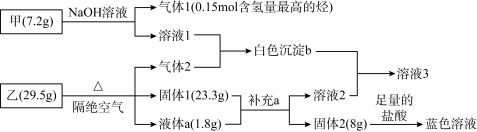
已知:向溶液1中连续滴加盐酸,先产生白色沉淀,后沉淀溶解;向溶液2中连续通入气体2,也是先产生白色沉淀,后沉淀溶解。请回答下列问题:
(1)甲的化学式为_______ ,气体1的电子式为_______ 。
(2)加热条件下,气体1与固体2反应,可产生三种产物,其中一种为常温下的液体,该反应的化学方程式为_______ 。
(3)乙的化学式为_______ 。
(4)足量气体2与溶液1反应的离子方程式为_______ 。有人认为,判断该反应的气体2是否过量较难,应对其中一种产物是“正盐”还是“酸式盐”进行检验,请设计实验证明这一产物的成分:_______ 。(可选的试剂为氨水、NaOH溶液、稀硫酸、 溶液)
溶液)

已知:向溶液1中连续滴加盐酸,先产生白色沉淀,后沉淀溶解;向溶液2中连续通入气体2,也是先产生白色沉淀,后沉淀溶解。请回答下列问题:
(1)甲的化学式为
(2)加热条件下,气体1与固体2反应,可产生三种产物,其中一种为常温下的液体,该反应的化学方程式为
(3)乙的化学式为
(4)足量气体2与溶液1反应的离子方程式为
 溶液)
溶液)
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列指定反应的离子方程式正确的是
A.足量的CO2通入饱和碳酸钠溶液中:CO2+CO +H2O=2HCO +H2O=2HCO |
| B.200mL1mol·L-1溴化亚铁溶液中通入4.48LCl2(标准状况下):Fe2++2Br-+2Cl2=Fe3++Br2+4Cl- |
| C.Ca(ClO)2溶液中通入SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
D.NaAlO2溶液和过量NaHSO4溶液混合:AlO +4H+=Al3++2H2O +4H+=Al3++2H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】我国杰出化学家侯德榜根据NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl都小的性质,运用CO2+NH3+H2O+NaCl=NaHCO3↓+NH4Cl的反应原理制备纯碱。下面是在实验室进行模拟实验的生产流程示意图:

则下列叙述不正确的是

则下列叙述不正确的是
| A.A气体是CO2,B气体是NH3 |
| B.第Ⅲ步得到的晶体是发酵粉的主要成分 |
| C.第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒 |
D.第Ⅳ步操作发生的化学反应方程式为:2NaHCO3 Na2CO3+CO2↑+H2O Na2CO3+CO2↑+H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】A、B、C、D为短周期主族元素,25℃时,其最高价氧化物的水化物溶液(浓度均为0.1mol·L-1) 的pH和原子序数的关系如图所示。下列有关说法正确的是

| A.简单离子半径:D离子>C离子>A离子>B离子 |
| B.D元素氧化物的水化物一定是强酸 |
| C.B、C的简单离子都能破坏水的电离平衡 |
| D.氢化物还原性:C >D |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】某阴离子由原子序数依次增大的同周期元素 、
、 、
、 、
、 组成,其结构如图,
组成,其结构如图, 的最外层电子数等于
的最外层电子数等于 的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是
的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是
 、
、 、
、 、
、 组成,其结构如图,
组成,其结构如图, 的最外层电子数等于
的最外层电子数等于 的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是
的核外电子总数,四种原子最外层电子数之和为20,下列说法正确的是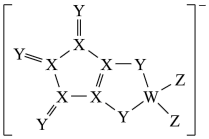
A.最高价含氧酸酸性: |
B. 、 、 的简单氢化物中 的简单氢化物中 的沸点高 的沸点高 |
C.原子半径: |
D.仅由 与 与 形成的化合物中可能含有非极性键 形成的化合物中可能含有非极性键 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】短周期元素X、Y、Z、W、Q的原子序数依次增大,且只有一种金属元素。其中X与W处于同一主族,Z元素原子半径在短周期中最大(稀有气体除外)。Z与W、W与Q的原子序数之差均为3,五种元素原子的最外层电子数之和为21,下列说法正确的是
| A.X和Y的常见氧化物都是大气污染物 |
| B.自然界中的W的储量丰富,高纯度的W的氧化物是将太阳能转化为电能的材料 |
| C.一定条件下,Q单质可把Y从其氢化物中置换出来 |
| D.最高价氧化物对应水化物的酸性顺序:Q>Y>W>X |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】X、Y、Z、W是原子序数依次增大的四种短周期元素,A、B、C、D、F都是由其中的两种或三种元素组成的化合物,E是由Z元素形成的单质,0.1mol·L-1D溶液的pH为13(25℃)。它们满足如图转化关系,则下列说法不正确的是
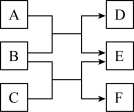

| A.B晶体中阴、阳离子个数比为1:2 |
| B.等体积等浓度的F溶液与D溶液中,阴离子总的物质的量F>D |
| C.0.1molB与足量A或C完全反应转移电子数均为0.1NA |
| D.Y、Z分别形成的简单氢化物的稳定性前者弱于后者,是因为后者分子间存在氢键 |
您最近一年使用:0次