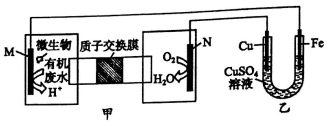
下列图示内容的对应说明正确的是
| 编号 | A | B | C | D |
| 图示 | 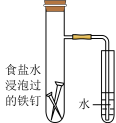 食盐水 |  片刻后在Fe 电极附近滴入K3[Fe(CN)6]溶液 | 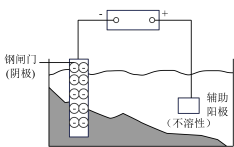 |  |
| 说明 | 验证铁钉发生 吸氧腐蚀 | 验证 Fe 电极被保护 | 该装置是牺牲阳极的阴极保护法 | 该化学反应为放热反应 |
| A.A | B.B | C.C | D.D |
19-20高二下·北京海淀·期末 查看更多[4]
北京市八一学校2019-2020学年高二下学期期末考试化学试题模拟卷03(必考+选考)——2020年秋高三化学开学摸底考试卷(全国通用)(已下线)专题12 化学反应与电能-2023年高考化学一轮复习小题多维练(全国通用)(已下线)专题12 化学反应与电能-2023年高考化学一轮复习小题多维练(全国通用)
更新时间:2020-07-04 17:17:40
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】下列有关如图所示的说法正确的是
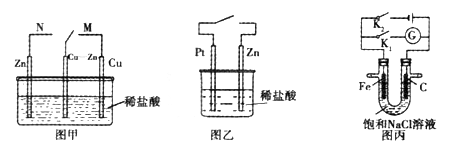

| A.图甲中开关置于N处时铜锌合金腐蚀的速率增大 |
| B.图乙中接通开关时,锌腐蚀的速率增大,锌上放出气体的速率增大 |
| C.图丙中接通K2时铁棒不被腐蚀,属于牺牲阳极保护法 |
| D.图丙中接通K1时,石墨棒周围溶液的pH增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】有关下列说法中,正确的是
| A.用标准盐酸滴定未知浓度的NaOH溶液,滴定前酸式滴定管尖嘴有气泡未排出,滴定后气泡消失,会造成测定结果偏低 |
| B.工业废水中的Cu2+、Hg2+等重金属阳离子可以通过加入FeS除去 |
| C.工业上常在铁板表面镀上一层锡(俗称马口铁)来防止铁板表面破损后发生电化学腐蚀 |
| D.等体积的pH均为2的酸HA和HB的溶液分别与足量的铁粉反应,HA放出的H2多,说明HA酸性强 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】钾离子电池资源丰富,在非水基电解液中具有更高的离子导电率等优点。一种钾离子电池的工作原理如图所示,已知该电池负极在KC24-KC16-KC8之间变化,正极在K2MnFe(CN)6-KMnFe(CN)6-MnFe(CN)6之间变化,下列说法不正确的是( )
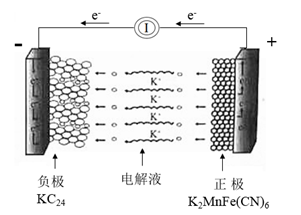

| A.如图所示为钾离子电池的放电过程 |
| B.放电时负极可发生反应:2KC8-e-=KC16+K+ |
| C.充电时正极反应式为K2MnFe(CN)6-e-=KMnFe(CN)6+K+ |
| D.若充电前正负极质量相同,则充电时每转移0.lmole-,理论上正负极质量差将增加7.8g |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】高能LiFePO4电池,多应用于公共交通。电池中间是聚合物的隔膜,主要作用是在反应过程中只让Li+通过。结构如图所示。
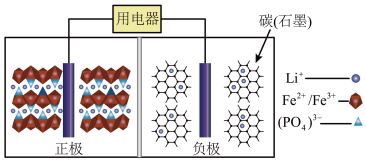
原理如下:(1-x)LiFePO4+xFePO4+LixCn LiFePO4+nC。
LiFePO4+nC。
下列说法不正确 的是

原理如下:(1-x)LiFePO4+xFePO4+LixCn
 LiFePO4+nC。
LiFePO4+nC。下列说法
| A.放电时,正极电极反应式:xFePO4+xLi++xe-=xLiFePO4 |
| B.放电时,电子由负极经导线、用电器、导线到正极 |
| C.充电时,阴极电极反应式:xLi++xe-+nC=LixCn |
| D.充电时,当导线中传递l mol电子,理论上将有1 mol Li+向左移动 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】将 NaCl 溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿棕色铁锈环(b),如图所示。下列说法不正确 的是( )
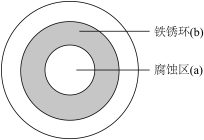

| A.铁片腐蚀过程发生的总化学方程式为:4Fe+6H2O+3O2 ==4 Fe(OH)3 |
| B.液滴之下氧气含量少, 铁片作负极,发生的还原反应为: Fe-2e-=Fe2+ |
| C.液滴边缘是正极区,发生的电极反应为: O2+2H2O+4e-=4OH- |
| D.铁片腐蚀最严重区域不是生锈最多的区域 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下列有关化学反应原理的说法中,不正确的说法组合是
①有效碰撞一定能导致化学反应的发生
②难溶物的溶解度和 Ksp 的大小都仅仅只受温度的影响
③某反应正方向能自发进行,则逆方向一定难以自发进行
④某溶液的 pH 不受温度的影响,那么该溶液一定显强酸性
⑤用盐酸滴定氨水,若选择酚酞做指示剂,则测定的结果会偏小
⑥中和热的测定实验,若量取 NaOH 溶液的量筒仰视读数,则所测的△H 偏大
⑦金属的吸氧腐蚀比析氢腐蚀更普遍,但吸氧腐蚀的速率不如金属的析氢腐蚀
①有效碰撞一定能导致化学反应的发生
②难溶物的溶解度和 Ksp 的大小都仅仅只受温度的影响
③某反应正方向能自发进行,则逆方向一定难以自发进行
④某溶液的 pH 不受温度的影响,那么该溶液一定显强酸性
⑤用盐酸滴定氨水,若选择酚酞做指示剂,则测定的结果会偏小
⑥中和热的测定实验,若量取 NaOH 溶液的量筒仰视读数,则所测的△H 偏大
⑦金属的吸氧腐蚀比析氢腐蚀更普遍,但吸氧腐蚀的速率不如金属的析氢腐蚀
| A.②③ | B.①③⑥ | C.①③④ | D.②③⑥ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】防止金属锈蚀的方法有多种,如图表示保护铁管的方法为


| A.牺牲阳极的阴极保护法 | B.改变金属的组成和结构法 |
| C.外加电流的阴极保护法 | D.表面覆盖保护层法 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】含可钝化金属的工业管道或反应器,由于会被内部溶液腐蚀,通过外接电源而钝化,称之为阳极保护法。下图是某金属外接电势与电流密度的变化关系,有关说法正确的是
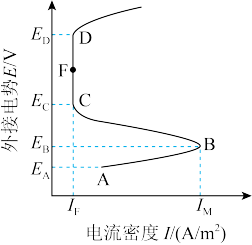

| A.阳极保护法中受保护的金属外接电源的负极 |
| B.电流密度越大,金属受保护程度越好 |
| C.CFD区,金属受到保护 |
| D.外接电势越高,对金属保护性越有效 |
您最近一年使用:0次