以铜为原料制取氢氧化铜,设计必要步骤并写出相应的化学方程式_____ 。
19-20高一·全国·假期作业 查看更多[1]
(已下线)衔接点02 酸碱盐的分类和命名-2020年【衔接教材·暑假作业】初高中衔接化学
更新时间:2020-07-06 21:39:00
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】2022年央视春晚的节目《只此青绿》,提到了颜料石绿{铜绿,又名孔雀石,主要成分是碱式碳酸铜[Cu2(OH)2CO3]}。某同学利用下述反应实现了“铜→铜绿→……→Cu”的转化。回答下列问题:
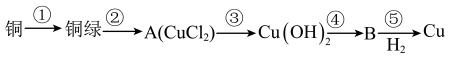
(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:___________ 。
(2)将绿豆大小的金属钠投入盛有A溶液的烧杯中,溶液中出现蓝色絮状沉淀,振荡摇匀即为悬浊液,悬浊液与溶液的本质区别是___________ 。若投入的钠块比较大,可能会出现黑色固体,其成分是___________ 。
(3)A、B在无色火焰上灼烧时,其焰色为________ 色,该原理是_______ (填“物理”或“化学”)变化。
(4)完成步骤②和③可选用的试剂分别为___________ 、___________ 。(填标号)
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d.KNO3溶液
写出CuCl2在水溶液中的电离方程式:___________ 。

(1)铜在潮湿的空气中容易产生铜绿,写出此反应的化学方程式:
(2)将绿豆大小的金属钠投入盛有A溶液的烧杯中,溶液中出现蓝色絮状沉淀,振荡摇匀即为悬浊液,悬浊液与溶液的本质区别是
(3)A、B在无色火焰上灼烧时,其焰色为
(4)完成步骤②和③可选用的试剂分别为
a.HCl溶液 b.NaCl溶液 c.NaOH溶液 d.KNO3溶液
写出CuCl2在水溶液中的电离方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】下列说法正确的是________ 。
①铜绿的主要成分是碱式碳酸铜,可用稀盐酸除铜器表面的铜绿
②除去Cu粉中混有CuO的方法是加入稀硝酸溶解、过滤、洗涤、干燥
③将铜粉加入1−0mol·L-1Fe2(SO4)3溶液中,现象是溶液变蓝,有黑色固体出现
④铁比铜活泼,铆在铜板上的铁钉在潮湿空气中不易生锈
⑤氧化铜可作为制造玻璃、搪瓷的红色颜料
⑥硫酸铜溶液可用作游泳池的消毒剂
⑦为了避免青铜器生成铜绿,在青铜器的表面覆盖一层防渗的高分子膜
⑧1molCu和足量热浓硫酸反应可生成NA个SO3分子
⑨冶炼铜的反应为8CuFeS2+21O2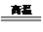 8Cu+4FeO+2Fe2O3+16SO2,若CuFeS2中Fe的化合价为+2,反应中被还原的元素是Cu和O
8Cu+4FeO+2Fe2O3+16SO2,若CuFeS2中Fe的化合价为+2,反应中被还原的元素是Cu和O
⑩CuSO4溶液与过量浓氨水反应的离子方程式:Cu2++2NH3·H2O=Cu(OH)2↓+2NH4+
⑪将CuCl2溶液在蒸发皿中加热蒸干,得到无水CuCl2固体
⑫H2通过灼热的CuO粉末,反应后固体物质增重
①铜绿的主要成分是碱式碳酸铜,可用稀盐酸除铜器表面的铜绿
②除去Cu粉中混有CuO的方法是加入稀硝酸溶解、过滤、洗涤、干燥
③将铜粉加入1−0mol·L-1Fe2(SO4)3溶液中,现象是溶液变蓝,有黑色固体出现
④铁比铜活泼,铆在铜板上的铁钉在潮湿空气中不易生锈
⑤氧化铜可作为制造玻璃、搪瓷的红色颜料
⑥硫酸铜溶液可用作游泳池的消毒剂
⑦为了避免青铜器生成铜绿,在青铜器的表面覆盖一层防渗的高分子膜
⑧1molCu和足量热浓硫酸反应可生成NA个SO3分子
⑨冶炼铜的反应为8CuFeS2+21O2
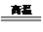 8Cu+4FeO+2Fe2O3+16SO2,若CuFeS2中Fe的化合价为+2,反应中被还原的元素是Cu和O
8Cu+4FeO+2Fe2O3+16SO2,若CuFeS2中Fe的化合价为+2,反应中被还原的元素是Cu和O⑩CuSO4溶液与过量浓氨水反应的离子方程式:Cu2++2NH3·H2O=Cu(OH)2↓+2NH4+
⑪将CuCl2溶液在蒸发皿中加热蒸干,得到无水CuCl2固体
⑫H2通过灼热的CuO粉末,反应后固体物质增重
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】A、B、C、D、E分别是镁片、氯化铜溶液、氢氧化钠溶液、氧化铜粉末、稀盐酸中的一种物质,用两个圆圈相切表示两种物质在常温下能反应,且A与B反应无现象,A与C反应生成D溶液。请回答下列问题:
(1)A、B周围画出C、D、E,并将物质名称标在圆中;______________
(2)写出发生置换反应的化学方程式_______________________________ ;
(3)描述B与D反应的实验现象为____________________ 。
(1)A、B周围画出C、D、E,并将物质名称标在圆中;
(2)写出发生置换反应的化学方程式
(3)描述B与D反应的实验现象为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】纯碱和烧碱都是重要的化工原料,在物质的分类中,纯碱属于_____ 类,烧碱属于_____ 类,纯碱和熟石灰反应可以制得烧碱,写出反应的化学方程式 ______ 从反应后的混合物中分离出烧碱的操作是______ ,从溶液中得到固体的操作是______
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】锡(Sn)是第IVA族元素,其常见的氯化物有SnCl4和SnCl2.SnCl4常温下为液体,遇水极易发生水解反应;SnCl2常温下为固体,具有还原性,可被空气中的氧气氧化。某化学实验小组制备SnCl4的装置如图(加热与夹持装置省略)。

回答下列问题:
(1)仪器a的名称是_______ ;装置B中盛放的试剂是_______ 。
(2)制取SnCl4的操作步骤为:①连接好装置;②_______ ;③添加药品、滴加浓盐酸;④待装置D_______ 后,加热装置C;⑤收集SnCl4。请补充上述实验步骤。

回答下列问题:
(1)仪器a的名称是
(2)制取SnCl4的操作步骤为:①连接好装置;②
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)写出磷酸主要的电离方程式:____ 。
(2)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式。
________ 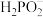 +
+________ Ag++________ __ =________ PO +
+________ Ag+________ ___
(3)由工业白磷(含少量砷、铁、镁等)制备高纯白磷(熔点44℃,沸点280℃),主要生产流程如图:

①除砷过程在75℃时进行,其合理的原因是__ (填字母)。
a.使白磷熔化,提高反应活性
b.降低白磷的毒性
c.温度不宜过高,防止硝酸分解
d.适当提高温度,增大反应速率
②生产过程在高纯氮气保护下进行,其目的是__ 。
(1)写出磷酸主要的电离方程式:
(2)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式。
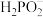 +
+ +
+(3)由工业白磷(含少量砷、铁、镁等)制备高纯白磷(熔点44℃,沸点280℃),主要生产流程如图:

①除砷过程在75℃时进行,其合理的原因是
a.使白磷熔化,提高反应活性
b.降低白磷的毒性
c.温度不宜过高,防止硝酸分解
d.适当提高温度,增大反应速率
②生产过程在高纯氮气保护下进行,其目的是
您最近一年使用:0次




