磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)写出磷酸主要的电离方程式:____ 。
(2)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式。
________ 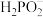 +
+________ Ag++________ __ =________ PO +
+________ Ag+________ ___
(3)由工业白磷(含少量砷、铁、镁等)制备高纯白磷(熔点44℃,沸点280℃),主要生产流程如图:

①除砷过程在75℃时进行,其合理的原因是__ (填字母)。
a.使白磷熔化,提高反应活性
b.降低白磷的毒性
c.温度不宜过高,防止硝酸分解
d.适当提高温度,增大反应速率
②生产过程在高纯氮气保护下进行,其目的是__ 。
(1)写出磷酸主要的电离方程式:
(2)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式。
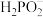 +
+ +
+(3)由工业白磷(含少量砷、铁、镁等)制备高纯白磷(熔点44℃,沸点280℃),主要生产流程如图:

①除砷过程在75℃时进行,其合理的原因是
a.使白磷熔化,提高反应活性
b.降低白磷的毒性
c.温度不宜过高,防止硝酸分解
d.适当提高温度,增大反应速率
②生产过程在高纯氮气保护下进行,其目的是
更新时间:2020-11-10 17:14:12
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】在常温常压下,有以下10种物质,请回答下列问题:
①干冰;②熔融氧化钠;③蔗糖;④稀硫酸;⑤NaHSO4溶液;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧铜
(1)其中能导电的是___________ (填写序号,下同);属于电解质的是___________ ;属于非电解质的是___________ 。
(2)写出物质⑦的电离方程式:___________ 。
(3)写出物质④和⑦反应的离子方程式:___________ 。
(4)写出物质④和⑥在水中发生反应的离子方程式:________ 。
①干冰;②熔融氧化钠;③蔗糖;④稀硫酸;⑤NaHSO4溶液;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧铜
(1)其中能导电的是
(2)写出物质⑦的电离方程式:
(3)写出物质④和⑦反应的离子方程式:
(4)写出物质④和⑥在水中发生反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】过氧化氢的水溶液适用于医用消毒、环境消毒和食品消毒。
Ⅰ.过氧化氢性质探究实验
(1)酸性条件下H2O2可将Fe2+转化成Fe3+,由此说明H2O2具有______ 性。
(2)已知H2O2是一种二元弱酸,其中Ka1=2.20×10-12、Ka2=1.05×10-25,则H2O2的电离方程式为______ ,常温下,1mol∙L-1的H2O2溶液的pH约为______ 。
Ⅱ.过氧化氢含量的测定实验。某兴趣小组同学用0.1000mol∙L-1的酸性高锰酸钾标准溶液滴定试样中的过氧化氢,反应原理为2 +5H2O2+6H+=2Mn2++8H2O+5O2↑。
+5H2O2+6H+=2Mn2++8H2O+5O2↑。
(3)滴定达到终点的现象是______ 。
(4)用移液管移取25.00mL试样置于锥形瓶中,重复滴定四次,每次消耗酸性高锰酸钾标准溶液的体积如表所示:
计算试样中过氧化氢的浓度为______ mol∙L-1。
(5)若滴定前滴定管尖嘴处有气泡,滴定后消失,则测定结果______ (填“偏高”“偏低”或“不变”)。
Ⅰ.过氧化氢性质探究实验
(1)酸性条件下H2O2可将Fe2+转化成Fe3+,由此说明H2O2具有
(2)已知H2O2是一种二元弱酸,其中Ka1=2.20×10-12、Ka2=1.05×10-25,则H2O2的电离方程式为
Ⅱ.过氧化氢含量的测定实验。某兴趣小组同学用0.1000mol∙L-1的酸性高锰酸钾标准溶液滴定试样中的过氧化氢,反应原理为2
 +5H2O2+6H+=2Mn2++8H2O+5O2↑。
+5H2O2+6H+=2Mn2++8H2O+5O2↑。(3)滴定达到终点的现象是
(4)用移液管移取25.00mL试样置于锥形瓶中,重复滴定四次,每次消耗酸性高锰酸钾标准溶液的体积如表所示:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| V(KMnO4溶液)/mL | 17.10 | 18.10 | 18.00 | 17.90 |
(5)若滴定前滴定管尖嘴处有气泡,滴定后消失,则测定结果
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】按要求完成下列填空:
(1)碳酸钡在水中的电离方程式:___________ 。
(2)硫酸氢钠在熔融状态的电离方程式:___________ 。
(3)盐酸和小苏打反应的离子方程式:___________ 。
(4)向澄清石灰水中通入过量CO2反应的离子方程式:___________ 。
(5)铜绿Cu2(OH)2CO3溶于硫酸溶液的离子方程式:___________ 。
(6)配平方程式:___________ 。
_______K2CrO4+______HCl(浓)=_______KCl+______CrCl3+_______Cl2↑+________
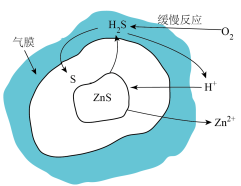
(7)锌矿(主要成分ZnS),浸出过程原理如图所示,ZnS浸出总反应的离子方程式为_______ 。
(1)碳酸钡在水中的电离方程式:
(2)硫酸氢钠在熔融状态的电离方程式:
(3)盐酸和小苏打反应的离子方程式:
(4)向澄清石灰水中通入过量CO2反应的离子方程式:
(5)铜绿Cu2(OH)2CO3溶于硫酸溶液的离子方程式:
(6)配平方程式:
_______K2CrO4+______HCl(浓)=_______KCl+______CrCl3+_______Cl2↑+________
(7)锌矿(主要成分ZnS),浸出过程原理如图所示,ZnS浸出总反应的离子方程式为

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】下图是元素周期表的一部分,用化学用语回答下列问题:

(1)元素Fe在周期表中的位置为________ 。
(2)⑦与⑧形成的化合物中各原子均满足8电子稳定结构的是_____ 。(用化学式表示)
(3)④、⑦、⑧三种元素的非金属性由强到弱的顺序是________ 。(用元素符号表示)
(4)用电子式表示含元素⑥的10电子二元化合物的形成过程________ 。
(5)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为_________ 。

(1)元素Fe在周期表中的位置为
(2)⑦与⑧形成的化合物中各原子均满足8电子稳定结构的是
(3)④、⑦、⑧三种元素的非金属性由强到弱的顺序是
(4)用电子式表示含元素⑥的10电子二元化合物的形成过程
(5)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】回答下列问题:
(1)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是____ ,又变为棕黄色的原因是____ (用离子方程式解释)。
(2)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。写出SO2吸收Br2反应的化学方程式为____ 。
(3)氮氧化物的治理是当前生态环境保护中的重要课题之一。从原理上看,NH3可用于治理NO2,该反应在催化剂条件下可实现,写出化学方程式____ 。
(4)一种新型催化剂能使NO和CO发生反应2NO+2CO 2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
①上述实验中a=_____ ,b=_____ 。
②上述实验中,能验证温度对化学反应速率影响规律的一组实验是_____ (填实验编号)。
(1)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是
(2)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。写出SO2吸收Br2反应的化学方程式为
(3)氮氧化物的治理是当前生态环境保护中的重要课题之一。从原理上看,NH3可用于治理NO2,该反应在催化剂条件下可实现,写出化学方程式
(4)一种新型催化剂能使NO和CO发生反应2NO+2CO
 2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:| 试验编号 | T(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| I | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| II | 280 | 1.20×10-3 | b | 124 |
| III | 350 | a | 5.80×10-3 | 82 |
②上述实验中,能验证温度对化学反应速率影响规律的一组实验是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】请回答在化学实验中发生下列意外事故时的处理方法:
(1)创伤处理:如被玻璃割伤________________________________ 。
(2)烫伤、烧伤的处理方法________________________________ 。
(3)少量浓硫酸沾到皮肤上________________________________ 。
(4)较多浓硫酸沾到皮肤上________________________________ 。
(5)浓碱沾到皮肤上________________________________ 。
(1)创伤处理:如被玻璃割伤
(2)烫伤、烧伤的处理方法
(3)少量浓硫酸沾到皮肤上
(4)较多浓硫酸沾到皮肤上
(5)浓碱沾到皮肤上
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】从矿石中获得化工原料
| 资源 | 名称 | 原理(主要的离子方程式、化学方程式) | 说明 |
| 矿产 | 1.工业制硫酸 |  (沸腾炉) (沸腾炉) (接触室) (接触室)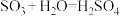 (吸收塔) (吸收塔) |  三步反应都是  ,得到发烟硫酸,再稀释 ,得到发烟硫酸,再稀释 |
| 2.铝的冶炼 |      |     一系列的变化是为了得到纯净的 一系列的变化是为了得到纯净的 | |
| 3.粗硅的提纯 |  粗硅提纯:   |  ,氧化产物不是 ,氧化产物不是 | |
| 4.硅酸盐工业——玻璃 |   | 制玻璃的原料是 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】锡(Sn)是第IVA族元素,其常见的氯化物有SnCl4和SnCl2.SnCl4常温下为液体,遇水极易发生水解反应;SnCl2常温下为固体,具有还原性,可被空气中的氧气氧化。某化学实验小组制备SnCl4的装置如图(加热与夹持装置省略)。

回答下列问题:
(1)仪器a的名称是_______ ;装置B中盛放的试剂是_______ 。
(2)制取SnCl4的操作步骤为:①连接好装置;②_______ ;③添加药品、滴加浓盐酸;④待装置D_______ 后,加热装置C;⑤收集SnCl4。请补充上述实验步骤。

回答下列问题:
(1)仪器a的名称是
(2)制取SnCl4的操作步骤为:①连接好装置;②
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】完成下列问题
(1)下列变化过程中有可能不涉及氧化还原反应的是_______
(2)氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用。下列叙述与氮元素的循环无关的是____
(3)关于新制饱和氯水,下列叙述正确的是_______
(4)下列实验中,能实现不同价态含硫物质的转化的是_______
(5)据文献报道,我国学者提出O2氧化HBr生成Br2的反应历程如图所示。下列有关该历程的说法错误的是_____

(6)高锰酸钾是生活中常用的一种消毒剂,也常被用于物质成分分析。二氧化锰是制取高锰酸钾的重要原料。制取高锰酸钾的方法是先用二氧化锰制取锰酸钾(K2MnO4),再转化为高锰酸钾。反应过程如下:
i.______MnO2+________KOH+____KClO3 ____K2MnO4+____KCl+____H2O
____K2MnO4+____KCl+____H2O
ii.3K2MnO4+4HCl=2KMnO4+4KCl+2H2O+MnO2
①下列反应中二氧化锰做氧化剂的是___________
a.实验室用氯酸钾和二氧化锰的混合物加热制取氧气
b.实验室用二氧化锰和浓盐酸混合加热制取氯气
c.用二氧化锰和铝混合发生铝热反应制取锰
d.用二氧化锰、氢氧化钾、氯酸钾共熔制取锰酸钾(K2MnO4)
②设计实验证明二氧化锰中含有哪种类型的化学键。(写出实验步骤、现象和结论)_________
③配平反应i的化学方程式_________ 。
④标出反应ii中电子转移的方向和数目_________ 。
⑤若工业上使用纯度为87%的软锰矿(主要成分为二氧化锰)制取高锰酸钾,理论上10吨软锰矿可制取高锰酸钾___________ 吨。
(1)下列变化过程中有可能不涉及氧化还原反应的是_______
| A.钝化 | B.漂白 | C.固氮 | D.燃烧 |
(2)氮元素在地球上含量丰富,氮及其化合物在工农业生产、生活中有着重要作用。下列叙述与氮元素的循环无关的是____
| A.工业合成氨的过程是固氮的过程 |
| B.自然界中,氨是动物体特别是蛋白质腐败后的产物 |
| C.为防止粮食、罐头、水果等食品腐烂,常用氮气作保护气 |
| D.在雷鸣的雨天,N2与O2会发生反应并最终转化为硝酸盐被植物吸收 |
(3)关于新制饱和氯水,下列叙述正确的是_______
| A.加入适量NaOH,溶液黄绿色褪去,说明氯水中含有Cl2分子 |
| B.加入少量NaCl粉末,溶液漂白性增强 |
| C.加入少量的碳酸钠粉末,pH增大,溶液漂白性一定减弱 |
| D.光照过程中,有气泡冒出,溶液的导电性减弱 |
(4)下列实验中,能实现不同价态含硫物质的转化的是_______
| A.向含足量NaOH的Na2S溶液中加入Na2SO3 |
| B.常温下,向试管中加入1mL浓硫酸和一小块铜片 |
| C.将0.5g硫粉和1.0g铁粉均匀混合,在石棉网上用红热玻璃棒触及粉末一端至粉末红热 |
| D.向Na2SO3固体中加入70%的浓硫酸制备SO2 |
(5)据文献报道,我国学者提出O2氧化HBr生成Br2的反应历程如图所示。下列有关该历程的说法错误的是_____

| A.O2氧化HBr生成Br2的总反应为:O2+4HBr=2Br2+2H2O |
| B.中间体HOOBr和HOBr中Br的化合价相同 |
| C.发生步骤②时,断裂的化学键既有极性键又有非极性键 |
| D.步骤③中,每生成1molBr2转移2mol电子 |
(6)高锰酸钾是生活中常用的一种消毒剂,也常被用于物质成分分析。二氧化锰是制取高锰酸钾的重要原料。制取高锰酸钾的方法是先用二氧化锰制取锰酸钾(K2MnO4),再转化为高锰酸钾。反应过程如下:
i.______MnO2+________KOH+____KClO3
 ____K2MnO4+____KCl+____H2O
____K2MnO4+____KCl+____H2Oii.3K2MnO4+4HCl=2KMnO4+4KCl+2H2O+MnO2
①下列反应中二氧化锰做氧化剂的是
a.实验室用氯酸钾和二氧化锰的混合物加热制取氧气
b.实验室用二氧化锰和浓盐酸混合加热制取氯气
c.用二氧化锰和铝混合发生铝热反应制取锰
d.用二氧化锰、氢氧化钾、氯酸钾共熔制取锰酸钾(K2MnO4)
②设计实验证明二氧化锰中含有哪种类型的化学键。(写出实验步骤、现象和结论)
③配平反应i的化学方程式
④标出反应ii中电子转移的方向和数目
⑤若工业上使用纯度为87%的软锰矿(主要成分为二氧化锰)制取高锰酸钾,理论上10吨软锰矿可制取高锰酸钾
您最近一年使用:0次

 体积液体的试管加热。(_____)
体积液体的试管加热。(_____)


