填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的化学符号:________ 。
(2)周期表中位于第8纵行的铁元素属于第________ 族。
(3)下列几种物质:①Ca(OH)2②H2O2③He④H2S ⑤MgCl2 ,只含有离子键的是(选填序号,下同)_________ ;只含有极性共价键的化合物是________ ;
(4)HClO的结构式______ ,I2的电子式______ 。
(5)下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④蔗糖溶液水⑤硫酸溶于水;未破坏化学键的是_____ ;
(6)下列不能说明氯元素原子得电子能力比硫元素原子得电子能力强的是_____________
①HCl的溶解度比H2S的大 ②HCl的酸性比H2S的强 ③HCl的稳定性比H2S的强④Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑤HClO4的酸性比H2SO4的强 ⑥Cl2能与H2S反应生成S
(1)写出表示含有8个质子、10个中子的原子的化学符号:
(2)周期表中位于第8纵行的铁元素属于第
(3)下列几种物质:①Ca(OH)2②H2O2③He④H2S ⑤MgCl2 ,只含有离子键的是(选填序号,下同)
(4)HClO的结构式
(5)下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④蔗糖溶液水⑤硫酸溶于水;未破坏化学键的是
(6)下列不能说明氯元素原子得电子能力比硫元素原子得电子能力强的是
①HCl的溶解度比H2S的大 ②HCl的酸性比H2S的强 ③HCl的稳定性比H2S的强④Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑤HClO4的酸性比H2SO4的强 ⑥Cl2能与H2S反应生成S
更新时间:2020-07-16 15:09:36
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】某化合物的化学式为Ca(H2RO4)2,则元素R的化合价是________ ,写出该元素以相同化合价形成的氧化物的化学式____________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】I.填空。
(1)人体的胃液中含有适量的盐酸,可以帮助消化。如果胃酸过多则需要服用药物,这些药物的主要成分可以是___________ (填字母序号)。
A.NaOH B. C.碳酸氢钠
C.碳酸氢钠
(2)人体体液中含有的最常见的电解质之一是氯化钠,目前我们食用的食盐中常常加入碘酸钾( ),其目的是防止人体缺碘。写出碘酸钾在水溶液中的电离方程式:
),其目的是防止人体缺碘。写出碘酸钾在水溶液中的电离方程式:___________ 。
(3)人体血液中含有下列物质,其中不属于电解质的是___________(填字母序号)。
II.有A、B、C、D四种化合物,分别由 、
、 、
、 、
、 、
、 中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(4)推断A、B、C、D的化学式。
A___________ ,B___________ ,C___________ ,D___________ 。
(5)写出下列反应的离子方程式。
B与盐酸反应:___________ ,
C与硫酸反应:___________ ,
E(少量)与澄清石灰水反应:___________ 。
(1)人体的胃液中含有适量的盐酸,可以帮助消化。如果胃酸过多则需要服用药物,这些药物的主要成分可以是
A.NaOH B.
 C.碳酸氢钠
C.碳酸氢钠(2)人体体液中含有的最常见的电解质之一是氯化钠,目前我们食用的食盐中常常加入碘酸钾(
 ),其目的是防止人体缺碘。写出碘酸钾在水溶液中的电离方程式:
),其目的是防止人体缺碘。写出碘酸钾在水溶液中的电离方程式:(3)人体血液中含有下列物质,其中不属于电解质的是___________(填字母序号)。
A. | B.水 | C.碳酸氢钠 | D.葡萄糖 |
II.有A、B、C、D四种化合物,分别由
 、
、 、
、 、
、 、
、 中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。(4)推断A、B、C、D的化学式。
A
(5)写出下列反应的离子方程式。
B与盐酸反应:
C与硫酸反应:
E(少量)与澄清石灰水反应:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】已知化学中有一些微粒核外均有10个电子,习惯上称“10电子微粒” 。根据要求填空:
(1)某电中性原子一般不和其他元素的原子反应,该原子的名称是_______ 。
(2)某单核微粒带一个单位负电荷,这种微粒的符号是_________ 。
(3)某单核微粒带一个单位正电荷,这种微粒的电子式是_________ 。
(4)某微粒得到2个电子后即变为原子,这种微粒的结构示意图是________ 。
(5)某微粒含有五个原子核并带一个单位正电荷,这种微粒的符号是_____ 。
(6)某微粒含有两个原子核且带一个单位负电荷,这种微粒的电子式是_____ 。
(1)某电中性原子一般不和其他元素的原子反应,该原子的名称是
(2)某单核微粒带一个单位负电荷,这种微粒的符号是
(3)某单核微粒带一个单位正电荷,这种微粒的电子式是
(4)某微粒得到2个电子后即变为原子,这种微粒的结构示意图是
(5)某微粒含有五个原子核并带一个单位正电荷,这种微粒的符号是
(6)某微粒含有两个原子核且带一个单位负电荷,这种微粒的电子式是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】铁盐在生产生活中有重要的作用。
(1)绿矾(FeSO4·7H2O)常用作补血剂。
①绿矾中含有的化学键类型有_______ 。
②配制含FeSO4的溶液时,为防止FeSO4被氧化,应采取的措施是_______ 。
(2)工业中常用高铁酸钾(K2FeO4)作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成Fe(OH)3胶体吸附杂质净水,同时还产生一种气体,该原理的离子方程式为_______ 。
(3)一种铁基脱硫剂脱除硫化氢(H2S)的方法包括吸收和再生两个阶段,其工艺流程原理如下:
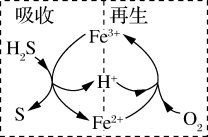
① 写出“再生”的反应的离子方程式:_______ 。
②当吸收224 mL(标准状况)H2S时,若要保持脱硫液中Fe3+的物质的量不变,则所通入的氧气的物质的量为_______ mol(写出计算过程)。
(1)绿矾(FeSO4·7H2O)常用作补血剂。
①绿矾中含有的化学键类型有
②配制含FeSO4的溶液时,为防止FeSO4被氧化,应采取的措施是
(2)工业中常用高铁酸钾(K2FeO4)作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成Fe(OH)3胶体吸附杂质净水,同时还产生一种气体,该原理的离子方程式为
(3)一种铁基脱硫剂脱除硫化氢(H2S)的方法包括吸收和再生两个阶段,其工艺流程原理如下:

① 写出“再生”的反应的离子方程式:
②当吸收224 mL(标准状况)H2S时,若要保持脱硫液中Fe3+的物质的量不变,则所通入的氧气的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】有以下8种物质:①Ne ②HCl ③ ④
④ ⑤
⑤ ⑥NaOH ⑦
⑥NaOH ⑦ ⑧
⑧
请用上述物质的序号填空:
(1)只存在离子键的是___________ 。
(2)只存在极性共价键的是___________ 。
(3)既存在非极性共价键又存在极性共价键的是___________ 。
(4)只存在非极性共价键的是___________ 。
(5)不存在化学键的是___________ 。
(6)既存在离子键又存在非极性共价键的是___________ 。
 ④
④ ⑤
⑤ ⑥NaOH ⑦
⑥NaOH ⑦ ⑧
⑧
请用上述物质的序号填空:
(1)只存在离子键的是
(2)只存在极性共价键的是
(3)既存在非极性共价键又存在极性共价键的是
(4)只存在非极性共价键的是
(5)不存在化学键的是
(6)既存在离子键又存在非极性共价键的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】有下列物质:①金属铜 ②NaOH ③I2 ④MgCl2 ⑤Na2O2 ⑥氩气 回答下列问题:
(1)不存在化学键的是_________________________
(2)只存在非极性键的是__________________________
(3)只存在离子键的是__________________________
(4)既存在离子键又存在极性键的是__________________________
(5)既存在离子键又存在非极性键的是____________________________
(1)不存在化学键的是
(2)只存在非极性键的是
(3)只存在离子键的是
(4)既存在离子键又存在极性键的是
(5)既存在离子键又存在非极性键的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】现有下列物质:
①N2②Na2O2③MgF2④NH4Cl⑤Na2CO3⑥NaOH⑦HCl⑧H2O2
(1)属于离子化合物的物质是_________ 。
(2)属于共价化合物的物质是_________ 。
(3)只由非极性键构成的物质是_________ 。
(4)由离子键和极性键构成的物质是_________ 。
(5)由极性键和非极性键构成的物质是_________ 。
①N2②Na2O2③MgF2④NH4Cl⑤Na2CO3⑥NaOH⑦HCl⑧H2O2
(1)属于离子化合物的物质是
(2)属于共价化合物的物质是
(3)只由非极性键构成的物质是
(4)由离子键和极性键构成的物质是
(5)由极性键和非极性键构成的物质是
您最近一年使用:0次
【推荐2】目前很多自来水厂使用ClO2来消毒、杀菌。工业制取ClO2的反应:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O。
(1)写出H2O的结构式_______ ,Na2SO4属于_______ 化合物(填“共价”或“离子”)。
(2)该反应的氧化剂为_______ 。
(3)用双线桥表示该反应的电子转移情况_______ 。
(1)写出H2O的结构式
(2)该反应的氧化剂为
(3)用双线桥表示该反应的电子转移情况
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】按照要求用序号回答下列问题:
(1)下列各种物质:①Ne ②HCl ③P4 ④NH4H ⑤Mg3N2 ⑥Ca(OH)2 ⑦CaC2 ⑧NH4I,只存在极性共价键的是___________ (填序号,下同);只存在非极性共价键的是___________ ;既存在离子键又存在非极性共价键的是___________ 。
(2)下列变化过程:①碘的升华 ②NaCl固体溶于水 ③O2溶于水 ④HCl气体溶于水 ⑤烧碱熔化 ⑥氯化铵受热分解,化学键没有被破坏的是___________ ;仅破坏离子键的是___________ ;仅破坏共价键的是___________ 。
(1)下列各种物质:①Ne ②HCl ③P4 ④NH4H ⑤Mg3N2 ⑥Ca(OH)2 ⑦CaC2 ⑧NH4I,只存在极性共价键的是
(2)下列变化过程:①碘的升华 ②NaCl固体溶于水 ③O2溶于水 ④HCl气体溶于水 ⑤烧碱熔化 ⑥氯化铵受热分解,化学键没有被破坏的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】完成下列填空。
(1)第三周期中,第一电离能最小的元素是___________ ,第一电离能最大的元素是___________ 。(填元素符号)
(2)分子中σ键数目:C2H4_____ CH4 ;原子轨道能量:3d___________ 4s(用“>”或“<”完成下列填空)
(3)N≡N的键能为942kJ·mol-1,N—N单键的键能为247kJ·mol-1,通过计算说明N2中的___________ 键更稳定(填“σ”或“π”)
(1)第三周期中,第一电离能最小的元素是
(2)分子中σ键数目:C2H4
(3)N≡N的键能为942kJ·mol-1,N—N单键的键能为247kJ·mol-1,通过计算说明N2中的
您最近一年使用:0次

 升华;③
升华;③ 溶于水;④
溶于水;④ 溶于水;⑤
溶于水;⑤ 溶于水;⑥
溶于水;⑥ 受热分解为
受热分解为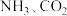 和
和 。其中仅离子键被破坏的是
。其中仅离子键被破坏的是

