完成下列填空。
(1)第三周期中,第一电离能最小的元素是___________ ,第一电离能最大的元素是___________ 。(填元素符号)
(2)分子中σ键数目:C2H4_____ CH4 ;原子轨道能量:3d___________ 4s(用“>”或“<”完成下列填空)
(3)N≡N的键能为942kJ·mol-1,N—N单键的键能为247kJ·mol-1,通过计算说明N2中的___________ 键更稳定(填“σ”或“π”)
(1)第三周期中,第一电离能最小的元素是
(2)分子中σ键数目:C2H4
(3)N≡N的键能为942kJ·mol-1,N—N单键的键能为247kJ·mol-1,通过计算说明N2中的
18-19高二上·福建福州·期中 查看更多[2]
【校级联考】福建省福州市三校2018-2019学年高二(理)上学期期中联考化学试题(已下线)第二单元 化学键与分子间作用力(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版选修3)
更新时间:2018-11-26 23:08:57
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】非金属元素在生产生活中扮演着重要角色。请根据题意填空:
(1)为了达到更好的消毒效果,我国已开始使用新的自来水消毒剂,如臭氧、___________ (填“ ”或“HCl”)等。
”或“HCl”)等。
(2)硝酸是一种重要的化工原料,在浓硝酸的运输过程中,可选择___________ (填“铁”或“铜”)作为罐体材料。
(3)碳化硅(SiC)具有类似金刚石的结构,可用作砂纸和砂轮的磨料,其中碳原子和硅原子之间的相互作用为___________ (填“离子键”或“共价键”)。
(1)为了达到更好的消毒效果,我国已开始使用新的自来水消毒剂,如臭氧、
 ”或“HCl”)等。
”或“HCl”)等。(2)硝酸是一种重要的化工原料,在浓硝酸的运输过程中,可选择
(3)碳化硅(SiC)具有类似金刚石的结构,可用作砂纸和砂轮的磨料,其中碳原子和硅原子之间的相互作用为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】有下列晶体:①冰 ②金刚石 ③氩 ④过氧化钠 ⑤二氧化硅 ⑥氯化镁 ⑦过氧化氢 ⑧白磷 ⑨氯化铵。用序号回答下列问题:
(1)只含有离子键的是________ ;
(2)只含有极性共价键的分子晶体是________ ;
(3)固态时,晶体中只含有范德华力的是______ ;
(4)含有非极性键的离子晶体是_______ ;
(5)只含有离子键的离子晶体是________ ;
(6)只含有非极性键的原子晶体是_________ ;
(1)只含有离子键的是
(2)只含有极性共价键的分子晶体是
(3)固态时,晶体中只含有范德华力的是
(4)含有非极性键的离子晶体是
(5)只含有离子键的离子晶体是
(6)只含有非极性键的原子晶体是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】实验室有如下物质:①熔融的氢氧化钠② 固体③金属铁④稀硫酸⑤二氧化碳气体⑥氨水⑦熔融
固体③金属铁④稀硫酸⑤二氧化碳气体⑥氨水⑦熔融 ⑧蔗糖晶体⑨
⑧蔗糖晶体⑨ 固体⑩
固体⑩ 晶体
晶体
(1)上述状态下可导电的是______ ;
(2)属于电解质的是______ ;
(3)属于非电解质的是______ ;
(4)上述状态下的电解质不能导电的是______ 。
 固体③金属铁④稀硫酸⑤二氧化碳气体⑥氨水⑦熔融
固体③金属铁④稀硫酸⑤二氧化碳气体⑥氨水⑦熔融 ⑧蔗糖晶体⑨
⑧蔗糖晶体⑨ 固体⑩
固体⑩ 晶体
晶体(1)上述状态下可导电的是
(2)属于电解质的是
(3)属于非电解质的是
(4)上述状态下的电解质不能导电的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在下列物质中:①HCl、②N2、③NH3、④Na2O2、⑤H2O2、⑥NH4Cl、⑦NaOH、⑧Ar、⑨CO2、⑩C2H4
(1)只存在非极性键的分子是___ ;既存在非极性键又存在极性键的分子是___ ;只存在极性键的分子是____ 。
(2)只存在单键的分子是___ ,存在叁键的分子是___ ,只存在双键的分子是____ ,既存在单键又存在双键的分子是____ 。
(3)只存在σ键的分子是___ ,既存在σ键又存在π键的分子是____ 。
(4)不存在化学键的是____ 。
(5)既存在离子键又存在极性键的是___ ;既存在离子键又存在非极性键的是___ 。
(1)只存在非极性键的分子是
(2)只存在单键的分子是
(3)只存在σ键的分子是
(4)不存在化学键的是
(5)既存在离子键又存在极性键的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】氮和氮的化合物与人类有密切关系.
(1)氮的固定有利于生物吸收氮.下列属于氮的固定的是_______ (填序号).
①工业上N2和H2合成NH3 ②N2和O2放电条件下生成NO ③NH3催化氧化生成NO
写出反应③的化学方程式_______ .
(2)治理NO通常是在氧化剂作用下,将NO氧化成溶解度高的NO2,然后用水或碱液吸收脱氮.下列物质可以用作氧化NO的是_______ (填序号).
A.NaCl溶液 B.NaOH溶液 C.Na2CO3溶液 D.KMnO4溶液
若以NaClO溶液氧化NO,写出该反应的化学方程式,并用双线桥法标出反应中电子的得失和数目_______ .
(3)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用Rh做催化剂时该反应的过程示意图如下:

①过程Ⅰ为_______ 过程(填“吸热”或“放热”)。过程Ⅱ生成的化学键有_______ (填“极性键”、“非极性键”或“极性键和非极性键”)
②已知过程Ⅰ的焓变为akJ/mol,过程Ⅱ的焓变为bkJ/mol,则该反应的热化学方程式为_______ 。
(1)氮的固定有利于生物吸收氮.下列属于氮的固定的是
①工业上N2和H2合成NH3 ②N2和O2放电条件下生成NO ③NH3催化氧化生成NO
写出反应③的化学方程式
(2)治理NO通常是在氧化剂作用下,将NO氧化成溶解度高的NO2,然后用水或碱液吸收脱氮.下列物质可以用作氧化NO的是
A.NaCl溶液 B.NaOH溶液 C.Na2CO3溶液 D.KMnO4溶液
若以NaClO溶液氧化NO,写出该反应的化学方程式,并用双线桥法标出反应中电子的得失和数目
(3)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用Rh做催化剂时该反应的过程示意图如下:

①过程Ⅰ为
②已知过程Ⅰ的焓变为akJ/mol,过程Ⅱ的焓变为bkJ/mol,则该反应的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
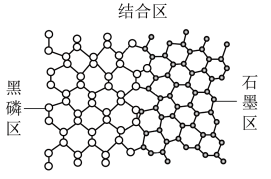
【推荐1】为提高锂电池的充电速率,科学家最近研发了黑磷~石墨复合负极材料,其单层结构俯视图如图所示。石墨与黑磷制备该复合材料的过程,发生了___________ (选填“物理”或“化学”)变化,复合材料单层中,P原子与C原子之间的作用力是___________ (选填“离子键”或“共价键”)。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在化合物YX2、ZX2中,X、Y、Z都是短周期元素,X与Y在同一周期,Z与X在同一主族,Z元素的原子核内有16个质子,Y元素原子最外层电子数是K层所能容纳的电子数的2倍。试写出YX2和ZX2的化学式____ 、____ ,并用电子式表示YX2的形成过程____ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】我国复旦大学魏大程团队开发的一种共形六方氮化硼修饰技术,可直接在二氧化硅表面生长高质量六方氮化硼薄膜。
(1)下列N原子的电子排布图表示的状态中,能量最高的是___________(填字母)。
(2)第二周期主族元素中,按第一电离能大小排序,第一电离能在B和N之间的元素有___________ 种。
(3)Na与N形成的 可用于汽车的安全气囊中,其中阴离子的空间结构为
可用于汽车的安全气囊中,其中阴离子的空间结构为___________ ,Na在空气中燃烧发出黄色火焰,这种黄色焰色用光谱仪摄取的光谱为___________ (填“发射”或“吸收”)光谱。
(4) 与同主族磷的氢化物
与同主族磷的氢化物 键角大小比较
键角大小比较___________ ,请解释 的键角比
的键角比 的键角大的原因:
的键角大的原因:___________ 。
(1)下列N原子的电子排布图表示的状态中,能量最高的是___________(填字母)。
A. | B. |
C. | D. |
(2)第二周期主族元素中,按第一电离能大小排序,第一电离能在B和N之间的元素有
(3)Na与N形成的
 可用于汽车的安全气囊中,其中阴离子的空间结构为
可用于汽车的安全气囊中,其中阴离子的空间结构为(4)
 与同主族磷的氢化物
与同主族磷的氢化物 键角大小比较
键角大小比较 的键角比
的键角比 的键角大的原因:
的键角大的原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)Cs(铯)的最外层电子排布式为6s1,与铯同主族的前四周期(包括第四周期)的三种元素A、B、C的电离能如下表:
那么三种元素A、B、C的元素符号分别为_______ ,形成其单质晶体的化学键类型是_______ 。
(2)F与I同主族,BeF2与H2O都是由三个原子构成的共价化合物分子,二者分子中的中心原子Be和O的杂化方式分别是_______ 、_______ 。
(3)与碘同主族的氯具有较高的活泼性,能够形成大量的含氯化合物,如金属氯化物、非金属氯化物等。BCl3是一种非金属氯化物,该物质分子中B—Cl键的键角为_______ 。
(4)碘131是碘单质,其晶胞结构如图甲所示,该晶胞中含有_______ 个I2分子;KI的晶胞结构如图乙所示,每个K+紧邻_______ 个I-。
元素代号 | A | B | C |
第一电离能/(kJ·mol-1) | 520 | 496 | 419 |
(2)F与I同主族,BeF2与H2O都是由三个原子构成的共价化合物分子,二者分子中的中心原子Be和O的杂化方式分别是
(3)与碘同主族的氯具有较高的活泼性,能够形成大量的含氯化合物,如金属氯化物、非金属氯化物等。BCl3是一种非金属氯化物,该物质分子中B—Cl键的键角为
(4)碘131是碘单质,其晶胞结构如图甲所示,该晶胞中含有

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】磷是生物体中不可缺少的元素之一,它能形成多种化合物。
(1)基态磷原子中,电子占据的最高能层符号为________ ;该能层能量最高的电子云在空间有________ 个伸展方向,原子轨道呈________ 形。
(2)磷元素与同周期相邻两元素相比,第一电离能由大到小的顺序为________ 。
(3)单质磷与Cl2反应,可以生成PCl3和PCl5,其中各原子均满足8电子稳定结构的化合物中,P原子的杂化轨道类型为________ ,其分子的空间构型为________ 。
(4)H3PO4为三元中强酸,与Fe3+形成H3[Fe(PO4)2],此性质常用于掩蔽溶液中的Fe3+。基态Fe3+的核外电子排布式为____________________ ;PO43-作为________ 为Fe提供________ 。
(1)基态磷原子中,电子占据的最高能层符号为
(2)磷元素与同周期相邻两元素相比,第一电离能由大到小的顺序为
(3)单质磷与Cl2反应,可以生成PCl3和PCl5,其中各原子均满足8电子稳定结构的化合物中,P原子的杂化轨道类型为
(4)H3PO4为三元中强酸,与Fe3+形成H3[Fe(PO4)2],此性质常用于掩蔽溶液中的Fe3+。基态Fe3+的核外电子排布式为
您最近一年使用:0次



