氮和氮的化合物与人类有密切关系.
(1)氮的固定有利于生物吸收氮.下列属于氮的固定的是_______ (填序号).
①工业上N2和H2合成NH3 ②N2和O2放电条件下生成NO ③NH3催化氧化生成NO
写出反应③的化学方程式_______ .
(2)治理NO通常是在氧化剂作用下,将NO氧化成溶解度高的NO2,然后用水或碱液吸收脱氮.下列物质可以用作氧化NO的是_______ (填序号).
A.NaCl溶液 B.NaOH溶液 C.Na2CO3溶液 D.KMnO4溶液
若以NaClO溶液氧化NO,写出该反应的化学方程式,并用双线桥法标出反应中电子的得失和数目_______ .
(3)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用Rh做催化剂时该反应的过程示意图如下:

①过程Ⅰ为_______ 过程(填“吸热”或“放热”)。过程Ⅱ生成的化学键有_______ (填“极性键”、“非极性键”或“极性键和非极性键”)
②已知过程Ⅰ的焓变为akJ/mol,过程Ⅱ的焓变为bkJ/mol,则该反应的热化学方程式为_______ 。
(1)氮的固定有利于生物吸收氮.下列属于氮的固定的是
①工业上N2和H2合成NH3 ②N2和O2放电条件下生成NO ③NH3催化氧化生成NO
写出反应③的化学方程式
(2)治理NO通常是在氧化剂作用下,将NO氧化成溶解度高的NO2,然后用水或碱液吸收脱氮.下列物质可以用作氧化NO的是
A.NaCl溶液 B.NaOH溶液 C.Na2CO3溶液 D.KMnO4溶液
若以NaClO溶液氧化NO,写出该反应的化学方程式,并用双线桥法标出反应中电子的得失和数目
(3)CO与NO在Rh催化剂上的氧化还原反应是控制汽车尾气对空气污染的关键反应。用Rh做催化剂时该反应的过程示意图如下:

①过程Ⅰ为
②已知过程Ⅰ的焓变为akJ/mol,过程Ⅱ的焓变为bkJ/mol,则该反应的热化学方程式为
20-21高二下·四川成都·期末 查看更多[3]
四川省成都市2020-2021学年高二下学期期末考试(2022届零诊)化学试题(已下线)1.3 化学反应热的计算-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第一单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)
更新时间:2021-07-15 10:01:44
|
相似题推荐
【推荐1】请回答有关合金的知识。
(1)电器修理中所用的焊锡是锡铅合金,它的熔点比纯铅的熔点_________ (填“高”或“低”);镁铝合金用于飞机制造,其硬度比纯铝的硬度_____________ (填“大”或“小”)。
(2)古代的“药金”外观与金相似,常被误认为是金子。将碳酸锌、木炭、赤铜(Cu2O)混合加热到800℃,就可得到金光闪闪的“药金”。“药金”的主要成分是__________ 。有关的化学方程式是 ___________________ ;_____________ ;________________ 。
(1)电器修理中所用的焊锡是锡铅合金,它的熔点比纯铅的熔点
(2)古代的“药金”外观与金相似,常被误认为是金子。将碳酸锌、木炭、赤铜(Cu2O)混合加热到800℃,就可得到金光闪闪的“药金”。“药金”的主要成分是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按要求完成下列填空:
(1)写出 在水中的电离方程式
在水中的电离方程式___________ 。
(2)向新制氯水中滴加石蕊试液,溶液变红,起作用的微粒是___________ ;然后又褪色,起作用的微粒是___________ 。
(3)实验证明铜、不能在低温下与 反应,也不能与稀
反应,也不能与稀 共热发生反应,但工业上却是将废铜屑倒入热的稀
共热发生反应,但工业上却是将废铜屑倒入热的稀 中并通入空气来制备
中并通入空气来制备 溶液的。铜屑在此状态下被溶解的化学方程式为
溶液的。铜屑在此状态下被溶解的化学方程式为___________ 。
(4)过量铁粉与稀硝酸反应方程式为: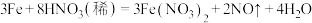 此反应中,被还原和未被还原的硝酸的物质的量之比为
此反应中,被还原和未被还原的硝酸的物质的量之比为___________ 。当产生 气体在标况下体积为
气体在标况下体积为 时,转移电子
时,转移电子___________  ,被还原的硝酸的物质的量为
,被还原的硝酸的物质的量为___________  。
。
(5)漂白粉是常用的消毒剂。漂白粉的有效成分是(填化学式)___________ 。
(1)写出
 在水中的电离方程式
在水中的电离方程式(2)向新制氯水中滴加石蕊试液,溶液变红,起作用的微粒是
(3)实验证明铜、不能在低温下与
 反应,也不能与稀
反应,也不能与稀 共热发生反应,但工业上却是将废铜屑倒入热的稀
共热发生反应,但工业上却是将废铜屑倒入热的稀 中并通入空气来制备
中并通入空气来制备 溶液的。铜屑在此状态下被溶解的化学方程式为
溶液的。铜屑在此状态下被溶解的化学方程式为(4)过量铁粉与稀硝酸反应方程式为:
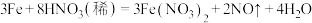 此反应中,被还原和未被还原的硝酸的物质的量之比为
此反应中,被还原和未被还原的硝酸的物质的量之比为 气体在标况下体积为
气体在标况下体积为 时,转移电子
时,转移电子 ,被还原的硝酸的物质的量为
,被还原的硝酸的物质的量为 。
。(5)漂白粉是常用的消毒剂。漂白粉的有效成分是(填化学式)
您最近一年使用:0次
【推荐3】金属及其化合物在生产和生活中有广泛的应用。回答下列问题:
(1)一种管道疏通剂的主要成分有NaOH和铝粉,解释该疏通剂的疏通原理_______ 。
(2)汽车安全气囊内装有NaN3、Fe2O3和NaHCO3等物质。
①当汽车发生严重碰撞时,引发NaN3分解并放出大量的热:2NaN3 2Na+3N2↑。该反应中氧化产物和还原产物的物质的量之比为
2Na+3N2↑。该反应中氧化产物和还原产物的物质的量之比为_______ 。
②产生的Na立即与Fe2O3发生置换反应生成Na2O,反应的化学方程式为_______ 。
(3)在含有Fe3+、Cu2+、Cl-、H+的混合溶液中加入铁粉,充分反应后,溶液中剩余固体可被磁铁吸引。此时溶液中存在较多的阳离子是_______ (填离子符号)。
(1)一种管道疏通剂的主要成分有NaOH和铝粉,解释该疏通剂的疏通原理
(2)汽车安全气囊内装有NaN3、Fe2O3和NaHCO3等物质。
①当汽车发生严重碰撞时,引发NaN3分解并放出大量的热:2NaN3
 2Na+3N2↑。该反应中氧化产物和还原产物的物质的量之比为
2Na+3N2↑。该反应中氧化产物和还原产物的物质的量之比为②产生的Na立即与Fe2O3发生置换反应生成Na2O,反应的化学方程式为
(3)在含有Fe3+、Cu2+、Cl-、H+的混合溶液中加入铁粉,充分反应后,溶液中剩余固体可被磁铁吸引。此时溶液中存在较多的阳离子是
您最近一年使用:0次
【推荐1】铜冶金术以火法治为主,炼铜的副产品SO2多用于制硫酸和石背等化学产品。火法炼铜的工艺流程如下:

反应I:2Cu2S(s)+3O2(g)→2Cu2O(s)+2SO2(g)+768.2kJ
反应II:2Cu2O(s)+Cu2S(s)→6Cu(s)+SO2(g)-116.0kJ
(1)在反应Ⅱ中,每生成1mol SO2转移电子_______ mol,反应Cu2S(s)+O2(g)→2Cu(s)+SO2(g)+Q的Q=_____ kJ。
(2)理论上m1:m2=_________ 。

反应I:2Cu2S(s)+3O2(g)→2Cu2O(s)+2SO2(g)+768.2kJ
反应II:2Cu2O(s)+Cu2S(s)→6Cu(s)+SO2(g)-116.0kJ
(1)在反应Ⅱ中,每生成1mol SO2转移电子
(2)理论上m1:m2=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】大气中的部分碘源于O3对海水中I-的氧化。某科学小组进行O3与含I-溶液反应相关研究。
(1)O3将I-氧化生成I2的过程由3步反应组成:
①I-(aq)+O3(g)=IO-(aq)+O2(g)
②IO-(aq)+H+(aq) HOI(aq)
HOI(aq)
③HOI(aq)+I-(aq)+H+(aq) I2(aq)+H2O(l) 写出O3氧化I-生成I2的化学方程式
I2(aq)+H2O(l) 写出O3氧化I-生成I2的化学方程式___________ 。
(2)O3在水中易分解,在一定条件下,O3的浓度减少一半时所需的时间(t)如下表所示。已知:O3的起始浓度为0.021 6 mol·L-1。
①在30 ℃、pH=4.0条件下,O3的分解速率为___________ mol·L-1·min-1。
②pH增大能加速O3分解,表明对O3分解起催化作用的是___________ 。
③根据表中数据,推测O3在下列条件下分解速率依次增大的顺序为___________ (填字母代号)。 a.40 ℃、pH=3.0 b.10 ℃、pH=4.0 c.30 ℃、pH=7.0
(3)PbSO4热激活电池可用作火箭、导弹的工作电源。基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。

①放电过程中,Cl-向___________ 填(“负极”或“正极”)移动。
②正极电极方程式为___________ 。
③电路中每转移0.3 mol电子,理论上会消耗___________ g Ca。
(1)O3将I-氧化生成I2的过程由3步反应组成:
①I-(aq)+O3(g)=IO-(aq)+O2(g)
②IO-(aq)+H+(aq)
 HOI(aq)
HOI(aq)③HOI(aq)+I-(aq)+H+(aq)
 I2(aq)+H2O(l) 写出O3氧化I-生成I2的化学方程式
I2(aq)+H2O(l) 写出O3氧化I-生成I2的化学方程式(2)O3在水中易分解,在一定条件下,O3的浓度减少一半时所需的时间(t)如下表所示。已知:O3的起始浓度为0.021 6 mol·L-1。
| pH t/min T/℃ | 3.0 | 4.0 | 5.0 | 6.0 |
| 20 | 301 | 231 | 169 | 58 |
| 30 | 158 | 108 | 48 | 15 |
| 50 | 31 | 35 | 15 | 7 |
②pH增大能加速O3分解,表明对O3分解起催化作用的是
③根据表中数据,推测O3在下列条件下分解速率依次增大的顺序为
(3)PbSO4热激活电池可用作火箭、导弹的工作电源。基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。

①放电过程中,Cl-向
②正极电极方程式为
③电路中每转移0.3 mol电子,理论上会消耗
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】在容积为0.4L的容器中,通入一定量的N2O4,发生反应N2O4(g) 2NO2(g),升高温度,混合气体的颜色变深。回答下列问题:
2NO2(g),升高温度,混合气体的颜色变深。回答下列问题:
(1)该反应的△H_______ 0(填“>”或“<”下同)。
(2)100℃时,体系中各物质浓度随时间变化如图所示。

在0~60s时段,反应速率v(N2O4)为__________ ;反应的平衡常数K的值为_________ 。反应达平衡后,再向容器中充入0.4molN2O4。平衡向_________ (填“正反应”或“逆反应”)方向移动,再次达到平衡时,N2O4的转化率与原平衡相比_________ (填“变大”“变小”或“不变”)。
(3)100℃,相同容器中充入2.4molNO2与0.8molN2O4,则反应达平衡之前v正_____ v逆。
 2NO2(g),升高温度,混合气体的颜色变深。回答下列问题:
2NO2(g),升高温度,混合气体的颜色变深。回答下列问题:(1)该反应的△H
(2)100℃时,体系中各物质浓度随时间变化如图所示。

在0~60s时段,反应速率v(N2O4)为
(3)100℃,相同容器中充入2.4molNO2与0.8molN2O4,则反应达平衡之前v正
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】能源危机当前是一个全球性问题,开源节流是应对能源危机的重要举措。
(1)下列做法有助于能源“开源节流”的是__________________ (填字母)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源、减少使用煤、石油等化石燃料
d.减少资源消耗,注重资源的重复使用、资源的循环再生
(2)水既是人们每天赖以生存的资源,也是工业生产的必要溶剂。
①已知H2 (g)+ O2(g)=H2O(g)反应过程中能量变化如图,图中a代表
O2(g)=H2O(g)反应过程中能量变化如图,图中a代表____________________________________ ;
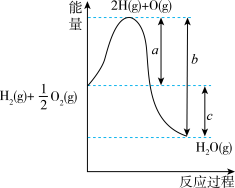
②已知:2H2(g)+O2(g)═2H2O(l) ΔH1=-285.8kJ∙mol﹣1;H2(g)═H2(l) ΔH2=-0.92kJ∙mol﹣1;O2(g)═O2(l) ΔH3=-6.84kJ∙mol﹣1;H2O(l)═H2O(g) ΔH4=+44.0kJ∙mol﹣1,请写出液氢和液氧生成气态水的热化学方程式:__________________________ 。
(3)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。

①在通常状况下,金刚石和石墨相比较,________ (填”金刚石”或”石墨”)更稳定,石墨的燃烧热为________ kJ∙mol-1。
②12g石墨在一定量的空气中燃烧,生成气体36 g,该过程放出的热量为________ kJ。
(1)下列做法有助于能源“开源节流”的是
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源、减少使用煤、石油等化石燃料
d.减少资源消耗,注重资源的重复使用、资源的循环再生
(2)水既是人们每天赖以生存的资源,也是工业生产的必要溶剂。
①已知H2 (g)+
 O2(g)=H2O(g)反应过程中能量变化如图,图中a代表
O2(g)=H2O(g)反应过程中能量变化如图,图中a代表
②已知:2H2(g)+O2(g)═2H2O(l) ΔH1=-285.8kJ∙mol﹣1;H2(g)═H2(l) ΔH2=-0.92kJ∙mol﹣1;O2(g)═O2(l) ΔH3=-6.84kJ∙mol﹣1;H2O(l)═H2O(g) ΔH4=+44.0kJ∙mol﹣1,请写出液氢和液氧生成气态水的热化学方程式:
(3)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。

①在通常状况下,金刚石和石墨相比较,
②12g石墨在一定量的空气中燃烧,生成气体36 g,该过程放出的热量为
您最近一年使用:0次
【推荐2】氢气既是一种优质的能源,又是一种重要化工原料,高纯氢的制备是目前的研究热点。
(1)甲烷水蒸气催化重整是制备高纯氢的方法之一,甲烷和水蒸气反应的热化学方程式是:CH4(g)+2H2O(g) CO2(g)+4H2(g) ∆H=+165.0kJ·mol-1,已知反应器中存在如下反应过程:
CO2(g)+4H2(g) ∆H=+165.0kJ·mol-1,已知反应器中存在如下反应过程:
I.CH4(g)+H2O(g)⇌CO(g)+3H2(g)∆H1=+206.4kJ·mol-1
II.CO(g)+H2O(g)⇌CO2(g)+H2(g)∆H2
根据上述信息计算:∆H2=_______ 。
(2)某温度下,4molH2O和lmolCH4在体积为2L的刚性容器内同时发生I、II反应,达平衡时,体系中n(CO)=bmol、n(CO2)=dmol,则该温度下反应I的平衡常数K值为_______ (用字母表示)。
(3)欲增大CH4转化为H2的平衡转化率,可采取的措施有_______ 填标号)。
A.适当增大反应物投料比n(H2O)∶n(CH4)
B.提高压强
C.分离出CO2
(4)H2用于工业合成氨:N2+3H2 2NH3.将n(N2)∶n(H2)=1∶3的混合气体,匀速通过装有催化剂的反应器反应,反应器温度变化与从反应器排出气体中NH3的体积分数φ(NH3)关系如图,反应器温度升高NH3的体积分数φ(NH3)先增大后减小的原因是
2NH3.将n(N2)∶n(H2)=1∶3的混合气体,匀速通过装有催化剂的反应器反应,反应器温度变化与从反应器排出气体中NH3的体积分数φ(NH3)关系如图,反应器温度升高NH3的体积分数φ(NH3)先增大后减小的原因是_______ 。

(5)某温度下,n(N2)∶n(H2)=1∶3的混合气体在刚性容器内发生反应,起始气体总压为2×l07Pa,平衡时总压为开始的90%,则H2的转化率为_______ 。
(1)甲烷水蒸气催化重整是制备高纯氢的方法之一,甲烷和水蒸气反应的热化学方程式是:CH4(g)+2H2O(g)
 CO2(g)+4H2(g) ∆H=+165.0kJ·mol-1,已知反应器中存在如下反应过程:
CO2(g)+4H2(g) ∆H=+165.0kJ·mol-1,已知反应器中存在如下反应过程:I.CH4(g)+H2O(g)⇌CO(g)+3H2(g)∆H1=+206.4kJ·mol-1
II.CO(g)+H2O(g)⇌CO2(g)+H2(g)∆H2
| 化学键 | H-H | O-H | C-H | C≡O |
| 键能E/(kJ·mol-1) | 436 | 465 | a | 1076 |
(2)某温度下,4molH2O和lmolCH4在体积为2L的刚性容器内同时发生I、II反应,达平衡时,体系中n(CO)=bmol、n(CO2)=dmol,则该温度下反应I的平衡常数K值为
(3)欲增大CH4转化为H2的平衡转化率,可采取的措施有
A.适当增大反应物投料比n(H2O)∶n(CH4)
B.提高压强
C.分离出CO2
(4)H2用于工业合成氨:N2+3H2
 2NH3.将n(N2)∶n(H2)=1∶3的混合气体,匀速通过装有催化剂的反应器反应,反应器温度变化与从反应器排出气体中NH3的体积分数φ(NH3)关系如图,反应器温度升高NH3的体积分数φ(NH3)先增大后减小的原因是
2NH3.将n(N2)∶n(H2)=1∶3的混合气体,匀速通过装有催化剂的反应器反应,反应器温度变化与从反应器排出气体中NH3的体积分数φ(NH3)关系如图,反应器温度升高NH3的体积分数φ(NH3)先增大后减小的原因是
(5)某温度下,n(N2)∶n(H2)=1∶3的混合气体在刚性容器内发生反应,起始气体总压为2×l07Pa,平衡时总压为开始的90%,则H2的转化率为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】化学反应过程既是物质的转化过程,也是能量的转化过程。
(1)下列属于吸热过程的是___________ (填序号)。
a.CO燃烧 b.铝和稀盐酸反应 c.碳酸氢钠溶于水 d.石灰石分解
(2)t℃时,关于N2、NH3的两个反应的信息如下表所示:
请写出t℃时,NH3被NO氧化生成无毒气体的热化学方程式___________ (反应热用a、b、c、d代数式表示)。t℃时,该反应的平衡常数___________ (用K1和K2表示)。
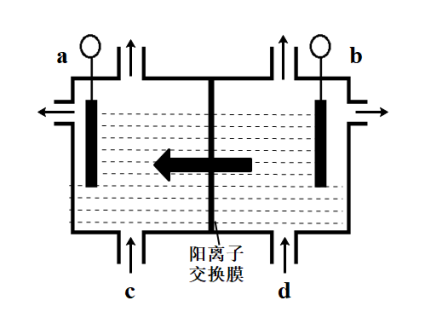
(3)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出如图所示用电解法制取ClO2的新工艺。用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。精制饱和食盐水入口是_______ 口(填“c”或“d”)产生ClO2的电极反应式为_______ 。
(1)下列属于吸热过程的是
a.CO燃烧 b.铝和稀盐酸反应 c.碳酸氢钠溶于水 d.石灰石分解
(2)t℃时,关于N2、NH3的两个反应的信息如下表所示:
| 化学反应 | 正反应活化能 | 逆反应活化能 | t℃时平衡常数 |
| N2(g)+O2(g)=2NO(g) △H>0 | akJ/mol | bkJ/mol | K1 |
| 4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H<0 | ckJ/mol | dkJ/mol | K2 |
(3)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出如图所示用电解法制取ClO2的新工艺。用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。精制饱和食盐水入口是

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】按照要求用序号回答下列问题:
(1)下列各种物质:①Ne ②HCl ③P4 ④NH4H ⑤Mg3N2 ⑥Ca(OH)2 ⑦CaC2 ⑧NH4I,只存在极性共价键的是___________ (填序号,下同);只存在非极性共价键的是___________ ;既存在离子键又存在非极性共价键的是___________ 。
(2)下列变化过程:①碘的升华 ②NaCl固体溶于水 ③O2溶于水 ④HCl气体溶于水 ⑤烧碱熔化 ⑥氯化铵受热分解,化学键没有被破坏的是___________ ;仅破坏离子键的是___________ ;仅破坏共价键的是___________ 。
(1)下列各种物质:①Ne ②HCl ③P4 ④NH4H ⑤Mg3N2 ⑥Ca(OH)2 ⑦CaC2 ⑧NH4I,只存在极性共价键的是
(2)下列变化过程:①碘的升华 ②NaCl固体溶于水 ③O2溶于水 ④HCl气体溶于水 ⑤烧碱熔化 ⑥氯化铵受热分解,化学键没有被破坏的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】位于元素周期表第七周期第VA族的元素Mc中文名为“镆”是2016年才确认的新元素。回答下列问题:
(1)元素Mc可由反应: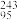 Am+
Am+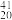 Ca=
Ca= Mc+3
Mc+3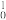 n得到。反应中钙原子的核内中子数为
n得到。反应中钙原子的核内中子数为___ ,镆元素的质子数为___ 。
(2)与Mc同族的元素的一种氢化物分子式为N2H4,写出该氢化物的电子式:___ ,该分子内存在的共价键类型有___ 。
(3)与Mc同族的元素P能呈现多种化合价,其中+3价氯化物的化学式为___ ,+5价简单含氧酸的分子式为___ 。
(1)元素Mc可由反应:
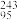 Am+
Am+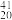 Ca=
Ca= Mc+3
Mc+3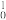 n得到。反应中钙原子的核内中子数为
n得到。反应中钙原子的核内中子数为(2)与Mc同族的元素的一种氢化物分子式为N2H4,写出该氢化物的电子式:
(3)与Mc同族的元素P能呈现多种化合价,其中+3价氯化物的化学式为
您最近一年使用:0次

 固体③金属铁④稀硫酸⑤二氧化碳气体⑥氨水⑦熔融
固体③金属铁④稀硫酸⑤二氧化碳气体⑥氨水⑦熔融 ⑧蔗糖晶体⑨
⑧蔗糖晶体⑨ 固体⑩
固体⑩ 晶体
晶体

