化学反应过程既是物质的转化过程,也是能量的转化过程。
(1)下列属于吸热过程的是___________ (填序号)。
a.CO燃烧 b.铝和稀盐酸反应 c.碳酸氢钠溶于水 d.石灰石分解
(2)t℃时,关于N2、NH3的两个反应的信息如下表所示:
请写出t℃时,NH3被NO氧化生成无毒气体的热化学方程式___________ (反应热用a、b、c、d代数式表示)。t℃时,该反应的平衡常数___________ (用K1和K2表示)。
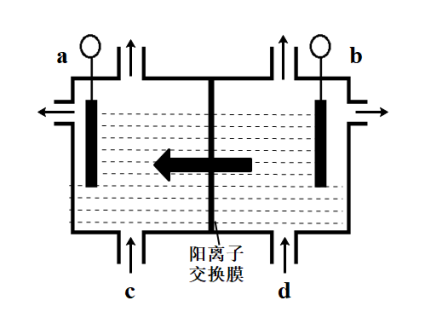
(3)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出如图所示用电解法制取ClO2的新工艺。用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。精制饱和食盐水入口是_______ 口(填“c”或“d”)产生ClO2的电极反应式为_______ 。
(1)下列属于吸热过程的是
a.CO燃烧 b.铝和稀盐酸反应 c.碳酸氢钠溶于水 d.石灰石分解
(2)t℃时,关于N2、NH3的两个反应的信息如下表所示:
| 化学反应 | 正反应活化能 | 逆反应活化能 | t℃时平衡常数 |
| N2(g)+O2(g)=2NO(g) △H>0 | akJ/mol | bkJ/mol | K1 |
| 4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H<0 | ckJ/mol | dkJ/mol | K2 |
(3)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出如图所示用电解法制取ClO2的新工艺。用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。精制饱和食盐水入口是

更新时间:2022-01-23 21:22:37
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】回答下列问题。
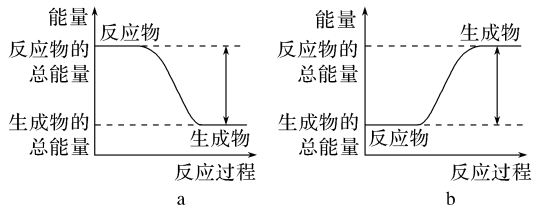
(1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知该反应为放热反应,如图能正确表示该反应中能量变化的是_______ 。
从断键和成键的角度分析上述反应中能量的变化,化学键的键能如表所示。
反应2H2(g)+O2(g)=2H2O(g)的ΔH=_______ kJ/mol。生成1 mol H2O(g)可以放出热量是_______ kJ。
(2)下列反应中,属于放热反应的是_______ ,属于吸热反应的是_______ 。
a.盐酸与烧碱溶液反应
b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
(1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知该反应为放热反应,如图能正确表示该反应中能量变化的是

从断键和成键的角度分析上述反应中能量的变化,化学键的键能如表所示。
| 化学键 | H—H | O=O | H—O |
| 键能(kJ/mol) | 436 | 496 | 463 |
反应2H2(g)+O2(g)=2H2O(g)的ΔH=
(2)下列反应中,属于放热反应的是
a.盐酸与烧碱溶液反应
b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水
d.高温煅烧石灰石使其分解
e.铝和盐酸反应
您最近一年使用:0次
【推荐2】我国成功发射的“天宫一号”飞行器的外壳覆盖了一种新型结构陶瓷材料,其主要成分是氮化硅,该陶瓷材料可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得:3SiO2+6C+2N2 Si3N4+6CO,该反应变化过程中的能量变化如图所示。回答以下问题:
Si3N4+6CO,该反应变化过程中的能量变化如图所示。回答以下问题:
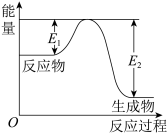
(1)上述反应中的还原剂是___________ ,还原产物是___________ 。
(2)该反应___________ (填“吸热”或“放热”)。
 Si3N4+6CO,该反应变化过程中的能量变化如图所示。回答以下问题:
Si3N4+6CO,该反应变化过程中的能量变化如图所示。回答以下问题:
(1)上述反应中的还原剂是
(2)该反应
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】合金贮氢材料具有优异的吸收氢性能,在配合氢能的开发中起到重要作用。贮氢合金ThNi5可催化由CO、H2合成CH4的反应,温度为T时,该反应的热化学方程式为_________ 。已知温度为T时:CH4(g)+2H2O=CO2(g)+4H2(g) △H=+165kJ•mol-1;CO(g)+H2O(g)=CO2(g)+H2(g) △H=-41 kJ•mol-1
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知: ①CaO(s)+H2O(l)=Ca(OH)2(s) ΔH1=-65.17 kJ·mol-1
②Ca(OH)2(s)=Ca2+(aq)+2OH-(aq) ΔH2=-16.73 kJ·mol-1
③Al(s)+OH-(aq)+3H2O(l)=[Al(OH)4]-(aq)+ H2(g) ΔH3=-415.0 kJ·mol-1
H2(g) ΔH3=-415.0 kJ·mol-1
则CaO(s)+2Al(s)+7H2O(l)=Ca2+(aq)+2[Al(OH)4]-(aq)+3H2(g)的ΔH4=_______ kJ·mol-1
②Ca(OH)2(s)=Ca2+(aq)+2OH-(aq) ΔH2=-16.73 kJ·mol-1
③Al(s)+OH-(aq)+3H2O(l)=[Al(OH)4]-(aq)+
 H2(g) ΔH3=-415.0 kJ·mol-1
H2(g) ΔH3=-415.0 kJ·mol-1则CaO(s)+2Al(s)+7H2O(l)=Ca2+(aq)+2[Al(OH)4]-(aq)+3H2(g)的ΔH4=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】将氯碱工业与燃料电池联合能够有效降低能源消耗,如图是该工艺的图示(电源及电极未标出),请回答下列问题。

(1)电解饱和食盐水(氯碱工业)的化学方程式为_____________________________ 。
(2)物质X为______________ ,装置Ⅰ和Ⅱ中属于燃料电池的是______________ 。
(3)装置Ⅰ中,NaOH溶液浓度m%_________ 填“>”或“<”)n%。
(4)利用装置Ⅱ可获得10mol/L盐酸,该产品出口为______________________ 填“A”或“B”)。

(1)电解饱和食盐水(氯碱工业)的化学方程式为
(2)物质X为
(3)装置Ⅰ中,NaOH溶液浓度m%
(4)利用装置Ⅱ可获得10mol/L盐酸,该产品出口为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】实验室用石墨电极电解加有酚酞的饱和NaCl溶液,装置如图1所示。氯碱工业用图2所示装置制备NaOH等工业原料。

Ⅰ.实验室电解饱和食盐水(图1)
(1)a处的电极反应式为_______ 。
(2)观察到的实验现象是_______ 。
(3)该电解池中发生的总反应的离子方程式为_______ 。
(4)下列与电解饱和食盐水有关的说法,正确的是_______ (填字母)。
A.通电使NaCl发生电离
B.在溶液中,阴离子向电极a移动
C.电解熔融NaCl与电解NaCl溶液所得产物相同
Ⅱ.氯碱工业(图2)
(5)利用实验室装置制备NaOH,不仅有安全隐患,而且存在 与NaOH的副反应,氯碱工业采用改进后的装置,如图2所示。
与NaOH的副反应,氯碱工业采用改进后的装置,如图2所示。
①气体X和气体Y被阳离子交换膜分隔开,避免混合爆炸。气体Y是_______ 。
②阳离子交换膜避免了 与NaOH发生反应,可得到NaOH浓溶液,简述NaOH浓溶液的生成过程
与NaOH发生反应,可得到NaOH浓溶液,简述NaOH浓溶液的生成过程_______ 。

Ⅰ.实验室电解饱和食盐水(图1)
(1)a处的电极反应式为
(2)观察到的实验现象是
(3)该电解池中发生的总反应的离子方程式为
(4)下列与电解饱和食盐水有关的说法,正确的是
A.通电使NaCl发生电离
B.在溶液中,阴离子向电极a移动
C.电解熔融NaCl与电解NaCl溶液所得产物相同
Ⅱ.氯碱工业(图2)
(5)利用实验室装置制备NaOH,不仅有安全隐患,而且存在
 与NaOH的副反应,氯碱工业采用改进后的装置,如图2所示。
与NaOH的副反应,氯碱工业采用改进后的装置,如图2所示。①气体X和气体Y被阳离子交换膜分隔开,避免混合爆炸。气体Y是
②阳离子交换膜避免了
 与NaOH发生反应,可得到NaOH浓溶液,简述NaOH浓溶液的生成过程
与NaOH发生反应,可得到NaOH浓溶液,简述NaOH浓溶液的生成过程
您最近一年使用:0次

 转化为乙烯,工作原理如图所示。
转化为乙烯,工作原理如图所示。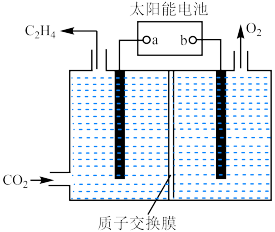
 为太阳能电池的
为太阳能电池的 的移动方向是
的移动方向是

