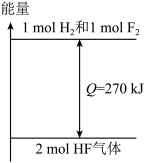
氢气和氟气反应生成氟化氢的过程中能量变化如图所示。由图可知

A.生成 气体要吸收的热量为 气体要吸收的热量为 |
B.热化学方程式为: ∆H=-270kJ/mol ∆H=-270kJ/mol |
| C.该反应是放热反应 |
| D.反应物的总能量小于生成物的总能量 |
更新时间:2020-07-29 10:27:47
|
相似题推荐
单选题
|
容易
(0.94)
【推荐1】下列反应中生成物总能量高于反应物总能量的是
| A.乙醇燃烧 | B.碳酸氢钠和盐酸反应 | C.镁与稀硫酸反应 | D.钠和水反应 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】对于反应中的能量变化,表述正确的是( )
| A.氧化反应均为吸热反应 |
| B.断开化学键的过程会放出能量 |
| C.吸热反应中,反应物的总能量大于生成物的总能量 |
| D.放热反应中,反应物的总能量大于生成物的总能量 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐1】BeCl2是有机反应的催化剂。铍和氯气反应的能量变化如图所示。下列说法正确的是( )


| A.E2是正反应的活化能 | B.该反应的ΔH<0 |
| C.加入催化剂,ΔH减小 | D.ΔH = E2 - E1 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】下列说法正确的是
| A.焓变单位是kJ•mol−1,是指1 mol物质参加反应时的能量变化 |
| B.当反应放热时ΔH>0,反应吸热时ΔH<0 |
| C.一个化学反应中,当反应物的总能量大于生成物的总能量时,反应放热,ΔH为“−” |
| D.一个化学反应中,生成物总键能大于反应物的总键能时,反应吸热,ΔH为“+” |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】将TiO2转化为TiCl4是工业冶炼金属Ti的主要反应之一。已知:
TiO2(s)+2Cl2(g)=TiCl4(1)+O2(g) ∆H=+140.5kJ/mol
2CO(g)=2C(s,石墨)+O2(g) ∆H=+221.0 kJ/mol
则反应TiO2(s)+2Cl2(g)+2C(s,石墨)=TiCl4(1)+2CO(g)的∆H为
TiO2(s)+2Cl2(g)=TiCl4(1)+O2(g) ∆H=+140.5kJ/mol
2CO(g)=2C(s,石墨)+O2(g) ∆H=+221.0 kJ/mol
则反应TiO2(s)+2Cl2(g)+2C(s,石墨)=TiCl4(1)+2CO(g)的∆H为
| A.-30.0kJ/mol | B.+30.0 kJ/mol | C.-80.5kJ/mol | D.+80.5kJ/mol |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐2】已知T℃时,CaCO3(s)=CaO(s)+CO2(g) △H=+177.70kJ·mol-1,则每生成28gCaO(s)时,吸收的热量为
| A.44.43KJ | B.88.85KJ | C.133.28KJ | D.177.70kJ |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐1】已知H—H键的键能是436.4 kJ.mol-1, Cl—Cl 键的键能是242.7 kJ.mol-1,H—Cl键的键能是431.8 kJ.mol-1 。则H2(g)+ Cl 2(g)=2H Cl(g)的反应热是:
| A.-184.5kJ/mol | B.+184.5kJ/mol |
| C.+247.3 kJ/mol | D.-247.3 kJ/mol |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐2】已知热化学方程式N2(g)+3H2(g)=2NH3(g) ΔH=-92kJ·mol-1。若断开1mol H-H键吸收的能量为436kJ,形成1mol H-N键释放的能量为391kJ,则断开1mol N≡N键须
| A.吸收946kJ能量 | B.放出946kJ能量 | C.放出618kJ能量 | D.吸收618kJ能量 |
您最近一年使用:0次

 2SO3(g)
2SO3(g) 

