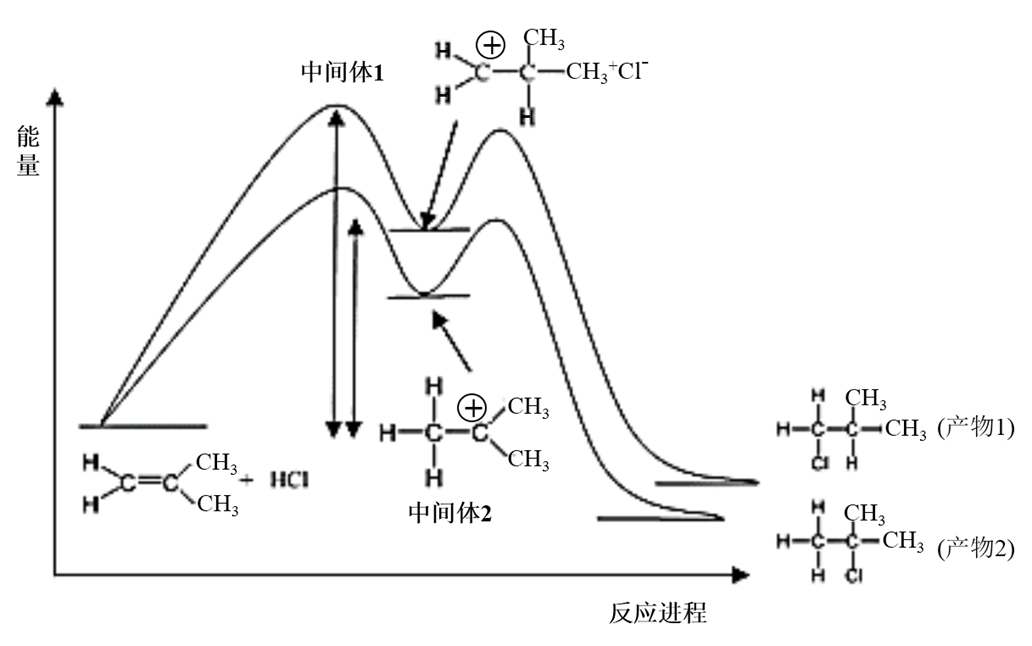
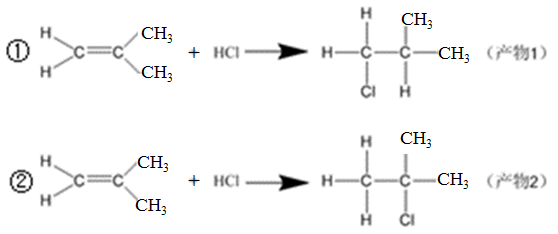
一定条件下,三个基元反应的正反应活化能[Ea(正)]和逆反应活化能[Ea(逆)]如表:
正反应为放热反应的是
| 基元反应 | Ea(正)(kJ•mol-1) | Ea(逆)(kJ•mol-1) |
| I | 30 | 55 |
| II | 70 | 21 |
| III | 16 | 35 |
| A.I、II | B.I、III | C.II、III | D.II |
更新时间:2023-02-11 11:09:52
|
相似题推荐
单选题
|
容易
(0.94)
名校
【推荐1】某反应的反应过程中能量变化如图所示,下列叙述不正确的是:
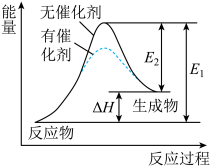

| A.催化剂能改变反应的焓变 | B.催化剂能降低反应所需活化能 |
| C.该反应是吸热反应 | D.逆反应的活化能小于正反应的活化能 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐2】下列说法错误的是
| A.化学反应中的能量变化都表现为热量变化 |
| B.需要加热才能发生的反应不一定是吸热反应 |
| C.向醋酸钠溶液中滴入酚酞试液,加热后若溶液红色加深,则说明盐类水解是吸热的 |
| D.反应物和生成物所具有的总能量决定了反应是放热还是吸热 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】下列关于有效碰撞理论与影响速率因素之间关系正确的是( )
| A.增大反应物浓度,可以提高活化分子百分数,从而提高反应速率 |
| B.对于气体反应来说,通过压缩体积增大压强,可以提高单位体积内活化分子数,从而提高反应速率 |
| C.活化分子之间发生的碰撞一定为有效碰撞 |
| D.加入催化剂可以降低活化能,活化分子百分比虽然没变,但可以加快反应速率 |
您最近一年使用:0次
单选题
|
容易
(0.94)
解题方法
【推荐2】下列说法正确的是
| A.减小反应物浓度,可减小反应物分子中的活化分子百分数,使有效碰撞次数减小 |
| B.升高温度能使化学反应速率增大,原因是增加了反应物分子中活化分子的百分数 |
| C.有气体参加的化学反应,若增大压强(即缩小反应容器的容积),可增加活化分子的百分数,从而使反应速率增大 |
| D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率 |
您最近一年使用:0次