实验一:以二氧化锰作催化剂,进行以下四组实验。
第1组:粉末状的二氧化锰0.2g+5mL6%H2O2
第2组:粉末状的二氧化锰0.2g+5mL10%H2O2
第3组:粉末状的二氧化锰0.1g+5mL6%H2O2
第4组:颗粒状的二氧化锰0.1g+5mL6%H2O2
| 催化剂:MnO2 | 0.2g粉末状的MnO2+5mL6%H2O2 | 0.2g粉末状的MnO2+5mL10%H2O2 | 0.1g粉末状的MnO2+5mL6%H2O2 | 0.1g颗粒状的MnO2+5mL6%H2O2 |
| 前15s产生O2(mL) | 11 | 15 | 8 | 7 |
| 前30s产生O2(mL) | 21 | 24 | 11 | 9 |
| 前45s产生O2(mL) | 31 | 35 | 18 | 12 |
| 前60s产生O2(mL) | 45 | 48 | 26 | 15 |
实验二:以不同的催化剂对过氧化氢(均为5mL6%H2O2)分解反应速率影响进行研究,记录反应的时间t和相应的量筒内的气体体积读数V,用
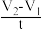 t作为反应速率的表达式(单位:mL•s﹣1),得到以下实验数据:
t作为反应速率的表达式(单位:mL•s﹣1),得到以下实验数据:| 催化剂 | 产生气体速率/mL•s﹣1 | 催化剂 | 产生气体速率/mL•s﹣1 |
| MnO2 | 0.03 | 土豆 | 0.03 |
| CuO | 0.07 | 活性炭 | 0.12 |
(1)写出实验一中H2O2分解的反应方程式
(2)实验一的几组数据能够说明在实验中影响反应速率的因素主要有
(3)实验二的几组数据反映出的问题是
(4)用碰撞理论解释使用正催化剂能增大化学反应速率的原因
相似题推荐
现有以下实验记录:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| 温度/℃ | 30 | 40 | 50 | 60 | 70 |
| 显色时间/s | 160 | 80 | 40 | 20 | 10 |
回答下列问题:
(1)该反应的离子方程式为
(2)该实验的目的是
(3)实验试剂除了1mol/LKI溶液、0.1mol/LH2SO4溶液外,还需要的试剂是
(4)上述实验操作中除了需要(3)的条件外,还必须控制不变的是
A.温度
B.试剂的浓度
C.试剂的用量(体积)
D.试剂添加的顺序
(5)由上述实验记录可得出的结论是
Ⅰ.某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”, 回答下面问题:
(1)发生反应的离子方程式为:
(2)已知随着反应进行试管的温度升高,化学反应速率与时间的关系如图:

时间t1以前反应速率缓慢增大的原因是
(3)某同学探究“外界条件改变对化学反应速率的影响”进行了如下实验:
| 实验序号 | 实验温度/K | 参加反应的物质 | ||||
| KMnO4溶液(含硫酸) | H2C2O4溶液 | H2O | ||||
| V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | ||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 |
| B | T1 | 2 | 0.02 | 3 | 0.1 | V1 |
| C | 313 | 2 | 0.02 | V2 | 0.1 | V3 |
②该实验配合使用计时器,通过测定
③某同学在设计“验证反应物浓度对速率影响”的几组平行实验中,保持H2C2O4溶液最终浓度不变,把KMnO4溶液的最终浓度设计为变量,该实验设计是否合理:
Ⅱ. 高锰酸钾还常用于亚硝酸盐的测定。欲测定某样品中NaNO2的含量,某同学设计如下实验:
①称取样品ag,加水溶解,配制成100mL溶液。
②取25.00mL溶液于锥形瓶中,用0.0200mol/LKMnO4标准溶液(酸性)进行滴定,滴定结束后消耗KMnO4溶液V mL。
(1)在进行滴定操作时,KMnO4溶液盛装在
(2)滴定过程中发生反应的离子方程式是
(3)以下操作造成测定结果偏高的是
A.滴定管未用KMnO4标准溶液润洗
B.锥形瓶未用待测液润洗
C.盛装标准溶液的滴定管,滴定前尖端有气泡,滴定后气泡消失
D.盛装标准溶液的滴定管,滴定前仰视凹液面最低处,滴定后俯视读数
E.若滴定过程中刚出现颜色变化就停止滴定
| 序号 | 纯锌粉(g) | 2.0 mol·L-1 硫酸溶液(mL) | 温度(℃) | 硫酸铜固体(g) | 加入蒸馏水(mL) |
| Ⅰ | 2.0 | 50.0 | 25 | 0 | 0 |
| Ⅱ | 2.0 | 40.0 | 25 | 0 | 10.0 |
| Ⅲ | 2.0 | 50.0 | 25 | 0.2 | 0 |
| Ⅳ | 2.0 | 50.0 | 25 | 4.0 | 0 |
②实验Ⅲ和实验Ⅳ的目的是
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验 序号 | 体积V/mL | ||||
| K2S2O8溶液 | 水 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| ② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
| ③ | 8.0 | Vx | 4.0 | 4.0 | 2.0 |
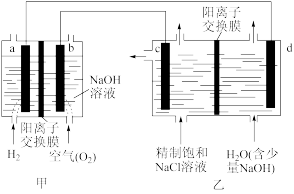
(1)写出b电极的电极反应式
(2)写出乙装置发生的总化学方程式
(3)若放电一段时间后,消耗空气22.4L(标况),不考虑损耗的情况下,乙池产生的气体
(4)下列说法正确的是
A.甲装置可以实现化学能向电能转化
B.甲装置中Na+透过阳离子交换膜向a极移动
C.乙装置中c极一侧流出的是淡盐水
Ⅱ.二氧化碳催化加氢也可合成甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH。在密闭容器中投入1mol CO2和2.75mol H2,在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示。
CH3OH(g)+H2O(g) ΔH。在密闭容器中投入1mol CO2和2.75mol H2,在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示。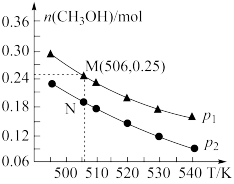
(5)二氧化碳合成甲醇正反应的ΔH
(6)一定条件下,向容积不变的某密闭容器中加入a mol CO2和b mol H2发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),欲使整个反应过程中CO2的体积分数为恒定值,则a与b的大小关系式是
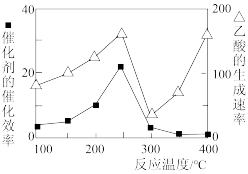
CH3OH(g)+H2O(g),欲使整个反应过程中CO2的体积分数为恒定值,则a与b的大小关系式是(7)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图所示。当乙酸的生成速率主要取决于温度时,其影响范围是
Ⅰ.焦炭催化还原
 生成
生成 的化学反应方程式为
的化学反应方程式为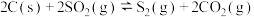 ,向1L的容密闭容器中加入2
,向1L的容密闭容器中加入2 C和1
C和1
 反应,
反应, 的转化率随温度的变化如图所示。
的转化率随温度的变化如图所示。
(1)700℃时,
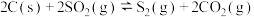 的平衡常数是
的平衡常数是(2)温度大于700℃后,
 的转化率降低的原因是
的转化率降低的原因是(3)下列有关说法正确的是_____。
A.将容器的体积缩小至0.5L,达到平衡时 的转化率增大 的转化率增大 |
B.当容器内 的浓度不在发生变化时,该反应达到平衡状态 的浓度不在发生变化时,该反应达到平衡状态 |
| C.向容器内加入一定量的焦炭,化学反应速率增大 |
| D.当容器内的气体的平均摩尔质量不变时,该反应达到平衡状态 |
Ⅱ.碘离子可以作为水溶液中
 歧化反应的催化剂,可能的催化过程如下。
歧化反应的催化剂,可能的催化过程如下。i.
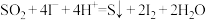
ii.
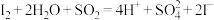
探究i、ii反应速率与
 歧化反应速率的关系,实验如下:分别将18
歧化反应速率的关系,实验如下:分别将18
 饱和溶液加入到2
饱和溶液加入到2 下列试剂中,密闭放置观察现象。(已知:
下列试剂中,密闭放置观察现象。(已知: 易溶解在
易溶解在 溶液中)
溶液中)| 序号 | A | B | C | D |
| 试剂组成 | X  | 0.4  0.2   | Y  | 0.2  0.0002   |
| 实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
(4)水溶液中
 歧化反应方程式是:
歧化反应方程式是:(5)A、B、C互为对比实验,则


(6)根据以上实验可知水溶液中
 歧化反应的速率主要由反应
歧化反应的速率主要由反应【推荐3】对H2O2的分解速率影响因素进行研究。
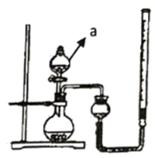
(1) A组为研究催化剂FeCl3的量对O2生成速率的影响,设计了如下三组实验方案(见下表),将表中所给的试剂按一定体积混合后进行反应。
| A | B | C |
10%H2O2/mL | 20.0 | V1 | V2 |
2 mol/LFeCl3/mL | 0 | 5.0 | 10.0 |
H2O/mL | V3 | V4 | 0 |
按要求回答下列问题:
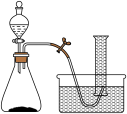
①a装置的名称为
②若读数时发现,量气装置左端液面低于右端液面,则测得的气体体积
(2) B组在相同的温度下,利用下图甲装置对H2O2在不同条件下的分解速率进行了探究,得到乙曲线:
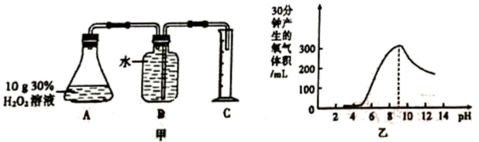
则B小组探究的是
(3)C小组利用如下装置探究100℃,H2O2在不同离子催化作用下反应24h的分解率,

实验编号 | 离子 | 加入量/(mg/L) | 分解率/% |
① | 无 | — | 2 |
② | Al3+ | 1.0 | 2 |
③ | Fe3+ | 1.0 | 15 |
④ | Cu2+ | 0.1 | 86 |
⑤ | Cr3+ | 0.1 | 96 |
则该小组实验时记录的数据应该是
 2CaSO4+2Cl2↑+2H2O,他们设计如下装置制取氯气并验证其性质。请回答下列问题:
2CaSO4+2Cl2↑+2H2O,他们设计如下装置制取氯气并验证其性质。请回答下列问题:
(1)漂白粉的有效成分是
(2)该实验中A部分的装置是
(3)装置B中的实验现象是
(4)实验结束时发现装置D中有色布条并没有褪色,此时取下E装置,加入少量蒸馏水,塞紧塞子振荡,有色布条褪色,写出有色布条褪色的原因是:
(5)装置E作用是吸收尾气,写出该反应的离子方程式
I.CuSO4溶液的制备
①取4g铜粉,在仪器A中灼烧10分钟并不断搅拌使其充分反应。
②将A中冷却后的固体转移到烧杯中,加入25 mL 3 mol·L-1H2SO4溶液,加热并不断搅拌至固体完全溶解。
(1)①中仪器A的名称为
(2)②中发生反应的离子方程式为
Ⅱ.晶体的制备
将I中制备的CuSO4溶液按如图所示进行操作:
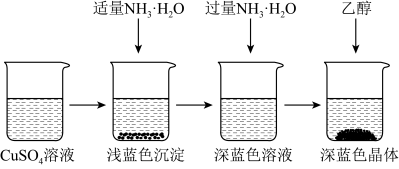
(3)向硫酸铜溶液中逐滴加入氨水至过量的过程中,可观察到的实验现象是
(4)缓慢加入乙醇会析出晶体的原因是
III.氨含量的测定
精确称取wg晶体,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用盐酸标准溶液完全吸收。取下接收瓶,再用NaOH标准溶液滴定剩余的盐酸溶液(选用甲基橙作指示剂)。
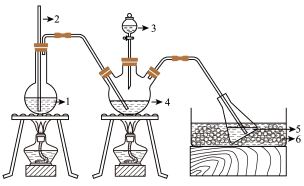
1.水 2.玻璃管 3.10%氢氧化钠溶液 4.样品液 5.盐酸标准溶液 6.冰盐水
(5)装置中玻璃管的作用是
(6)在实验装置中,若没有使用冰盐水冷却会使氨含量测定结果
(1)甲组同学利用CaSO4·2H2O 在400--500℃脱水制取无水CaSO4 。实验中需用到的加热装置中的硅酸盐质的仪器除玻璃棒外,还用到
(2)乙组同学利用H2C2O4 ·2H2O 在浓硫酸作用下脱水生成CO、CO2并制备纯净的CO气体,实验装置如下:
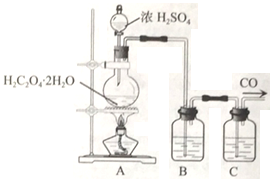
B、C中盛放的试剂依次为
(3)丙组同学利用甲组制得的无水CaSO4和乙组制得的CO 并利用下列装置验证反应并检验气态产物中有SO2 和CO2产生。

①上述装置(部分装置可重复使用)的连接顺序为C→
②若E溶液褪色,则发生反应的离子方程式为
③能证明有CO2的生成的实验依据是
④若G中产物为CaO,则G中发生反应的化学方程式为
(4)丁组的同学取丙组实验后G装置中的固体产物加入试管中,然后加入足量稀盐酸,固体完全溶液且产生少量气体,通入CuSO4溶液有黑色沉淀。可验证CO 与CaSO4在高温下还发生了一个副反应,该反应为




