下表是元素周期表的一部分。回答下列问题:
(1)元素①~⑩中,金属性最强的元素的原子结构示意图为__________ 。
(2)写出元素②常见的一种同素异形体的名称:____________ 。
(3)元素⑦的单质与元素⑧氢化物的水溶液反应的离子方程式为___________ 。
(4)元素⑥的最高价氧化物对应的水化物的电子式为_________ ,元素⑩的单质的氧化性比元素⑤的单质的氧化性__________ (填“强”或“弱”)。
(5)元素④、⑧可组成多种微粒,其中可作为饮用水消毒剂的化合物分子是________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ||||||||||||||
| ⑥ | ⑦ | ⑧ | |||||||||||||||
| ⑨ | ⑩ |
(1)元素①~⑩中,金属性最强的元素的原子结构示意图为
(2)写出元素②常见的一种同素异形体的名称:
(3)元素⑦的单质与元素⑧氢化物的水溶液反应的离子方程式为
(4)元素⑥的最高价氧化物对应的水化物的电子式为
(5)元素④、⑧可组成多种微粒,其中可作为饮用水消毒剂的化合物分子是
更新时间:2020-08-06 10:08:04
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】随原子序数的递增,八种短周期元素(用字母表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。根据判断出的元素回答问题:
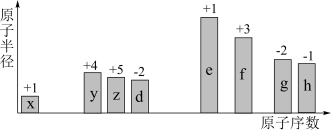
(1)f在元素周期表的位置是_______ 。
(2)上述元素形成的简单阴、阳离子中,离子半径最大的是(用化学式表示,下同)_______________ ;在e、f、g、h四种元素的最高价氧化物对应的水化物中的酸性最强的是___________________ 。
(3)d、e能形成原子个数比为1:1的化合物,该化合物的电子式为________________ ,0.1 mol该化合物与足量水反应时转移的电子数为____________ 。

(1)f在元素周期表的位置是
(2)上述元素形成的简单阴、阳离子中,离子半径最大的是(用化学式表示,下同)
(3)d、e能形成原子个数比为1:1的化合物,该化合物的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在构成宇宙万物的一百多种元素中,金属约占了80%,它们在现代工业和新材料、新技术研究中具有至关重要的意义。现有a、b、c、d四种金属元素,a是人体内含量最多的金属元素,b是地壳中含量最多的金属元素,c是海水中含量最多的金属元素,d是人类冶炼最多的金属元素。
(1)元素a在元素周期表中的位置为______ ;a原子的核外能量不同的电子有____ 种。
(2)下列可以证明b、c金属性强弱的是_____ 。
A.最高价氧化物对应水化物的溶解性:b<c
B.单质与水反应的剧烈程度:b<c
C.相同条件下,氯化物水溶液的pH值:b<c
D.c可以从b的氯化物水溶液中置换出b
(3)人类冶炼d的时候一般得到的是d的合金,潮湿环境中其表面会产生一层水膜,从而发生腐蚀。下列关于该腐蚀的说法正确的是_____ 。
A.腐蚀过程中,一定会有气体放出
B.腐蚀过程中,水膜的碱性会增强
C.在酸性条件下,负极的电极反应式为:2H++2e-=H2↑
D.与电源的负极相连,可以防止发生这种腐蚀
(4)d单质在高温下会与水蒸气反应生成一种黑色固体和一种易燃性气体,且每生成1 mol该易燃气体放出37.68 kJ热量,请写出此反应的热化学方程式:_____________ 。
(1)元素a在元素周期表中的位置为
(2)下列可以证明b、c金属性强弱的是
A.最高价氧化物对应水化物的溶解性:b<c
B.单质与水反应的剧烈程度:b<c
C.相同条件下,氯化物水溶液的pH值:b<c
D.c可以从b的氯化物水溶液中置换出b
(3)人类冶炼d的时候一般得到的是d的合金,潮湿环境中其表面会产生一层水膜,从而发生腐蚀。下列关于该腐蚀的说法正确的是
A.腐蚀过程中,一定会有气体放出
B.腐蚀过程中,水膜的碱性会增强
C.在酸性条件下,负极的电极反应式为:2H++2e-=H2↑
D.与电源的负极相连,可以防止发生这种腐蚀
(4)d单质在高温下会与水蒸气反应生成一种黑色固体和一种易燃性气体,且每生成1 mol该易燃气体放出37.68 kJ热量,请写出此反应的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白(填写序号不得分):
(1)⑦元素的离子半径__ S2-(填“>”或“<”),比较③与⑥的氢化物,___ 更稳定(填化学式),最不活泼的元素是___ (填元素符号)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是____ ,碱性最强的化合物的化学式是:_____ 。
(3)比较①与⑤的最高价氧化物对应的水化物,_____ 的酸性强(填化学式),能证明两者酸性强弱的离子反应方程式为______
(4)实验室制取②的氢化物的化学方程式________
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(1)⑦元素的离子半径
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)比较①与⑤的最高价氧化物对应的水化物,
(4)实验室制取②的氢化物的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列问题:
(1)④、⑥、⑦的离子半径由大到小的顺序为___________ 。
(2)1971年美国科学家通过细冰获得含元素④的含氧酸(HXO),在与水反应时,两种分子中的共价键分别断裂成两部分,再重新组合,写出该反应的化学方程式___________ 。
(3)①、②两种元素的原子按1:1组成的常见液态化合物的电子式为________ 。在酸性溶液中该物质能将Fe2+氧化,写出该反应的离子方程式___________ 。
(4)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气
体,D溶液显碱性。
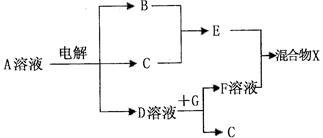
①写出D溶液与G反应的化学方程式_________________________________ 。
②常温下,若电解l L 0.1 mol/L A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为________ mol。
③若仅电解l L 0.1 mol/L A溶液,图中各步反应均为完全转化,而各物质在反应过程中没有损耗,则混合物X中含有的物质有_______________ 。
| ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ④ | ||||||
| 3 | ⑤ | ③ | ⑥ | ⑦ | ||||
(1)④、⑥、⑦的离子半径由大到小的顺序为
(2)1971年美国科学家通过细冰获得含元素④的含氧酸(HXO),在与水反应时,两种分子中的共价键分别断裂成两部分,再重新组合,写出该反应的化学方程式
(3)①、②两种元素的原子按1:1组成的常见液态化合物的电子式为
(4)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气
体,D溶液显碱性。

①写出D溶液与G反应的化学方程式
②常温下,若电解l L 0.1 mol/L A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为
③若仅电解l L 0.1 mol/L A溶液,图中各步反应均为完全转化,而各物质在反应过程中没有损耗,则混合物X中含有的物质有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】为人们寻找_______ 提供了科学的途径:
(1)在ⅠA族可以找到制造_______ 材料的元素;
(2)在ⅢA、ⅣA、ⅤA族可以找到制造优良的_______ 材料的元素。
(1)在ⅠA族可以找到制造
(2)在ⅢA、ⅣA、ⅤA族可以找到制造优良的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下面是元素周期表的一部分,参照元素①~⑧在表中的位置。
请用化学用语回答下列问题:
(1)④、⑤、⑦的原子半径由大到小的顺序为(元素符号)___________________ 。
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是(填化学式)_____________ 。
(3)在①、④、⑤、⑧中的某些元素之间可形成既含离子键又含非极性共价键的离子化合物,写出其中一种化合物的电子式:_____________________ 。
(4)由②最高价氧化物与⑤的同周期相邻主族元素的单质反应的化学方程式为:___________________________ 。
(5)②单质与③的最高价氧化物的水化物的浓溶液反应的离子方程式为______________________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
请用化学用语回答下列问题:
(1)④、⑤、⑦的原子半径由大到小的顺序为(元素符号)
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是(填化学式)
(3)在①、④、⑤、⑧中的某些元素之间可形成既含离子键又含非极性共价键的离子化合物,写出其中一种化合物的电子式:
(4)由②最高价氧化物与⑤的同周期相邻主族元素的单质反应的化学方程式为:
(5)②单质与③的最高价氧化物的水化物的浓溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】根据题意填空:
(1)表中是几种短周期元素的原子半径及主要化合价。
则L元素的名称是_____ ,R元素在周期表中的位置为_____ 。
(2)某种融雪剂的主要成分为XY2,且X、Y均为周期表中前20号元素。XY2中阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子,则该融雪剂主要成分的电子式为_____ 。
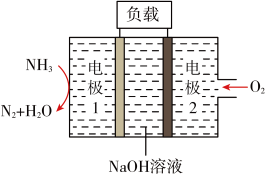
(3)瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池如图所示,该燃料电池工作时,负极的电极反应式为_____ ;电池的总反应为_____ 。
(1)表中是几种短周期元素的原子半径及主要化合价。
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.111 | 0.106 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
则L元素的名称是
(2)某种融雪剂的主要成分为XY2,且X、Y均为周期表中前20号元素。XY2中阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子,则该融雪剂主要成分的电子式为
(3)瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池如图所示,该燃料电池工作时,负极的电极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下面是元素周期表的一部分。
根据以上元素在周期表中的位置,用元素符号或化学式填写空白。
(1)非金属性最强的元素是_____________ ;化学性质最不活泼的是__________ ;除L外,原子半径最大的是____________ 。
(2)写出B、G两种元素的最高价氧化物对应水化物的化学式 :________ 、_______ 。
(3)形成化合物种类最多的元素是_____________________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 一 | A | |||||||
| 二 | F | D | J | L | ||||
| 三 | B | C | E | G |
根据以上元素在周期表中的位置,用元素符号或化学式填写空白。
(1)非金属性最强的元素是
(2)写出B、G两种元素的最高价氧化物对应水化物的
(3)形成化合物种类最多的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】元素周期律是指导我们学习元素及其化合物知识的重要工具。已知氧族元素(不含Po)的部分知识如下表所示。
回答下列问题:
(1)硫元素在元素周期表中位置是_______ ,硒原子最外层电子数为_______ 。
(2)依据元素周期律和表中知识,预测单质硒的熔点范围_______ ℃<硒<_______ ℃,元素碲的主要化合价可能有_______ 。
(3)从物质类别和硫元素的价态分析,在一定条件下,SO2能与下列物质发生反应,在横线上写出反应产物中含硫物质的化学式:①NaOH溶液_______ ,②H2S_______ ,③Na2O2_______ 。
(4)已知硒最高价氧化物对应的硒酸是强酸,写出能证明硒酸比碳酸强的离子方程式:_______ 。
(5)氢硒酸(H2Se)有较强的还原性,因此露置在空气中长期保存易变质出现浑浊,可能发生反应的化学方程式为_______ 。
| 氧族元素 | 8O(氧) | 16S(硫) | 34Se(硒) | 52Te(碲) |
| 单质熔点/℃ | -218.4 | 113 | 450 | |
| 单质沸点/℃ | -183 | 444.6 | 685 | 1390 |
| 元素主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 |
回答下列问题:
(1)硫元素在元素周期表中位置是
(2)依据元素周期律和表中知识,预测单质硒的熔点范围
(3)从物质类别和硫元素的价态分析,在一定条件下,SO2能与下列物质发生反应,在横线上写出反应产物中含硫物质的化学式:①NaOH溶液
(4)已知硒最高价氧化物对应的硒酸是强酸,写出能证明硒酸比碳酸强的离子方程式:
(5)氢硒酸(H2Se)有较强的还原性,因此露置在空气中长期保存易变质出现浑浊,可能发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】利用物质的结构与性质对周期表进行研究,有助于我们更好地掌握同类知识。
Ⅰ.2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(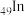 )等9种元素相对原子质量的新值,被采用为国际新标准。
)等9种元素相对原子质量的新值,被采用为国际新标准。
(1) 在周期表中的位置是
在周期表中的位置是___________ 。
(2) 的最高价氧化物对应的水化物的碱性
的最高价氧化物对应的水化物的碱性___________  的碱性(填“>”或“<”)。
的碱性(填“>”或“<”)。
(3) 的中子数与电子数的差值为
的中子数与电子数的差值为___________ 。
Ⅱ.硒( )是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。
)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。
(4) 和
和 的最高价氧化物对应水化物的酸性由强到弱的顺序
的最高价氧化物对应水化物的酸性由强到弱的顺序___________ (用化学式表示)。 与足量
与足量 元素的最高价氧化物的水化物反应的化学方程式为
元素的最高价氧化物的水化物反应的化学方程式为___________ 。
(5) 和
和 的气态氢化物的稳定性由强到弱的顺序
的气态氢化物的稳定性由强到弱的顺序___________ (用化学式表示)。
Ⅰ.2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(
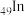 )等9种元素相对原子质量的新值,被采用为国际新标准。
)等9种元素相对原子质量的新值,被采用为国际新标准。(1)
 在周期表中的位置是
在周期表中的位置是(2)
 的最高价氧化物对应的水化物的碱性
的最高价氧化物对应的水化物的碱性 的碱性(填“>”或“<”)。
的碱性(填“>”或“<”)。(3)
 的中子数与电子数的差值为
的中子数与电子数的差值为Ⅱ.硒(
 )是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。
)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。(4)
 和
和 的最高价氧化物对应水化物的酸性由强到弱的顺序
的最高价氧化物对应水化物的酸性由强到弱的顺序 与足量
与足量 元素的最高价氧化物的水化物反应的化学方程式为
元素的最高价氧化物的水化物反应的化学方程式为(5)
 和
和 的气态氢化物的稳定性由强到弱的顺序
的气态氢化物的稳定性由强到弱的顺序
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】短周期主族元素 A、B、C、D、E 的原子序数依次增大。常温下,A、C 组成的化合物是常见液体,B 原子最外层电子数等于次外层电子数的 2 倍,D 与 C 同主族。回答下列问题:
(1) A 的单质的电子式为______ ;B 在元素周期表中的位置为第____ 周期第_____ 族。
(2) B、C 中,原子半径大的是______ (填元素符号);D、E 的简单氢化物中,稳定性较强的是______ (填化学式)。
(3) A、C 组成的原子个数比为 1:1 的化合物常用于制备 C 的单质,反应的化学方程式为_______ 。
(1) A 的单质的电子式为
(2) B、C 中,原子半径大的是
(3) A、C 组成的原子个数比为 1:1 的化合物常用于制备 C 的单质,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】在第三周期元素中,除稀有气体元素外:
(1)最高价氧化物对应水化物碱性最强的是___ ;
(2)氧化物中具有两性的是_____ ;
(3)最高价氧化物对应水化物酸性最强的是_____ (用化学式回答,下同);
(4)最不稳定的气态氢化物是____ ;
(5)原子半径最小的元素是___ (填元素符号);
(6)金属性最强的元素是____ (填元素符号) 。
(1)最高价氧化物对应水化物碱性最强的是
(2)氧化物中具有两性的是
(3)最高价氧化物对应水化物酸性最强的是
(4)最不稳定的气态氢化物是
(5)原子半径最小的元素是
(6)金属性最强的元素是
您最近一年使用:0次



