元素周期律是指导我们学习元素及其化合物知识的重要工具。已知氧族元素(不含Po)的部分知识如下表所示。
回答下列问题:
(1)硫元素在元素周期表中位置是_______ ,硒原子最外层电子数为_______ 。
(2)依据元素周期律和表中知识,预测单质硒的熔点范围_______ ℃<硒<_______ ℃,元素碲的主要化合价可能有_______ 。
(3)从物质类别和硫元素的价态分析,在一定条件下,SO2能与下列物质发生反应,在横线上写出反应产物中含硫物质的化学式:①NaOH溶液_______ ,②H2S_______ ,③Na2O2_______ 。
(4)已知硒最高价氧化物对应的硒酸是强酸,写出能证明硒酸比碳酸强的离子方程式:_______ 。
(5)氢硒酸(H2Se)有较强的还原性,因此露置在空气中长期保存易变质出现浑浊,可能发生反应的化学方程式为_______ 。
| 氧族元素 | 8O(氧) | 16S(硫) | 34Se(硒) | 52Te(碲) |
| 单质熔点/℃ | -218.4 | 113 | 450 | |
| 单质沸点/℃ | -183 | 444.6 | 685 | 1390 |
| 元素主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 |
回答下列问题:
(1)硫元素在元素周期表中位置是
(2)依据元素周期律和表中知识,预测单质硒的熔点范围
(3)从物质类别和硫元素的价态分析,在一定条件下,SO2能与下列物质发生反应,在横线上写出反应产物中含硫物质的化学式:①NaOH溶液
(4)已知硒最高价氧化物对应的硒酸是强酸,写出能证明硒酸比碳酸强的离子方程式:
(5)氢硒酸(H2Se)有较强的还原性,因此露置在空气中长期保存易变质出现浑浊,可能发生反应的化学方程式为
20-21高一下·浙江·阶段练习 查看更多[2]
更新时间:2021-03-26 16:20:39
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下列编号代表元素周期表中的一部分元素,用化学式回答下列问题:
(1)①、③、⑤的最高价氧化物的水化物碱性由强到弱顺序为___________ (填化学式,下同)。
(2)②、③、④形成的简单阳离子半径由大到小的顺序是_______________ 。
(3)⑨和⑩的最高价氧化物对应的水化物化学式为_______ 和_________ 。①在氧气中点燃生成淡黄色的固体,该固体的电子式为_______________ ,①能够与水剧烈反应,请写出该反应的化学方程式_______________ ,将元素⑩的单质通入NaBr溶液中,反应的离子方程式为_______________ 。
(4)⑥、⑦、⑧三种元素形成的气态氢化物的稳定性排序是____________ (填化学式,下同),三种元素非金属性由强到弱的顺序为___________ 。
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ⑦ | ⑧ | |||||
| 三 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 四 | ② | ④ |
(1)①、③、⑤的最高价氧化物的水化物碱性由强到弱顺序为
(2)②、③、④形成的简单阳离子半径由大到小的顺序是
(3)⑨和⑩的最高价氧化物对应的水化物化学式为
(4)⑥、⑦、⑧三种元素形成的气态氢化物的稳定性排序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】稀土元素是周期表中Ⅲ B族钪、钇和镧系元素的总称,它们都是很活泼的金属,性质极为相似,常见化合价为+3。其中钇(Y)元素是激光和超导的重要材料。
我国蕴藏着丰富的钇矿石( Y2 FeBe2Si2O10),以此矿石为原料生产氧化钇(Y2O3)的主要流程如下:

已知:
I.有关金属离子形成氢氧化物沉淀时的pH如下表:
Ⅱ.在周期表中,铍、铝元素处于第二周期和第三周期的对角线位置,化学性质相似。
(1)钇矿石(Y2 FeBe2Si2O10)的组成用氧化物的形式可表示为__________ 。
(2)欲从Na2 SiO3和Na2BeO2的混合溶液中制得Be(OH)2沉淀。则
①最好选用盐酸、_____ (填字母代号)两种试剂,再通过必要的实验操作方可实现。
a.NaOH溶液 b.氨水 c.CO2气 d.HNO3
②写出Na2BeO2与足量盐酸发生反应的离子方程式:_______________ :必要的实验操作应是________________ 。
(3)为使Fe3+沉淀完全,须用氨水调节pH =a,则a应控制在______ 的范围内;继续加氨
水调节pH =b发生反应的离子方程式为_______________ ,溶液中Fe3+完全沉淀的判定标准是__________________ 。
(4)写出草酸钇[Y2(C2O4)3.Nh2O]煅烧的化学方程式______________ 。
我国蕴藏着丰富的钇矿石( Y2 FeBe2Si2O10),以此矿石为原料生产氧化钇(Y2O3)的主要流程如下:

已知:
I.有关金属离子形成氢氧化物沉淀时的pH如下表:
| 开始沉淀时的pH | 完全沉淀时的pH | |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
Ⅱ.在周期表中,铍、铝元素处于第二周期和第三周期的对角线位置,化学性质相似。
(1)钇矿石(Y2 FeBe2Si2O10)的组成用氧化物的形式可表示为
(2)欲从Na2 SiO3和Na2BeO2的混合溶液中制得Be(OH)2沉淀。则
①最好选用盐酸、
a.NaOH溶液 b.氨水 c.CO2气 d.HNO3
②写出Na2BeO2与足量盐酸发生反应的离子方程式:
(3)为使Fe3+沉淀完全,须用氨水调节pH =a,则a应控制在
水调节pH =b发生反应的离子方程式为
(4)写出草酸钇[Y2(C2O4)3.Nh2O]煅烧的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:___________ ,I的最高价氧化物对应水化物的化学式为:___________ 。
(2)根据元素周期律等有关知识,推断:
①阴影部分元素的氢化物沸点最高的是___________ (填化学式)。
②O2-、Al3+、S2-三种离子半径大小顺序:___________ (用离子符号排序)。
(3)已知某主族元素离子结构示意图为 ,其中x-y=12,此元素在元素周期表中的位置为:
,其中x-y=12,此元素在元素周期表中的位置为:___________ 。
(4)卤素互化物(如IBr)与卤素单质性质相似。已知IBr能与水发生非氧化还原反应,写出IBr与水反应的化学方程式:___________ ;IBr中含有的化学键是___________ (填“离子键”、“极性键”或“非极性键”)。

(2)根据元素周期律等有关知识,推断:
①阴影部分元素的氢化物沸点最高的是
②O2-、Al3+、S2-三种离子半径大小顺序:
(3)已知某主族元素离子结构示意图为
 ,其中x-y=12,此元素在元素周期表中的位置为:
,其中x-y=12,此元素在元素周期表中的位置为:(4)卤素互化物(如IBr)与卤素单质性质相似。已知IBr能与水发生非氧化还原反应,写出IBr与水反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】用相应的化学用语回答下列问题
(1)用化学方程式说明实验室不能用带玻璃塞试剂瓶装NaOH溶液的原因_________
(2)用化学方程式说明用氢氟酸雕刻玻璃的原因_________
(3)生产过程中产生的SO2、Cl2等大气污染物,若将二者按照一定比例通入水中可减少或消除污染。写出该反应的离子反应方程式_______ 。
(4)Sr是第5周期第IIA族元素,用离子方程式表示SrCO3与稀盐酸的反应_____
(1)用化学方程式说明实验室不能用带玻璃塞试剂瓶装NaOH溶液的原因
(2)用化学方程式说明用氢氟酸雕刻玻璃的原因
(3)生产过程中产生的SO2、Cl2等大气污染物,若将二者按照一定比例通入水中可减少或消除污染。写出该反应的离子反应方程式
(4)Sr是第5周期第IIA族元素,用离子方程式表示SrCO3与稀盐酸的反应
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。
(1)在光照条件下,氯气和氢气反应过程如下:①Cl2→Cl+Cl ②Cl+H2→HCl+H ③H+Cl2→HCl+Cl ……反应②中形成的化合物的电子式为______ ;反应③中被破坏的化学键属于______ 键(填“极性”或“非极性”)。
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是______ (用元素符号表示)。与氯元素同周期且金属性最强的元素位于周期表的第______ 周期______ 族。
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是______ 。
a.卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深
b.卤化氢的键长按H—F、H—C1、H—Br、H—I的顺序依次减小
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(1)在光照条件下,氯气和氢气反应过程如下:①Cl2→Cl+Cl ②Cl+H2→HCl+H ③H+Cl2→HCl+Cl ……反应②中形成的化合物的电子式为
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是
a.卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深
b.卤化氢的键长按H—F、H—C1、H—Br、H—I的顺序依次减小
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)下列反应中,属于放热反应的_________ ,属于吸热反应的是__________ 填序号)
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的炭 ⑤食物因氧化而腐败 ⑥Ba(OH)2·8H2O与NH4Cl反应 ⑦铁粉与稀盐酸反应
(2)断开1 mol H—H键、1 mol N—H键、1 mol N N分别需要吸收能量为436 kJ、391 k、946kJ,则1 mol H2与足量N2反应生成NH3需
N分别需要吸收能量为436 kJ、391 k、946kJ,则1 mol H2与足量N2反应生成NH3需__________ (填“吸收”或“放出”)能量______ kJ。(认为反应进行到底)。(小数点后保留两位数字)
(3)X、Y两种前20号主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,且X、Y两元素不在相邻的两个周期,则XY2的电子式为:____________ 。
(1)下列反应中,属于放热反应的
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的炭 ⑤食物因氧化而腐败 ⑥Ba(OH)2·8H2O与NH4Cl反应 ⑦铁粉与稀盐酸反应
(2)断开1 mol H—H键、1 mol N—H键、1 mol N
 N分别需要吸收能量为436 kJ、391 k、946kJ,则1 mol H2与足量N2反应生成NH3需
N分别需要吸收能量为436 kJ、391 k、946kJ,则1 mol H2与足量N2反应生成NH3需(3)X、Y两种前20号主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,且X、Y两元素不在相邻的两个周期,则XY2的电子式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,请参照元素①﹣⑩在表中的位置,回答下列问题:
(1)自然界物质种类最多的元素在周期表中的位置是______
(2)⑧⑨⑩的离子半径由大到小的顺序为______ (填化学用语).
(3)写出由⑥、⑧、⑩元素形成的一种离子化合物的电子式______
(4)根据斜线性质相似规则,②的最高价氧化物对应的水化物与盐酸反应的离子方程式____________
(5)③的氧化物,氢氧化物有两性,写出③的单质与⑧的最高价氧化物的水化物反应的化学方程式______
(6)已知W+X=Y+Z,W、X、Y、Z分别是由①⑤⑥三种元素形成的四种十电子粒子,写出该反应的离子方程式______ .
| IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
| 3 | ⑧ | ⑨ | ⑩ |
(1)自然界物质种类最多的元素在周期表中的位置是
(2)⑧⑨⑩的离子半径由大到小的顺序为
(3)写出由⑥、⑧、⑩元素形成的一种离子化合物的电子式
(4)根据斜线性质相似规则,②的最高价氧化物对应的水化物与盐酸反应的离子方程式
(5)③的氧化物,氢氧化物有两性,写出③的单质与⑧的最高价氧化物的水化物反应的化学方程式
(6)已知W+X=Y+Z,W、X、Y、Z分别是由①⑤⑥三种元素形成的四种十电子粒子,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图是元素周期表的一部分,表中列出了八种元素的位置:
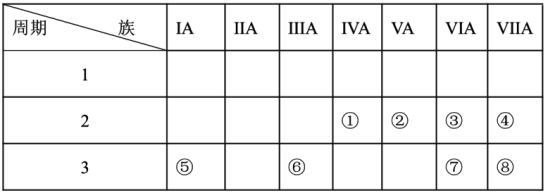
请回答下列问题:
(1)①元素的最简单氢化物的电子式为___________ 。
(2)在元素①-⑧中,金属性最强的元素是___________ (填元素符号);在元素⑤-⑧中,最高价含氧酸酸性最强的是___________ (填化学式)。
(3)③、④、⑤三种元素的原子半径由大到小的顺序是___________ (填元素符号),③和⑦的简单氢化物的稳定性较强的是___________ (填化学式)。
(4)④和⑤所形成的化合物属于___________ (填“离子”或“共价”)化合物。
(5)将等物质的量的①的最简单的氢化物和⑧的单质混合后,在漫射光的照射下充分反应,生成物中物质的量最大的是___________ (写分子式);
(6)⑤和⑥的最高价氧化物对应的水化物之间发生反应的离子方程式为___________ 。

请回答下列问题:
(1)①元素的最简单氢化物的电子式为
(2)在元素①-⑧中,金属性最强的元素是
(3)③、④、⑤三种元素的原子半径由大到小的顺序是
(4)④和⑤所形成的化合物属于
(5)将等物质的量的①的最简单的氢化物和⑧的单质混合后,在漫射光的照射下充分反应,生成物中物质的量最大的是
(6)⑤和⑥的最高价氧化物对应的水化物之间发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】四种短周期元素 W、X、Y、Z,原子序数依次增大,请回答下列问题。
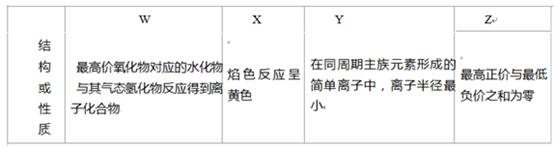
(1)Z 在元素周期表中位于_____ 族。
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他三种物质发生化学 反应,该元素是_____ (填元素符号).
(3)① 下列可作为比较 X 和 Y 金属性强弱的依据是_____ (填序号).
a.自然界中的含量 b.单质与酸反应时失去的电子数
c.单质与水反应的难易程度 d.最高价氧化物对应水化物的碱性
② 从原子结构的角度解释 X 的金属性强于 Y 的原因:_____ ,原子半径 X>Y,所以原子核 对最外层电子的吸引力 X失电子能力 X>Y.
(4)W 的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与 X 的最高 价氧化物对应的水化物混合,反应的化学方程式是_____ 。
(5)Y 单质和 Mg 组成的混合物是一种焰火原料,某兴趣小组设计如下所示的实验方案,测定混合物中Y的质量分数。

能确定混合物中 Y 的质量分数的数据有_____ (填序号).
a. m、n b. m、y c. n、y

(1)Z 在元素周期表中位于
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他三种物质发生化学 反应,该元素是
(3)① 下列可作为比较 X 和 Y 金属性强弱的依据是
a.自然界中的含量 b.单质与酸反应时失去的电子数
c.单质与水反应的难易程度 d.最高价氧化物对应水化物的碱性
② 从原子结构的角度解释 X 的金属性强于 Y 的原因:
(4)W 的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与 X 的最高 价氧化物对应的水化物混合,反应的化学方程式是
(5)Y 单质和 Mg 组成的混合物是一种焰火原料,某兴趣小组设计如下所示的实验方案,测定混合物中Y的质量分数。

能确定混合物中 Y 的质量分数的数据有
a. m、n b. m、y c. n、y
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知元素A的一价阴离子的电子层结构与氩原子相同,元素B的二价阳离子的电子层结构与氖原子相同。请回答:
(1)元素A离子的结构示意图为___ ,A的单质呈___ 色,检验该物质的方法是___ 。
(2)由A、B形成的化合物的电子式是___ 。
(3)与A离子具有相同电子数的一种分子是___ (填名称)。
(4)A的单质与Ca(OH)2反应的化学方程式___ ,该反应工业上的用途是___ 。
(5)蓝色石蕊试纸遇到A的水溶液现象是___ ,请你解释这个现象___ 。
(1)元素A离子的结构示意图为
(2)由A、B形成的化合物的电子式是
(3)与A离子具有相同电子数的一种分子是
(4)A的单质与Ca(OH)2反应的化学方程式
(5)蓝色石蕊试纸遇到A的水溶液现象是
您最近一年使用:0次




