下列事实不能用元素周期律解释的是( )
| A.与水反应,Cs比Na剧烈 | B.与H2反应,F2比Cl2容易 |
| C.碱性:NaOH>Al(OH)3 | D.酸性:HCl>H2CO3 |
更新时间:2020-08-21 13:19:40
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】短周期主族元素X、Y、Z、W原子序数依次增大,X原子的核外有7个电子,Y在周期表中位于IIA族,Y、Z原子的最外层电子数之和等于W原子的最外层电子数,W的氢化物热稳定性在同周期元素中最强。下列说法正确的是
| A.原子半径:r(X)<r(Y)<r(Z)<r(W) |
| B.元素Y、W的简单离子具有相同的电子层结构 |
| C.Z的最高价氧化物对应水化物的酸性比X的弱 |
| D.X的简单氢化物水溶液酸碱性与W的简单氢化物水溶液酸碱性不同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列关于第ⅦA族元素的叙述正确的是
| A.第ⅦA族元素中F元素的非金属性最强,对应的含氧酸的酸性最强 |
| B.第ⅦA族元素,随着核电荷数增大,氢化物的稳定性增强 |
| C.第ⅦA族元素,随着核电荷数增大,离子半径增大 |
| D.第ⅦA族元素的最高正价均等于其最外层电子数 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】X、Y、Z、W是原子序数依次增大的短周期主族元素,X与W的质子数之和为12且可形成WX型离子化合物,Y、Z同周期相邻且可形成常见的气态化合物,下列说法正确的是
| A.简单离子半径:W>Y>Z | B.X、W均位于IA族 |
| C.简单氢化物的沸点:Y>Z | D.化合物WX中含有共价键 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】如图是元素周期表的一部分,W、X、Y、Z均为短周期主族元素,Z与X的最高化合价之和为10。下列说法错误的是

A.简单离子半径: |
| B.常温常压下,X的单质为固态 |
C.气态氢化物的稳定性: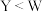 |
| D.Z的最高价氧化物对应的水化物的浓溶液具有脱水性 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】短周期主族元素X、Y、Z和W的原子序数依次增大,X是形成化合物种类最多的元素,Y和X元素原子的核电荷数之比为2∶1,Z的最低负价的绝对值等于Y的最高正价。下列说法不正确的是
| A.原子半径的大小顺序:Y>Z>W>X |
| B.Y的单质可以与X的最高价氧化物反应 |
| C.Z的气态氢化物比W的气态氢化物更稳定 |
| D.Y、Z对应的最高价氧化物的水化物反应生成的一种产物中含有共价键和离子键 |
您最近一年使用:0次

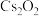 、
、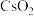 、
、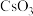 等复杂产物
等复杂产物

