有A、B、C、D四种短周期元素, 它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数, 且A的L层电子数是K层电子数的两倍, C在空气中燃烧时呈现黄色火焰, C的单质在高温下与B的单质充分反应, 可以得到与D单质颜色相同的淡黄色固态化合物。
试根据以上叙述回答:
(1)元素名称: A______ B _____ C _____ D ______ 。
(2)D元素位于周期表中______ 周期___________ 族。
(3)写出AB2与C2B2反应的化学方程式________________________________________________ 。
(4)画出B的原子结构简图___________________ 。
(5)用电子式表示化合物 C2D 的形成过程:__________________________________ 。
试根据以上叙述回答:
(1)元素名称: A
(2)D元素位于周期表中
(3)写出AB2与C2B2反应的化学方程式
(4)画出B的原子结构简图
(5)用电子式表示化合物 C2D 的形成过程:
10-11高二下·浙江宁波·阶段练习 查看更多[3]
(已下线)2010-2011学年浙江省宁海县正学中学高一下学期第二次阶段性测试化学试卷(已下线)2011-2012学年太原五中高一下学期期中考试化学试卷人教版高一化学必修2同步练习:第一章第二节第二课时《元素周期律的应用》
更新时间:2016-12-09 03:10:08
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】近日,科学家开发并发现立方GeMnTe2和GeMnTe2-x%SbTe具有高热电性能。回答下列问题:
(1)基态碲(Te)价层电子排布式为5s25p4,它位于元素周期表第_______ 周期_______ 族。基态锰原子中有_______ 种运动状态不同的电子。
(2)基态锗原子核外电子排布简式为[Ar]_______ ;氧族元素基态原子价层电子排布通式为_______ (能层数用n表示);锰(Mn)、锝(Tc)、铼(Re)位于同族,它们的最高正化合价为_______ 。
(3)氢气与某单质直接化合生成1mol气态物质的焓变,通常称为气态氢化物的生成热。氧族元素R的氢化物H2R的生成热与R的原子序数关系如图所示。
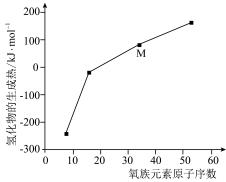
M的化学式为_______ ,氧族元素的氢化物的生成热随着原子序数增大而升高的主要原因是(从结构的角度解释)_______ 。
(4)大多数锗的化合物是共价化合物,不容易形成离子化合物,其主要原因是_______ 。
(1)基态碲(Te)价层电子排布式为5s25p4,它位于元素周期表第
(2)基态锗原子核外电子排布简式为[Ar]
(3)氢气与某单质直接化合生成1mol气态物质的焓变,通常称为气态氢化物的生成热。氧族元素R的氢化物H2R的生成热与R的原子序数关系如图所示。

M的化学式为
(4)大多数锗的化合物是共价化合物,不容易形成离子化合物,其主要原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同。
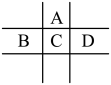
回答下列问题:
(1)A与E形成的化合物的化学式是___ 。
(2)B的最高价氧化物化学式为___ ,C的元素名称为___ 。
(3)D的单质与水反应的离子方程式为___ 。
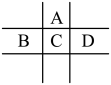
回答下列问题:
(1)A与E形成的化合物的化学式是
(2)B的最高价氧化物化学式为
(3)D的单质与水反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有A、B、C、D、E、F、G七种短周期主族元素,其原子序数依次增大。已知A、D位于同一主族,D是短周期中原子半径最大的元素。B、E最外层电子数是最内层电子数的2倍。C、F的最外层电子数相等,且C、F的原子序数之和为A、D原子序数之和的两倍。
(1)A、C、D、F形成的简单离子半径由大到小的顺序是___________ (用元素符号填写);
(2)B、E、F、G的最高价氧化物对应的水化物酸性最强的是___________ (用化学式填写);
(3)由C、D两元素能形成一种原子个数比为1:1的化合物,该化合物所含的化学键类型有___________ ;
(4)下列事实能说明G元素的非金属性比F元素的非金属性强的是___________ (填字母序号)。
a.G单质与Na2S溶液反应溶液变浑浊
b.F氢化物的酸性比G的氢化物酸性弱
c.G和F两元素的简单氢化物受热分解,前者的分解温度高
(1)A、C、D、F形成的简单离子半径由大到小的顺序是
(2)B、E、F、G的最高价氧化物对应的水化物酸性最强的是
(3)由C、D两元素能形成一种原子个数比为1:1的化合物,该化合物所含的化学键类型有
(4)下列事实能说明G元素的非金属性比F元素的非金属性强的是
a.G单质与Na2S溶液反应溶液变浑浊
b.F氢化物的酸性比G的氢化物酸性弱
c.G和F两元素的简单氢化物受热分解,前者的分解温度高
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E三种原子最外层共有10个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4。
(1)写出下列元素符号:C___________ ,D___________ ;
(2)用电子式表示D的氢化物的形成过程:___________ ;
(3)写出A与氧元素形成的原子个数比为1:1的化合物的电子式___________ ;
(4)写出B的最高价氧化物的水化物与E的最高价氧化物的水化物反应的离子方程式:___________ ;
(5)A的最高价氧化物的水化物中含有的化学键类型(填离子键、极性键、非极性键)___________ 。
(1)写出下列元素符号:C
(2)用电子式表示D的氢化物的形成过程:
(3)写出A与氧元素形成的原子个数比为1:1的化合物的电子式
(4)写出B的最高价氧化物的水化物与E的最高价氧化物的水化物反应的离子方程式:
(5)A的最高价氧化物的水化物中含有的化学键类型(填离子键、极性键、非极性键)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】有A、B、C、D、E五种原子序数依次增大的短周期主族元素,A是短周期主族元素中原子半径最大的元素,B是地壳中含量最多的金属元素,C元素原子的最外层电子数比次外层电子数少4,D元素原子的次外层电子数比最外层电子数多3,A、B、E三种原子的最外层电子数之和为11,请回答下列问题:
(1)写出A、B、C三种元素的元素符号:A_____ 、B________ 、C________ 。
(2) C的原子结构示意图为______ 。
(3) D的最简单氢化物的化学式为____ ,E的最高价氧化物对应的水化物的化学式为_____ 。
(4) A与氧元素形成的化合物的电子式为________ 。
(5) D和E的最简单氢化物中稳定性强的是_______ (填化学式)。.
(1)写出A、B、C三种元素的元素符号:A
(2) C的原子结构示意图为
(3) D的最简单氢化物的化学式为
(4) A与氧元素形成的化合物的电子式为
(5) D和E的最简单氢化物中稳定性强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知有原子序数依次增大的A、B、C、D、E五种短周期元素和过度金属元素F,其相关信息如下:
①A与C形成的化合物的水溶液呈碱性
②B的最高正价和最低负价的代数和为0
③D的常见化合物的焰色反应为黄色
④E的氧化物属于两性氧化物。
(1)分子式为B5A12且其一氯代物只有一种的有机物的名称为____ .
(2)C元素的气态氢化物与其最高价氧化物对应的水化物化合生成M,M的水溶液呈___ 性。
(3)1molD元素的最高价氧化物对应的水化物与2molE元素的单质反应产生气体体积为_______ L(标准状况下)
(4)F与B形成的合金在潮湿的空气中易发生电化学腐蚀形成红棕色固体,腐蚀过程中正极的电极反应式为______ .
①A与C形成的化合物的水溶液呈碱性
②B的最高正价和最低负价的代数和为0
③D的常见化合物的焰色反应为黄色
④E的氧化物属于两性氧化物。
(1)分子式为B5A12且其一氯代物只有一种的有机物的名称为
(2)C元素的气态氢化物与其最高价氧化物对应的水化物化合生成M,M的水溶液呈
(3)1molD元素的最高价氧化物对应的水化物与2molE元素的单质反应产生气体体积为
(4)F与B形成的合金在潮湿的空气中易发生电化学腐蚀形成红棕色固体,腐蚀过程中正极的电极反应式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】X、Y、Z、W是原子序数依次增大的短周期元素。已知:①X、Z同主族,Y、W同主族;②X、Y可形成两种化合物X2Y和X2Y2;③X2W和WY2之间可发生反应生成W单质;Z2Y2和X2Y之间可发生反应生成Y单质。请回答下列问题:
(1)写出元素符号:X__________ ,Y__________ 。
(2)W元素在周期表中的位置________________ 。
(3)写出有关反应的方程式:③反应的化学方程式_________________ ,④反应的离子方程式__________________ 。
(4)由X、Y、Z、W四种元素中任选三种元素分别构成两种化合物,写出这两种化合物与Z2W反应生成W单质的离子方程式_________________________ 。
(1)写出元素符号:X
(2)W元素在周期表中的位置
(3)写出有关反应的方程式:③反应的化学方程式
(4)由X、Y、Z、W四种元素中任选三种元素分别构成两种化合物,写出这两种化合物与Z2W反应生成W单质的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】Q、W、X、Y、Z 是位于不同主族的五种短周期元素,其原子序数依次增大。
①W 的氢化物与 W 最高价氧化物对应水化物反应生成化合物甲。
②X、Y、Z 的最高价氧化物对应水化物之间两两反应均可生成盐和水。
③常温下,Q 的最高价气态氧化物与化合物 X2O2 发生反应生成盐乙。
请回答下列各题:
(1)甲的水溶液呈酸性,用离子方程式表示其原因____________________________________________________________________________ 。
(2)③中反应的化学方程式为________________________________________________________________________________________________ 。
(3)已知:ZO3n-+M2++H+→Z-+M4+ + H2O(M 为金属元素,方程式未配平)由上述信息可推测 Z 在周期表中位置为________________________________________________________________________________________________ 。
(4)Y 形成的难溶半导体材料 CuYO2 可溶于稀硝酸,同时生成 NO。写出此反应的离子方秳式_____________________________ 。
①W 的氢化物与 W 最高价氧化物对应水化物反应生成化合物甲。
②X、Y、Z 的最高价氧化物对应水化物之间两两反应均可生成盐和水。
③常温下,Q 的最高价气态氧化物与化合物 X2O2 发生反应生成盐乙。
请回答下列各题:
(1)甲的水溶液呈酸性,用离子方程式表示其原因
(2)③中反应的化学方程式为
(3)已知:ZO3n-+M2++H+→Z-+M4+ + H2O(M 为金属元素,方程式未配平)由上述信息可推测 Z 在周期表中位置为
(4)Y 形成的难溶半导体材料 CuYO2 可溶于稀硝酸,同时生成 NO。写出此反应的离子方秳式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知A、B、C、D、E五种元素为周期表前20号元素,且原子序数依次增大,其中只有A、D为非金属元素。A的气态氢化物溶于水得到的溶液能使酚酞溶液变红。B、C、D的最高价氧化物对应水化物之间能够两两反应,且D原子最外层电子数是C原子最外层电子数的2倍。B、E元素同主族。
(1)E在元素周期表中的位置:____________ ,写出E的最高价氧化物对应水化物与C的单质反应的化学方程式:________________________________________________ 。
(2)B单质在空气中燃烧的产物的电子式为____________ ,产物中存在的化学键类型有____________ 。
(1)E在元素周期表中的位置:
(2)B单质在空气中燃烧的产物的电子式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】叠氮化钾能促进难以萌发的种子发育,在新作物育种中应用广泛。实验室制备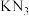 流程如下。回答下列问题:
流程如下。回答下列问题:
I.制备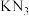 :
:

已知:①制备亚硝酸异丙酯在烧杯中进行;
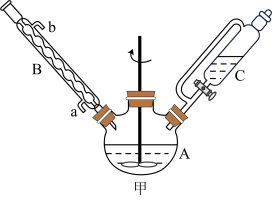
②制备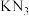 的D、E和F阶段均在图甲装置中完成。
的D、E和F阶段均在图甲装置中完成。
(1)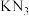 属于
属于_______ (填“离子化合物”或“共价化合物”)。
(2)仪器A的名称为_______ ,仪器B的作用是_______ 。
(3)仪器A中发生反应时,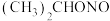 与水合肼在碱性条件下,重新生成
与水合肼在碱性条件下,重新生成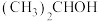 (异丙醇),该反应的化学方程式为
(异丙醇),该反应的化学方程式为_______ 。
(4)关于上述流程中各步骤的说法,错误的是_______ (填标号)。
A.步骤D还需要的仪器是容量瓶和胶头滴管
B.制备亚硝酸异丙酯时用冰盐浴的目的是防止反应过于剧烈
C.步骤F加入无水乙醇的目的是促进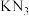 的溶解
的溶解
II.纯度检测——“分光光度法”: 与
与 反应灵敏,生成红色配合物,在一定波长下测量红色溶液的吸光度,利用“
反应灵敏,生成红色配合物,在一定波长下测量红色溶液的吸光度,利用“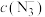 —吸光度”曲线确定样品溶液中的
—吸光度”曲线确定样品溶液中的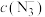 。
。
查阅文献可知:不同浓度的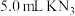 标准溶液,分别加入5.0 mL(足量)
标准溶液,分别加入5.0 mL(足量) 溶液,摇匀后测量吸光度,可绘制标准溶液的
溶液,摇匀后测量吸光度,可绘制标准溶液的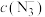 与吸光度的关系曲线如图乙所示。
与吸光度的关系曲线如图乙所示。

乙
纯度检测步骤如下:
①准确称取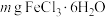 晶体,配制100mLFeCl3标准液(与文献浓度一致)。
晶体,配制100mLFeCl3标准液(与文献浓度一致)。
②准确称取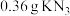 样品,配制成100 mL溶液,取5.0 mL待测溶液,向其中加入V mL(足量)
样品,配制成100 mL溶液,取5.0 mL待测溶液,向其中加入V mL(足量) 标准液,摇匀后测得吸光度为0.6。
标准液,摇匀后测得吸光度为0.6。
(5)配制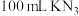 溶液需要用到下列操作:
溶液需要用到下列操作:
a.打开容量瓶玻璃塞,加入适量水,塞紧塞子,倒立;
b.将塞子反转180°,倒立;
c.洗涤烧杯内壁和玻璃棒2~3次;
d.冷却至室温;
e.轻轻振荡容量瓶;
f.称取0.36 g试样置于烧杯中,加入适量水充分溶解;
g.将溶液转移到容量瓶中;
h.定容,摇匀。
上述给出操作的正确顺序:a→_____→______→_______→g→_______→_______→_______→h(操作可重复)。_______
(6)步骤②中取用 标准液V=
标准液V=_______ mL,样品的质量分数为_______ 。
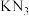 流程如下。回答下列问题:
流程如下。回答下列问题:I.制备
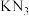 :
:
已知:①制备亚硝酸异丙酯在烧杯中进行;
②制备
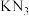 的D、E和F阶段均在图甲装置中完成。
的D、E和F阶段均在图甲装置中完成。
(1)
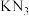 属于
属于(2)仪器A的名称为
(3)仪器A中发生反应时,
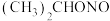 与水合肼在碱性条件下,重新生成
与水合肼在碱性条件下,重新生成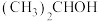 (异丙醇),该反应的化学方程式为
(异丙醇),该反应的化学方程式为(4)关于上述流程中各步骤的说法,错误的是
A.步骤D还需要的仪器是容量瓶和胶头滴管
B.制备亚硝酸异丙酯时用冰盐浴的目的是防止反应过于剧烈
C.步骤F加入无水乙醇的目的是促进
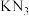 的溶解
的溶解II.纯度检测——“分光光度法”:
 与
与 反应灵敏,生成红色配合物,在一定波长下测量红色溶液的吸光度,利用“
反应灵敏,生成红色配合物,在一定波长下测量红色溶液的吸光度,利用“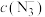 —吸光度”曲线确定样品溶液中的
—吸光度”曲线确定样品溶液中的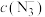 。
。查阅文献可知:不同浓度的
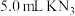 标准溶液,分别加入5.0 mL(足量)
标准溶液,分别加入5.0 mL(足量) 溶液,摇匀后测量吸光度,可绘制标准溶液的
溶液,摇匀后测量吸光度,可绘制标准溶液的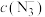 与吸光度的关系曲线如图乙所示。
与吸光度的关系曲线如图乙所示。
乙
纯度检测步骤如下:
①准确称取
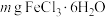 晶体,配制100mLFeCl3标准液(与文献浓度一致)。
晶体,配制100mLFeCl3标准液(与文献浓度一致)。②准确称取
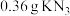 样品,配制成100 mL溶液,取5.0 mL待测溶液,向其中加入V mL(足量)
样品,配制成100 mL溶液,取5.0 mL待测溶液,向其中加入V mL(足量) 标准液,摇匀后测得吸光度为0.6。
标准液,摇匀后测得吸光度为0.6。(5)配制
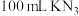 溶液需要用到下列操作:
溶液需要用到下列操作:a.打开容量瓶玻璃塞,加入适量水,塞紧塞子,倒立;
b.将塞子反转180°,倒立;
c.洗涤烧杯内壁和玻璃棒2~3次;
d.冷却至室温;
e.轻轻振荡容量瓶;
f.称取0.36 g试样置于烧杯中,加入适量水充分溶解;
g.将溶液转移到容量瓶中;
h.定容,摇匀。
上述给出操作的正确顺序:a→_____→______→_______→g→_______→_______→_______→h(操作可重复)。
(6)步骤②中取用
 标准液V=
标准液V=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2型离子化合物。
(1)Y2O2含有的化学键有非极性共价键与_____ ,该化合物属于______ (填“离子化合物” 、“共价化合物”)。
(2)用电子式表示Y2O的形成过程______________________________ 。
(3)Z、W两种元素的最高价氧化物对应的水化物中,酸性最强的水化物是_____ (填化学式)。
(4)X与氢组成的化合物中, 既含有极性共价键又含有非极性共价键的化合物的结构式__________ 。
(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成两种化合物,其中一种具有漂白性,另一种能使湿润的红色石蕊试纸变蓝。写出该化合物与水反应的化学方程式_________________ 。
(1)Y2O2含有的化学键有非极性共价键与
(2)用电子式表示Y2O的形成过程
(3)Z、W两种元素的最高价氧化物对应的水化物中,酸性最强的水化物是
(4)X与氢组成的化合物中, 既含有极性共价键又含有非极性共价键的化合物的结构式
(5)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成两种化合物,其中一种具有漂白性,另一种能使湿润的红色石蕊试纸变蓝。写出该化合物与水反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知五种元素的原子序数的大小顺序为C>A>B>D>E, A、C同周期,B、C同主族;A与B可形成离子化合物A2B,A2B2;D和E可形成4个原子的分子,能使湿润的红色石蕊试液变蓝。试回答下列问题:
(1)写出元素的名称:A____ , D_____ ,
(2)写出下列物质的电子式:A、B、E形成的化合物_________ ;DE形成的化合物_______ ;
(3)A、B两元素组成的化合物A2B2属于__________ (填“离子”或“共价”)化合物;
(4)写出A2B2与水反应的化学方程式____________________
(1)写出元素的名称:A
(2)写出下列物质的电子式:A、B、E形成的化合物
(3)A、B两元素组成的化合物A2B2属于
(4)写出A2B2与水反应的化学方程式
您最近一年使用:0次



