已知A、B、C、D、E五种元素为周期表前20号元素,且原子序数依次增大,其中只有A、D为非金属元素。A的气态氢化物溶于水得到的溶液能使酚酞溶液变红。B、C、D的最高价氧化物对应水化物之间能够两两反应,且D原子最外层电子数是C原子最外层电子数的2倍。B、E元素同主族。
(1)E在元素周期表中的位置:____________ ,写出E的最高价氧化物对应水化物与C的单质反应的化学方程式:________________________________________________ 。
(2)B单质在空气中燃烧的产物的电子式为____________ ,产物中存在的化学键类型有____________ 。
(1)E在元素周期表中的位置:
(2)B单质在空气中燃烧的产物的电子式为
更新时间:2020-09-02 14:25:33
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期元素A、B、C、D的原子序数依次增大,X、Y、Z、W是由这四种元素中的两种元素组成的常见化合物,X为有刺激性气味的气体,Y为淡黄色固体,甲是由C元素形成的气体单质,乙为红棕色气体,上述物质之间的转化关系如图所示(部分反应物或生成物省略)。
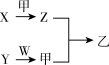
(1)A、B、C、D的原子半径大小顺序为_______ 。(用元素符号表示)
(2)B、C的气态氢化物的稳定性顺序为_______ 。(用化学式表示)
(3)B的最高价氧化物的水化物为_______ 。(用化学式表示)
(4)Y生成甲的化学方程式_______ 。
(5)若Z与甲反应生成1.12L乙(标准状况下),则该反应转移的电子数目为_______ 。

(1)A、B、C、D的原子半径大小顺序为
(2)B、C的气态氢化物的稳定性顺序为
(3)B的最高价氧化物的水化物为
(4)Y生成甲的化学方程式
(5)若Z与甲反应生成1.12L乙(标准状况下),则该反应转移的电子数目为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C、D、E、F、G、H是核电荷数依次增大的短周期主族元素。元素A的原子半径是所有元素中最小的。A、E同主族,B、C、D同周期,D、G最外层电子数相等,G的质量数为D的2倍,元素B的一种常见单质可做惰性电极材料,其最高价氧化物甲为常见温室气体。B、D、G的质子数之和等于F、H的质子数之和,I单质是日常生活中用量最大的金属,易被腐蚀或损坏。回答下列问题:
(1)I元素在周期表中的位置________________ 。
(2)化合物甲的结构式为______________________ 。
(3)根据以上信息,下列说法不正确的是______________。
(4)常温下,相同浓度F、I简单离子的溶液中滴加NaOH溶液,F、I两元素先后沉淀,F (OH)n完全沉淀的pH是4.7,I (OH)n完全沉淀的pH是2.8,则ksp较大的是:_______________ (填化学式)
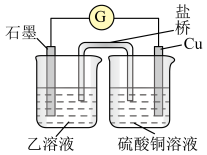
(5)若在H与I组成的某种化合物的溶液乙中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图所示,其反应中正极电极反应式为______________ 。
(6)若用石墨电极电解含有0.04 mol CuGD4和0.04 mol EH的混合溶液400 mL,当阳极产生的气体784 mL(标况)时,溶液的pH=___________ (假设电解后溶液体积不变)。
(1)I元素在周期表中的位置
(2)化合物甲的结构式为
(3)根据以上信息,下列说法不正确的是______________。
| A.A和B能形成多种化合物 |
| B.热稳定性:H2D< H2G |
| C.元素G的最高价氧化物对应水化物的酸性比H的弱 |
| D.简单离子半径的大小顺序:rD<rE<rF |
| E.沸点:H2D< H2G |
| F.同温同压下,将a L CA3和b L AH通入水中,若所得溶液的pH=7,则a>b |
(5)若在H与I组成的某种化合物的溶液乙中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图所示,其反应中正极电极反应式为

(6)若用石墨电极电解含有0.04 mol CuGD4和0.04 mol EH的混合溶液400 mL,当阳极产生的气体784 mL(标况)时,溶液的pH=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知几种元素的性质或原子结构的相关叙述如表所示。
回答下列问题:
(1)元素X的一种同位素用作相对原子质量的标准,这种同位素的原子符号是________ 。
(2)Y形成的另一种单质主要存在于地球的平流层中,被称作地球生物的保护伞,该单质的化学式是________ 。
(3)元素Z在海水中含量非常高,海水中含Z元素的化合物主要是__________ (写化学式)。
(4)画出T原子的结构示意图:____________ 。
(5)T元素组成的单质在Y元素组成的常见单质中燃烧,得到的产物是________ (填化学式)。
| 元素 | 元素性质或原子结构的相关叙述 |
| T | 失去1个电子后,形成与Ne相同的核外电子排布 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 其某种单质是空气的主要成分,也是最常见的助燃剂 |
| Z | 原子核外有3个电子层,最外层比次外层少1个电子 |
(1)元素X的一种同位素用作相对原子质量的标准,这种同位素的原子符号是
(2)Y形成的另一种单质主要存在于地球的平流层中,被称作地球生物的保护伞,该单质的化学式是
(3)元素Z在海水中含量非常高,海水中含Z元素的化合物主要是
(4)画出T原子的结构示意图:
(5)T元素组成的单质在Y元素组成的常见单质中燃烧,得到的产物是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知A、B、C、D、E、F、G、H为原子序数依次增大的主族元素,其中A、D与G同主族,且A、B不同周期,D元素的焰色试验为黄色,F的单质为有色气体,元素H的核电荷数为34。B、C、E、F在元素周期表中的相对位置如图,请回答下列问题:
(1)元素A与B组成的六原子平面分子中同一碳原子形成的任意两个键的夹角约为_______ 。元素H在元素周期表中的位置为_______ 。
(2)请用电子式表示A和E的原子形成化合物的过程:_______ ,C和F形成的化合物中化学键类型是_______ (填“离子键”、“极性共价键”或“非极性共价键”)。
(3)元素E和F的简单氢化物的还原性顺序为_______ (用化学式表示)。
(4)少量E的低价氧化物与G的最高价氧化物对应水化物的水溶液发生反应的离子方程式_______ 。
(5)简述如何确定D的化合物中是否含有G元素_______ 。
| B | C | ||
| E | F |
(2)请用电子式表示A和E的原子形成化合物的过程:
(3)元素E和F的简单氢化物的还原性顺序为
(4)少量E的低价氧化物与G的最高价氧化物对应水化物的水溶液发生反应的离子方程式
(5)简述如何确定D的化合物中是否含有G元素
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】短周期元素W、X、Y、Z的原子序数依次增大,Y的原子半径是短周期主族元素中最大的,元素W的最外层电子数是次外层的2.5倍,元素X的最外层电子数是电子层数的3倍,元素Z的单质,通常为黄绿色气体,与Y的最高价氧化物的水化物反应的产物可作漂白剂和消毒剂。
(1)元素W、X、Y、Z的符号分别是______ ,______ ,______ ,______ 。
(2)实验中制备Z单质的反应方程式为________________________ 。
(3)Z单质与X的氢化物发生反应的化学方程式为__________________ 。若将干燥的有色布条放入Z的单质中,观察到的现象是 ___________________ ,原因是__________ 。
(4)Z单质与Y的最高价氧化物的水化物反应的化学方程式是_______ ,该反应中2mol Z完全反应时转移电子的数目_______ NA。
(5)实验中制备W的氢化物的反应方程式为_________________ 。
(1)元素W、X、Y、Z的符号分别是
(2)实验中制备Z单质的反应方程式为
(3)Z单质与X的氢化物发生反应的化学方程式为
(4)Z单质与Y的最高价氧化物的水化物反应的化学方程式是
(5)实验中制备W的氢化物的反应方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有A、B、C、D、E五种元素,它们的质子数依次增多。
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3型化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+比B3+多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于C的下两个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质后的量之比为2:1。
试回答:
(1)B是__________ (写元素符号,下同),E是___________ 。
(2)D的单质分子的电子式:_________ ,C元素最高价氧化物对应的水化物的电子式:________ ;B的离子结构示意图:__________ 。
(3)用电子式表示H2A形成过程:___________ 。
(4)写出一例能证明B与C化学性质强弱的事实___________ 。
(5)写出CD的溶液中通入氯气的离子方程式:_____________ 。
(6)比较B、C、E三种元素形成的简单离子氧化性的强弱(B、C、E离子用实际离子符号表示):_______ 。
①A的核电荷数大于2,可形成氢化物H2A,该氢化物在常温下是液体;
②A和B两元素可形成B2A3型化合物,该化合物既能溶于强酸,又能溶于强碱;
③C+比B3+多8个电子;
④C与D元素可以形成化合物CD;
⑤CD的溶液中通入氯气后加淀粉溶液显蓝色;
⑥在周期表中E处于C的下两个周期,E单质可与冷水反应生成氢气,反应时E的单质与生成的氢气的物质后的量之比为2:1。
试回答:
(1)B是
(2)D的单质分子的电子式:
(3)用电子式表示H2A形成过程:
(4)写出一例能证明B与C化学性质强弱的事实
(5)写出CD的溶液中通入氯气的离子方程式:
(6)比较B、C、E三种元素形成的简单离子氧化性的强弱(B、C、E离子用实际离子符号表示):
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E、F六种短周期元素,原子序数依次增大。A、E同主族,且E元素原子的核外电子数是A元素原子核内质子数的两倍。B、C两元素原子的最外层电子数之和等于D元素原子的最外层电子数,C、D两元素原子最外层电子数之和等于F元素原子的最外层电子数。D元素原子最外层电子数是次外层电子数的一半。回答下列问题:
(1)用电子式表示B、F两元素形成化合物的过程:_______________________________ 。
(2)A、C两元素的化合物与B的氢氧化物反应的离子方程式为:___________________ 。
(3)B的最高价氧化物的水化物与C的最高价氧化物的水化物反应的离子方程式为:__________ 。
(4)写出下列物质的电子式,指出化学键类型。
B2E:___________ 、___________ ; EF2:___________ 、___________ 。
(1)用电子式表示B、F两元素形成化合物的过程:
(2)A、C两元素的化合物与B的氢氧化物反应的离子方程式为:
(3)B的最高价氧化物的水化物与C的最高价氧化物的水化物反应的离子方程式为:
(4)写出下列物质的电子式,指出化学键类型。
B2E:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表短周期的一部分:
(1) ①-⑦元素中非金属性最强的元素位于周期表中的位置为______________________ 。
(2) ③与⑤形成的化合物与水反应产生气体,该反应的化学方程式_______________ 。该化合物的电子式为______
(3) ④所形成的单质与水反应的方程式_____________ 。
(4) ②、⑦、⑨的最高价含氧酸的酸性由弱到强的顺序是__________________ (用化学式表示)。
(5) 表中元素⑤和⑥的最高价氧化物的水化物之间相互反应的离子方程式为____________ 。
(6) ②的气态氢化物的实验室制法的反应原理:____________________ ;(写出化学方程式)
②的气态氢化物和它的最高价氧化物的水化物反应的产物为______________ (“离子”或“共价”)化合物。
| ① | ||||||||
| ⑨ | ② | ③ | ④ | |||||
| ⑤ | ⑥ | ⑦ | ⑧ | |||||
(1) ①-⑦元素中非金属性最强的元素位于周期表中的位置为
(2) ③与⑤形成的化合物与水反应产生气体,该反应的化学方程式
(3) ④所形成的单质与水反应的方程式
(4) ②、⑦、⑨的最高价含氧酸的酸性由弱到强的顺序是
(5) 表中元素⑤和⑥的最高价氧化物的水化物之间相互反应的离子方程式为
(6) ②的气态氢化物的实验室制法的反应原理:
②的气态氢化物和它的最高价氧化物的水化物反应的产物为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、R、Q、M是六种短周期元素,原子序数依次增大。X是原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z为地壳中含量最多的元素,R与X同主族,Y、R、Q最外层电子数之和为8,M的单质为黄绿色有害气体。请回答下列问题:
(1)R在元素周期表中的位置为__ 。
(2)Z、Q、M简单离子半径由大到小的顺序为__ (写离子符号)。
(3)X、Y、Z三种元素形成盐类化合物的水溶液呈酸性的原因:__ (用离子方程式表示)。
(4)YX4M的电子式为__ ;Q3Y2与水可剧烈反应,产生沉淀与气体,反应的化学方程式为__ 。
(5)X、Z两元素形成的原子个数比为1∶1的化合物中含有的化学键类型为__ 。
(6)M的单质与R的最高价氧化物对应的水化物反应的离子方程式为__ 。
(1)R在元素周期表中的位置为
(2)Z、Q、M简单离子半径由大到小的顺序为
(3)X、Y、Z三种元素形成盐类化合物的水溶液呈酸性的原因:
(4)YX4M的电子式为
(5)X、Z两元素形成的原子个数比为1∶1的化合物中含有的化学键类型为
(6)M的单质与R的最高价氧化物对应的水化物反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E都是前四周期元素,A原子价电子排布式为nsnnPn,B原子核外有3种能量不同的电子,B、C同主族,B与C形成的一种化合物是形成酸雨的重要物质。D原子核外电子有11种不同的运动状态。E是前四周期中原子核外成单电子数最多的元素。
回答下列问题:
(1)元素A的一种单质的结构如图所示。
其中A-A-A键之间的夹角是____________ ,含有1mol A的该单质中,形成的共价键有____ mol。
(2)等径圆球在二维空间里可形成密置层和非密置层排列。在二维空间里D晶体的配位数是_______ 。
(3)E的基态原子的外围电子排布式为_______ ,AC2的电子式为 _______________ 。
(4)下列关于AB2的晶体和冰的比较中正确的是______ (填标号)。
a.晶体的密度:AB2的晶体 > 冰
b.晶体的熔点:AB2的晶体 >冰
c.晶体中的空间利用率:AB2的晶体 >冰
d.晶体中分子间相互作用力类型相同
(5)D2C的晶胞如图,设晶体密度是ρg/㎝3
①比较D2C与D2B的熔点,较高的是_______ (填化学式),其原因是 ___________________ 。
②试计算●与〇的最短距离______ (只写出计算式,阿伏伽德罗常数的值用NA表示)。
回答下列问题:
(1)元素A的一种单质的结构如图所示。

其中A-A-A键之间的夹角是
(2)等径圆球在二维空间里可形成密置层和非密置层排列。在二维空间里D晶体的配位数是
(3)E的基态原子的外围电子排布式为
(4)下列关于AB2的晶体和冰的比较中正确的是
a.晶体的密度:AB2的晶体 > 冰
b.晶体的熔点:AB2的晶体 >冰
c.晶体中的空间利用率:AB2的晶体 >冰
d.晶体中分子间相互作用力类型相同
(5)D2C的晶胞如图,设晶体密度是ρg/㎝3
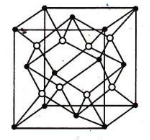
①比较D2C与D2B的熔点,较高的是
②试计算●与〇的最短距离
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。回答下列问题:
(1)W、X对应的两种最高价氧化物的水化物可以反应生成盐和水,该反应的离子方程式为______________________________________________________ 。
(2)X的硝酸盐水溶液显______ 性,用离子方程式解释原因______________________ 。
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为____________ 。
(4)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是: > > > 。(填写离子符号)_____________
(5)Z的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出QkJ的热量。写出该反应的热化学方程式:___________________________ 。
(1)W、X对应的两种最高价氧化物的水化物可以反应生成盐和水,该反应的离子方程式为
(2)X的硝酸盐水溶液显
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为
(4)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是: > > > 。(填写离子符号)
(5)Z的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出QkJ的热量。写出该反应的热化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、J、Q五种短周期主族元素,原子序数依次增大,元素Z在地壳中含量最高,J元素的焰色反应呈黄色,Q的最外层电子数与其电子总数比为3∶8,X能与J形成离子化合物,且J+的半径大于X—的半径,Y的氧化物是形成酸雨的主要物质之一。请回答:
(1)Q元素在周期表中的位置______________________________ 。
(2)这五种元素原子半径从大到小的顺序为____________ (填元素符号)。
(3)元素的非金属性Z________ Q(填“>”或“<”),下列各项中,不能说明这一结论的事实有________ (填序号)。
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态
D.Z和Q在周期表中的位置
(4)Q的氢化物与Z的氢化物反应的化学方程式为___________ 。
(5)X与Y可形成分子A,也可形成阳离子B,A、B在水溶液中酸、碱性恰好相反,写出A的电子式__________ ;B的水溶液不呈中性的原因________________________ (用离子方程式表示)。
(6)液态A类似X2Z,也能微弱电离且产生电子数相同的两种离子,则液态A的电离方程式为___________________________________________ 。
(1)Q元素在周期表中的位置
(2)这五种元素原子半径从大到小的顺序为
(3)元素的非金属性Z
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态
D.Z和Q在周期表中的位置
(4)Q的氢化物与Z的氢化物反应的化学方程式为
(5)X与Y可形成分子A,也可形成阳离子B,A、B在水溶液中酸、碱性恰好相反,写出A的电子式
(6)液态A类似X2Z,也能微弱电离且产生电子数相同的两种离子,则液态A的电离方程式为
您最近一年使用:0次



