W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。回答下列问题:
(1)W、X对应的两种最高价氧化物的水化物可以反应生成盐和水,该反应的离子方程式为______________________________________________________ 。
(2)X的硝酸盐水溶液显______ 性,用离子方程式解释原因______________________ 。
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为____________ 。
(4)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是: > > > 。(填写离子符号)_____________
(5)Z的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出QkJ的热量。写出该反应的热化学方程式:___________________________ 。
(1)W、X对应的两种最高价氧化物的水化物可以反应生成盐和水,该反应的离子方程式为
(2)X的硝酸盐水溶液显
(3)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为
(4)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是: > > > 。(填写离子符号)
(5)Z的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出QkJ的热量。写出该反应的热化学方程式:
更新时间:2020-03-06 09:04:17
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】我国 车用燃料甲醇国家标准
车用燃料甲醇国家标准 的实施拉开了车用燃料低碳革命的大幕,一些省市正在陆续试点与推广使用甲醇汽油。甲醇可通过
的实施拉开了车用燃料低碳革命的大幕,一些省市正在陆续试点与推广使用甲醇汽油。甲醇可通过 和
和 在一定条件下发生如下反应制得:
在一定条件下发生如下反应制得: 图Ⅰ、图Ⅱ是关于该反应进行情况的图示。
图Ⅰ、图Ⅱ是关于该反应进行情况的图示。
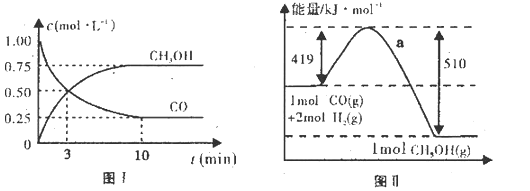
请根据图示回答下列问题:
(1)图 是反应时
是反应时 和
和 的浓度随时间的变化情况,从反应开始到平衡,用
的浓度随时间的变化情况,从反应开始到平衡,用 浓度变化表示平均反应速率v(CO)=
浓度变化表示平均反应速率v(CO)=___________ 。
(2)图Ⅱ表示该反应进行过程中能量的变化,曲线 表示不使用催化剂时反应的能量变化,在图Ⅱ中画出使用催化剂后的能量变化曲线b
表示不使用催化剂时反应的能量变化,在图Ⅱ中画出使用催化剂后的能量变化曲线b________________
(3)写出该反应的热化学方程式___________ 。
(4)该反应的平衡常数 的表达式为
的表达式为___________ ;当温度升高时,该平衡常数 将
将___________ (填“增大”、“减小”或“不变”)
(5)恒容条件下,下列措施中能使 增大的有___________。
增大的有___________。
(6)若在一体积可变的密闭容器中充入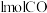 、
、 和
和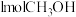 ,达到平衡时测得混合气体的密度是同温同压下起始的
,达到平衡时测得混合气体的密度是同温同压下起始的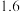 倍,则该反应向
倍,则该反应向___________ (填“正”、“逆”)反应方向移动,理由是___________ 。
 车用燃料甲醇国家标准
车用燃料甲醇国家标准 的实施拉开了车用燃料低碳革命的大幕,一些省市正在陆续试点与推广使用甲醇汽油。甲醇可通过
的实施拉开了车用燃料低碳革命的大幕,一些省市正在陆续试点与推广使用甲醇汽油。甲醇可通过 和
和 在一定条件下发生如下反应制得:
在一定条件下发生如下反应制得: 图Ⅰ、图Ⅱ是关于该反应进行情况的图示。
图Ⅰ、图Ⅱ是关于该反应进行情况的图示。
请根据图示回答下列问题:
(1)图
 是反应时
是反应时 和
和 的浓度随时间的变化情况,从反应开始到平衡,用
的浓度随时间的变化情况,从反应开始到平衡,用 浓度变化表示平均反应速率v(CO)=
浓度变化表示平均反应速率v(CO)=(2)图Ⅱ表示该反应进行过程中能量的变化,曲线
 表示不使用催化剂时反应的能量变化,在图Ⅱ中画出使用催化剂后的能量变化曲线b
表示不使用催化剂时反应的能量变化,在图Ⅱ中画出使用催化剂后的能量变化曲线b(3)写出该反应的热化学方程式
(4)该反应的平衡常数
 的表达式为
的表达式为 将
将(5)恒容条件下,下列措施中能使
 增大的有___________。
增大的有___________。| A.升高温度 | B.充入 气 气 | C.再充入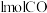 和 和 | D.使用催化剂 |
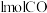 、
、 和
和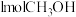 ,达到平衡时测得混合气体的密度是同温同压下起始的
,达到平衡时测得混合气体的密度是同温同压下起始的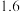 倍,则该反应向
倍,则该反应向
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题
(1)在 、
、 下,
下,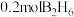 (气态高能燃料)在氧气中完全燃烧,生成固态三氧化二硼和液态水,放出
(气态高能燃料)在氧气中完全燃烧,生成固态三氧化二硼和液态水,放出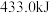 的热量,写出该反应的热化学方程式:
的热量,写出该反应的热化学方程式:_____________________ 。
(2)在一定条件下, 和
和 反应生成
反应生成 的热化学方程式为
的热化学方程式为
①将 和
和 充入
充入 密闭容器中进行反应,一定条件下,达到平衡时放出的热量
密闭容器中进行反应,一定条件下,达到平衡时放出的热量_________ (填“>”“<”或“=”)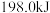 ;若反应进行到
;若反应进行到 时,
时, 的转化率为
的转化率为 ,则
,则 内,
内, 的平均反应速率为
的平均反应速率为__________  。
。
②上述反应达到平衡状态的标志是_______________ (填字母)。
A.反应速率 B.反应停止,容器内压强不再发生变化
B.反应停止,容器内压强不再发生变化
C. 的浓度不再发生变化 D.混合气体的平均相对分子质量不再改变
的浓度不再发生变化 D.混合气体的平均相对分子质量不再改变
(1)在
 、
、 下,
下,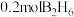 (气态高能燃料)在氧气中完全燃烧,生成固态三氧化二硼和液态水,放出
(气态高能燃料)在氧气中完全燃烧,生成固态三氧化二硼和液态水,放出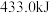 的热量,写出该反应的热化学方程式:
的热量,写出该反应的热化学方程式:(2)在一定条件下,
 和
和 反应生成
反应生成 的热化学方程式为
的热化学方程式为
①将
 和
和 充入
充入 密闭容器中进行反应,一定条件下,达到平衡时放出的热量
密闭容器中进行反应,一定条件下,达到平衡时放出的热量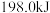 ;若反应进行到
;若反应进行到 时,
时, 的转化率为
的转化率为 ,则
,则 内,
内, 的平均反应速率为
的平均反应速率为 。
。②上述反应达到平衡状态的标志是
A.反应速率
 B.反应停止,容器内压强不再发生变化
B.反应停止,容器内压强不再发生变化C.
 的浓度不再发生变化 D.混合气体的平均相对分子质量不再改变
的浓度不再发生变化 D.混合气体的平均相对分子质量不再改变
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】运用化学反应原理研究氮、碳、硫等单质及其化合物的反应有重要意义。氨在国民经济中占有重要地位。合成氨工业中,合成塔中每产生2 mol NH3,放出92.2 kJ热量。
(1)合成氨反应的热化学方程式是_______ 。
(2)若起始时向容器内充入2 mol N2和6 mol H2,达平衡后放出的热量为Q,则Q_______ (填“>”“<”或“=”)184.4 kJ。
(3) ①已知拆开1 mol H—H键、1 mol N—H键分别需要的能量是436 kJ、391 k,若产生2 mol NH3,放出92.2 kJ热量,则拆开1 mol N≡N需要吸收的能量为_______ 。
(4)在稀溶液中,强酸跟强碱发生中和反应生成_______ 液态水时所释放的热量叫做中和热,1 L 1 mol·L-1 KOH溶液中和1 L 1 mol·L-1 HNO3溶液,放出57.3 kJ热量,则中和热为_______ 。
(5)若适量的N2和O2完全反应,每生成23 g NO2需要吸收16.95 kJ热量,其热化学方程式为_______ 。若在一定温度下,可逆反应2NO2⇌2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是_______ (填序号)
①单位时间内生成nmolO2的同时生成2nmolNO2
②混合气体的平均相对分子质量不再改变的状态
③混合气体的密度不再改变的状态
④混合气体的颜色不再改变的状态
⑤NO2、NO、O2的物质的量浓度比为2:2:1的状态
(1)合成氨反应的热化学方程式是
(2)若起始时向容器内充入2 mol N2和6 mol H2,达平衡后放出的热量为Q,则Q
(3) ①已知拆开1 mol H—H键、1 mol N—H键分别需要的能量是436 kJ、391 k,若产生2 mol NH3,放出92.2 kJ热量,则拆开1 mol N≡N需要吸收的能量为
(4)在稀溶液中,强酸跟强碱发生中和反应生成
(5)若适量的N2和O2完全反应,每生成23 g NO2需要吸收16.95 kJ热量,其热化学方程式为
①单位时间内生成nmolO2的同时生成2nmolNO2
②混合气体的平均相对分子质量不再改变的状态
③混合气体的密度不再改变的状态
④混合气体的颜色不再改变的状态
⑤NO2、NO、O2的物质的量浓度比为2:2:1的状态
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了①~⑨九种元素在周期表中的位置。
请回答:
(1)这九种元素分别是①_______ (填元素符号,下同)、②_______ 、③_______ 、④_______ 、⑤_______ 、⑥_______ 、⑦_______ 、⑧_______ 、⑨_______ ,其中化学性质最不活泼的是_______ 。
(2)在①、②、③三种元素的氧化物对应的水化物中,碱性最强的是_______ (填化学式)。
(3)①、②、③三种元素按原子半径由大到小的顺序依次为_______ (填元素符号)。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑨ | |||
| 4 | ② | ⑧ |
(1)这九种元素分别是①
(2)在①、②、③三种元素的氧化物对应的水化物中,碱性最强的是
(3)①、②、③三种元素按原子半径由大到小的顺序依次为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】1869年门捷列夫提出元素周期表,根据元素周期表和周期律,回答问题。
下表显示了元素周期表中短周期的一部分,①~⑥代表6种短周期元素。其中②与氢元素形成的简单氢化物分子中含10个电子,能够使湿润的红色石蕊试纸变蓝
(1)①在周期表中所处的位置为_______ 。
(2)与⑥同主族的第五周期元素的原子原子序数为_______ 。
(3)写出元素③与氢形成18电子分子的电子式_______ 。
(4)比较④⑤⑥简单离子半径从大到小依次为(用离子符号表示)_______
(5)用一个化学方程式证明①②的非金属性强弱_______
(6)到目前为止,元素周期表的第七周期已经被填满。请你设想一下,如果发现120号元素,下列有关它在周期表的位置或性质的说法错误的两项是_______ 。
a.在第八周期IIA族 b.最外层电子数是2
c.比钙的熔点高 d.与水反应放出氢气但比钙缓慢
e.该元素单质需隔绝空气密封保存 f.该元素的氧化物属于离子化合物
下表显示了元素周期表中短周期的一部分,①~⑥代表6种短周期元素。其中②与氢元素形成的简单氢化物分子中含10个电子,能够使湿润的红色石蕊试纸变蓝
| ① | ② | ③ | ||||
| ④ | ⑤ | ⑥ |
(2)与⑥同主族的第五周期元素的原子原子序数为
(3)写出元素③与氢形成18电子分子的电子式
(4)比较④⑤⑥简单离子半径从大到小依次为(用离子符号表示)
(5)用一个化学方程式证明①②的非金属性强弱
(6)到目前为止,元素周期表的第七周期已经被填满。请你设想一下,如果发现120号元素,下列有关它在周期表的位置或性质的说法错误的两项是
a.在第八周期IIA族 b.最外层电子数是2
c.比钙的熔点高 d.与水反应放出氢气但比钙缓慢
e.该元素单质需隔绝空气密封保存 f.该元素的氧化物属于离子化合物
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、C同周期,A、D同主族,A、C常温下能形成两种液态化合物A2C和A2C2,E元素的周期序数与主族序数相等。请用化学用语回答下列问题:
(1)E元素在周期表中的位置为___________ ,请写出E的最高价氧化物对应水化物的电离方程式:___________ 。
(2)C、D、E三种元素对应简单离子半径从大到小的顺序为(用离子符号表示) ___________>___________>___________,___________ ;由A、B、C三种元素组成的18电子微粒的分子式 为___________ 。
(3)用电子式表示BC2的形成过程:___________ 。
(4)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出该反应的离子方程式:___________ 。
(1)E元素在周期表中的位置为
(2)C、D、E三种元素对应简单离子半径从大到小的顺序为(用离子符号表示) ___________>___________>___________,
(3)用电子式表示BC2的形成过程:
(4)废印刷电路板上含有铜,以往的回收方法是将其灼烧使铜转化为氧化铜,再用硫酸溶解。现改用A2C2和稀硫酸浸泡废印刷电路板既达到上述目的,又保护了环境,试写出该反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】W、X、Y和Z都是周期表中前20号元素,其中W的原子序数均大于X、Y、Z,已知:
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为WY的化合物;
②Y和Z属同族元素,它们能形成两种常见化合物;
③X和Z属同一周期元素,它们能形成两种气态化合物;
④W和X能形成组成为WX2的化合物;
⑤X和Y不在同一周期,它们能形成组成为XY2的化合物。
请回答:
(1)W元素是________ ;Z元素是________ 。
(2)化合物WY和WX2的化学式分别是____________ 和 ____________ 。
(3)写出Y和Z形成的两种常见化合物之一的分子式是________________ 。
(4)写出X和Z形成的一种气态化合物跟WZ反应的化学方程式:____________________________________ 。
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为WY的化合物;
②Y和Z属同族元素,它们能形成两种常见化合物;
③X和Z属同一周期元素,它们能形成两种气态化合物;
④W和X能形成组成为WX2的化合物;
⑤X和Y不在同一周期,它们能形成组成为XY2的化合物。
请回答:
(1)W元素是
(2)化合物WY和WX2的化学式分别是
(3)写出Y和Z形成的两种常见化合物之一的分子式是
(4)写出X和Z形成的一种气态化合物跟WZ反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】现有部分短周期元素的性质或原子结构如下表:
(1)元素X位于元素周期表的第___________ 周期___________ 族,它的一种核素可测定文物年代,这种核素的符号是___________ 。
(2)元素Y的原子结构示意图为___________ 。
(3)元素Z与元素T相比,非金属性较强的是___________ (用元素符号表示),下列表述中能证明这一事实的是___________ (填字母)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一、T、X、Y、Z四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种的是___________ ,理由是___________ 。
| 元素编号 | 元素性质或原子结构 |
| T | M层电子数是K层电子数的3倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,是空气中含量最多的物质 |
| Z | 元素最高正价是+7价 |
(2)元素Y的原子结构示意图为
(3)元素Z与元素T相比,非金属性较强的是
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一、T、X、Y、Z四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
真题
解题方法
【推荐3】考生注意:下题为分叉题,分A、B两题,考生可任选一题。若两题均做,一律按A题计分。A题适合使用二期课改新教材的考生解答,B题适合使用一期课改教材的考生解答。
(A)现有部分短周期元素的性质或原子结构如下表:
(1)元素T的原子最外层共有______ 种不同运动状态的电子。元素X的一种同位素可测定文物年代,这种同位素的符号是___________
(2)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式_______________ (用元素符号表示)
(3)元素Z与元素T相比,非金属性较强的是________ (用元素符号表示),下列表述中能证明这一事实的是_______
a.常温下Z的单质和T的单质状态不同 b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是__________________ ,理由是
__________________________________________ 。
(B)现有部分短周期元素的性质或原子结构如下表:
(1)写出元素X的离子结构示意图______________ 。
写出元素Z的气态氢化物的电子式______________ (用元素符号表示)
(2)写出Y元素最高价氧化物水化物的电离方程式___________________________
(3)元素T与氯元素相比,非金属性较强的是___________ (用元素符号表示),下列表述中能证明这一事实的是________
a.常温下氯气的颜色比T单质的颜色深
b.T的单质通入氯化钠水溶液不能置换出氯气
c.氯与T形成的化合物中氯元素呈正价态
(4)探寻物质的性质差异性是学习的重要方法之—。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是_______ ,理由__________________________ 。
(A)现有部分短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| T | M层上有2对成对电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(2)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式
(3)元素Z与元素T相比,非金属性较强的是
a.常温下Z的单质和T的单质状态不同 b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是
(B)现有部分短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
写出元素Z的气态氢化物的电子式
(2)写出Y元素最高价氧化物水化物的电离方程式
(3)元素T与氯元素相比,非金属性较强的是
a.常温下氯气的颜色比T单质的颜色深
b.T的单质通入氯化钠水溶液不能置换出氯气
c.氯与T形成的化合物中氯元素呈正价态
(4)探寻物质的性质差异性是学习的重要方法之—。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素。A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应的水化物的化学式为HBO3;C元素原子的最外层电子数比次外层电子数多4个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E元素同主族。
(1)B在元素周期表中的位置是____ 。
(2)E元素形成的最高价氧化物对应的水化物的化学式为____ ,由C、D、E三种元素形成的离子化合物的化学式为____ 。
(3)C、D、E形成的简单离子的半径由大到小顺序是____ (用离子符号表示)。
(4)用电子式表示化合物D2E的形成过程____ ,化合物D2C2中的化学键类型是____ 。
(5)过量EC2与DCA溶液反应的离子方程式____ 。
(1)B在元素周期表中的位置是
(2)E元素形成的最高价氧化物对应的水化物的化学式为
(3)C、D、E形成的简单离子的半径由大到小顺序是
(4)用电子式表示化合物D2E的形成过程
(5)过量EC2与DCA溶液反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E、F六种元素分布在三个不同的短周期,他们的原子序数依次增大,其中 B与C为同一周期,A 与D,C与F分别在同一主族 ,A、D两元素原子核内的质子数之和是C、F两元素原子核内质子数之和的一半。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体,请回答下列问题:
(1)由A、B两种元素可以组成B2A4型化合物,该化合物中存在的共价键类型为是_________ 。写出该化合物的电子式______________
(2)E 是非金属元素,但能表现出一些金属元素的性质,写出E与D元素的最高价氧化物的水化物反应的离子方程式__________________________________ 。
(3)等浓度的ABC2溶液、HClO溶液、盐酸溶液,其导电能力:盐酸溶液>ABC2溶液>HClO溶液,则溶液的 pH (DBC2)____________ pH(DClO)(填“>、<、=”)理由是_________________________________________________ (用离子方程式解释)
(4)现有100.00mL 未知浓度的ABC2溶液,用_____________ (仪器名称)量取10.00mL待测溶液于锥形瓶中,加入几滴__________ (可选指示剂:酚酞、石蕊、甲基橙),用A、C、 D三种元素组成的浓度为0.10mol/L的标准溶液来测定未知浓度的ABC2溶液,判断滴定终点的现象是_______________________________ ;记录消耗标准溶液的体积为12.00mL,则该ABC2溶液的浓度为mol/L;
(1)由A、B两种元素可以组成B2A4型化合物,该化合物中存在的共价键类型为是
(2)E 是非金属元素,但能表现出一些金属元素的性质,写出E与D元素的最高价氧化物的水化物反应的离子方程式
(3)等浓度的ABC2溶液、HClO溶液、盐酸溶液,其导电能力:盐酸溶液>ABC2溶液>HClO溶液,则溶液的 pH (DBC2)
(4)现有100.00mL 未知浓度的ABC2溶液,用
您最近一年使用:0次




