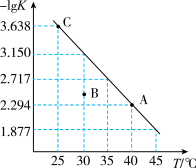
将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中, 发生反应 NH2COONH4(s)  2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是
2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是
 2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是
2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法错误的是
| A.C 点对应状态的平衡常数 K(C)=10-3.638 |
| B.该反应的ΔH>0 |
| C.混合气体的平均相对分子质量不变时,该反应一定达到平衡状态 |
D.30℃时,B 点对应状态的  < < |
更新时间:2020-08-28 17:25:10
|
【知识点】 化学平衡常数的影响因素及应用解读
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】已知:CO(g)+H2O(g)⇌H2(g)+CO2(g)∆H=-41. 2kJ·mol-1,850℃时在一体积为10L的恒容密闭容器中,通入一定量的CO和H2O,CO和H2O浓度变化如图所示。下列说法正确的是
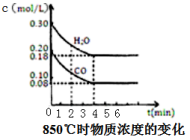

| A.达到平衡时,氢气的物质的量是0.12mol |
| B.达到平衡时,反应体系最终会放出49.44kJ热量 |
| C.第6min时,若升高温度,反应平衡常数会减小 |
| D.第8min时,若充入氦气,会导致v正(CO)<v逆(H2O) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】CO2催化加氢制取甲醇的研究,对于环境、能源问题都具有重要的意义。反应如下:
反应ⅰ:CO2(g) + 3H2(g) ⇌ CH3OH(g) + H2O(g) ∆H1 =﹣58 kJ· mol-1
反应ⅱ:CO2(g) + H2(g) ⇌ CO(g) + H2O(g) ∆H2 = +42 kJ· mol-1
下列说法不正确 的是
反应ⅰ:CO2(g) + 3H2(g) ⇌ CH3OH(g) + H2O(g) ∆H1 =﹣58 kJ· mol-1
反应ⅱ:CO2(g) + H2(g) ⇌ CO(g) + H2O(g) ∆H2 = +42 kJ· mol-1
下列说法
| A.增大氢气浓度能提高二氧化碳的转化率 |
| B.增大压强,有利于向生成甲醇的方向进行,反应ⅰ的平衡常数增大 |
| C.升高温度,生成甲醇的速率加快,反应ⅱ的限度同时增加 |
| D.选用理想的催化剂可以提高甲醇在最终产物中的比率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】在恒温恒压下,某一体积可变的密闭容器中发生反应A(g)+B(g) C(g) ΔH<0,t1时达到平衡后,在t2时改变某一条件,其反应过程如图所示。下列说法正确的是
C(g) ΔH<0,t1时达到平衡后,在t2时改变某一条件,其反应过程如图所示。下列说法正确的是

 C(g) ΔH<0,t1时达到平衡后,在t2时改变某一条件,其反应过程如图所示。下列说法正确的是
C(g) ΔH<0,t1时达到平衡后,在t2时改变某一条件,其反应过程如图所示。下列说法正确的是
| A.I、II两过程达到平衡时,A的体积分数:I>II |
| B.t2时改变的条件是向密闭容器中加入物质C |
| C.0~t2时,v正>v逆 |
| D.I、II两过程达到平衡时,平衡常数:K(I)<K(II) |
您最近一年使用:0次



