海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是( ) (填序号)。
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是____ 。
(3)图是从海水中提取镁的简单流程。

工业上常用于沉淀Mg2+的试剂A的俗名是____ ,氢氧化镁转化为MgCl2的离子方程式是_____ 。
(4)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如图所示:
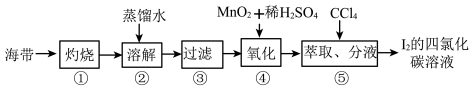
①灼烧海带至灰烬时所用的主要仪器名称是______ 。步骤②加热煮沸一会的目的是_____ 。
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式______ 。反应结束后,再加入CCl4作萃取剂,振荡、静置,可以观察到CCl4层呈_____ 色。
(1)无需经过化学变化就能从海水中获得的物质是
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是
(3)图是从海水中提取镁的简单流程。

工业上常用于沉淀Mg2+的试剂A的俗名是
(4)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如图所示:

①灼烧海带至灰烬时所用的主要仪器名称是
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
更新时间:2020-08-28 22:34:11
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】 常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备
常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备 的一种流程如下:
的一种流程如下:
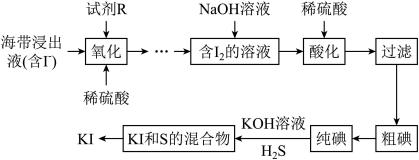
回答下列问题:
(1)“酸化”时稀硫酸的作用是___________ 。
(2)分离 和S的混合物得到
和S的混合物得到 溶液的试剂和方法如下,正确的是
溶液的试剂和方法如下,正确的是___________ (填标号)。
(3)利用下图装置完成 与
与 反应制备
反应制备 。
。

① 溶液的作用是
溶液的作用是___________ (用离子方程式表示)。
②三颈烧瓶中产生 的正确操作顺序为
的正确操作顺序为___________ (填标号)。
a.旋开活塞K,通入 b.加入稀硫酸 c.加入
b.加入稀硫酸 c.加入 溶液
溶液
(4)产品纯度测定。
准确称取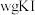 样品溶于水配成
样品溶于水配成 溶液,量取
溶液,量取 溶液于锥形瓶中,加入足量用稀硫酸酸化的
溶液于锥形瓶中,加入足量用稀硫酸酸化的 溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用
溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用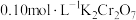 标准溶液反应至完全(还原产物只有
标准溶液反应至完全(还原产物只有 ),消耗标准溶液
),消耗标准溶液 。该
。该 产品的纯度为
产品的纯度为___________ (用含w,V的式子表示)。
 常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备
常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备 的一种流程如下:
的一种流程如下:
回答下列问题:
(1)“酸化”时稀硫酸的作用是
(2)分离
 和S的混合物得到
和S的混合物得到 溶液的试剂和方法如下,正确的是
溶液的试剂和方法如下,正确的是| 选项 | 试剂 | 方法 |
| a | 二硫化碳 | 分液 |
| b | 酒精 | 分液 |
| c |  溶液 溶液 | 过滤 |
(3)利用下图装置完成
 与
与 反应制备
反应制备 。
。
①
 溶液的作用是
溶液的作用是②三颈烧瓶中产生
 的正确操作顺序为
的正确操作顺序为a.旋开活塞K,通入
 b.加入稀硫酸 c.加入
b.加入稀硫酸 c.加入 溶液
溶液(4)产品纯度测定。
准确称取
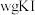 样品溶于水配成
样品溶于水配成 溶液,量取
溶液,量取 溶液于锥形瓶中,加入足量用稀硫酸酸化的
溶液于锥形瓶中,加入足量用稀硫酸酸化的 溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用
溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用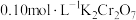 标准溶液反应至完全(还原产物只有
标准溶液反应至完全(还原产物只有 ),消耗标准溶液
),消耗标准溶液 。该
。该 产品的纯度为
产品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验(苯,一种不溶于水,密度比水小的液体):
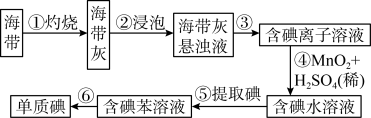
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是_______ (从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是_______ ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是_______ 。
(3)步骤⑤是萃取、分液,某学生选择用苯来提取碘的理由是_________ ;萃取后,上层液体呈_________ 色,下层液体呈_________ 色。

请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是
(3)步骤⑤是萃取、分液,某学生选择用苯来提取碘的理由是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】开发和利用海洋资源是当前科学研究的一项重要任务,如图是某化工厂对海洋资源综合利用的流程图:
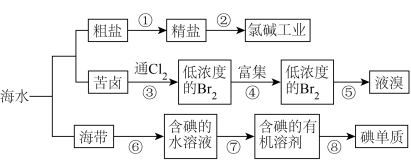
请回答下列问题:
(1)粗盐中含有泥沙、 、
、 、
、 等杂质,精制时一般步骤如下:
等杂质,精制时一般步骤如下:
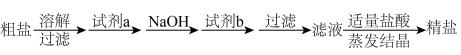
加入的试剂a、b分别是___________ 、___________ 。
(2)③中发生反应的离子方程式为___________ ,可推断氧化性:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(3)⑥通常分三个步骤:
第1步:灼烧,将足量海带灼烧成灰烬;
第2步: 溶液的获取;
溶液的获取;
第3步:氧化。
下列仪器在第1步中不会用到的有___________ 。
A.试管B.瓷坩埚C.坩埚钳D.铁三脚架E.泥三角F.酒精灯G.烧杯H.量筒
第3步中最好选用的氧化剂是___________ 。
A.浓硫酸B.新制氯水C.酸性高锰酸钾D.
(4)⑦中所用的操作方法有___________ 、___________ 。

请回答下列问题:
(1)粗盐中含有泥沙、
 、
、 、
、 等杂质,精制时一般步骤如下:
等杂质,精制时一般步骤如下:
加入的试剂a、b分别是
(2)③中发生反应的离子方程式为

 (填“>”或“<”)。
(填“>”或“<”)。(3)⑥通常分三个步骤:
第1步:灼烧,将足量海带灼烧成灰烬;
第2步:
 溶液的获取;
溶液的获取;第3步:氧化。
下列仪器在第1步中不会用到的有
A.试管B.瓷坩埚C.坩埚钳D.铁三脚架E.泥三角F.酒精灯G.烧杯H.量筒
第3步中最好选用的氧化剂是
A.浓硫酸B.新制氯水C.酸性高锰酸钾D.

(4)⑦中所用的操作方法有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】海洋是一个巨大的化学资源宝库,下面是海水资源综合利用的部分流程图,请根据该图回答下列问题:
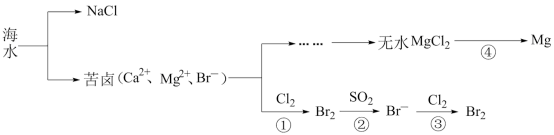
(1)淡化海水的方法有___ (写一种合理方法即可)。由海水提取的粗盐中含有Ca2+、Mg2+、SO 等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、
等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、___ (填化学式),之后___ (填操作名称),再加入适量___ (填试剂名称)。将所得溶液加热浓缩、冷却结晶,得到精盐。
(2)反应④由无水MgCl2制取金属镁的常用工业方法是___ 。
(3)向苦卤中通入Cl2置换出Br2,再用空气吹出溴并用SO2吸收,转化为Br-,反复多次,以达到富集溴的目的。由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由强到弱的顺序是___ 。
(4)工业上也可以用Na2CO3溶液吸收吹出的Br2,生成溴化钠和溴酸钠,同时放出CO2。写出反应的离子方程式___ ,最后再用H2SO4处理所得溶液重新得到Br2。

(1)淡化海水的方法有
 等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、
等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、(2)反应④由无水MgCl2制取金属镁的常用工业方法是
(3)向苦卤中通入Cl2置换出Br2,再用空气吹出溴并用SO2吸收,转化为Br-,反复多次,以达到富集溴的目的。由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由强到弱的顺序是
(4)工业上也可以用Na2CO3溶液吸收吹出的Br2,生成溴化钠和溴酸钠,同时放出CO2。写出反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】海洋资源的利用具有广阔前景。
I.海带中含有丰富的碘元素。灼烧海带获取的海带灰中碘元素主要以I-形式存在。在实验室中,从海带灰中提取碘的流程如图:
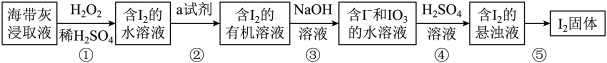
回答下列问题:
(1)实验室灼烧海带的主要仪器有酒精灯、三脚架、泥三角、坩埚钳、___________ (填名称)。
(2)步骤①中选择H2O2氧化I-,不用Cl2的原因是___________ 。
(3)步骤④中反应的离子方程式为___________ ,在此反应中,每生成38.1g I2转移电子的数目为___________ 。
(4)上述流程中,含I2的水溶液经3步转化为含I2的悬浊液,主要目的是___________ 。
II.如图是某工厂对海水资源进行综合利用的示意图。

回答下列问题:
(5)往母液中加石灰乳发生反应的离子方程式为___________ 。
(6)由MgCl2溶液得到MgCl2·6H2O晶体的操作是___________ ,过滤、洗涤、干燥。
(7)操作b需在HCl气流氛围中进行,若在空气中加热,则会水解生成Mg(OH)2,写出在空气中加热MgCl2·6H2O的化学方程式___________ 。
(8)由MgCl2制备金属镁的冶炼方法为___________ (填名称)。
I.海带中含有丰富的碘元素。灼烧海带获取的海带灰中碘元素主要以I-形式存在。在实验室中,从海带灰中提取碘的流程如图:

回答下列问题:
(1)实验室灼烧海带的主要仪器有酒精灯、三脚架、泥三角、坩埚钳、
(2)步骤①中选择H2O2氧化I-,不用Cl2的原因是
(3)步骤④中反应的离子方程式为
(4)上述流程中,含I2的水溶液经3步转化为含I2的悬浊液,主要目的是
II.如图是某工厂对海水资源进行综合利用的示意图。

回答下列问题:
(5)往母液中加石灰乳发生反应的离子方程式为
(6)由MgCl2溶液得到MgCl2·6H2O晶体的操作是
(7)操作b需在HCl气流氛围中进行,若在空气中加热,则会水解生成Mg(OH)2,写出在空气中加热MgCl2·6H2O的化学方程式
(8)由MgCl2制备金属镁的冶炼方法为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】海洋中储有大量的化学物质,储量可观的化学元素就有80多种,其中70多种可以被人类提取利用,全世界每年都要从海洋中提取大量的食盐、铁、溴、碘、钾等有用物质,海水被誉为“液体工业原料”。从海水中提取食盐、镁和溴的流程如图所示。回答下列问题:
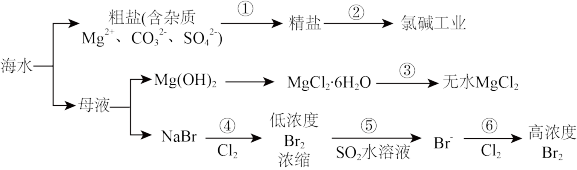
(1)从海水中得到的粗盐中含Mg2+、Ca2+、 等杂质离子,如用试剂BaCl2、NaOH、盐酸和Na2CO3溶液,除去杂质离子,则加入试剂的顺序是
等杂质离子,如用试剂BaCl2、NaOH、盐酸和Na2CO3溶液,除去杂质离子,则加入试剂的顺序是_______ 。
(2)氨碱工业的主要反应是电解饱和氯化钠溶液,写出反应的离子方程式_______ 。
(3)MgCl2·6H2O脱水过程中易水解生成碱式氯化镁,涉及的离子方程式为_______ 。因此工业上常使MgCl2·6H2O晶体在_______ 气体中脱水而得到干燥无水的MgCl2。
(4)第⑤步是用热空气将Br2吹入SO2溶液中,写出反应的化学方程式_______ 。
(5)电解无水MgCl2可得金属镁和氯气,利用副产品氯气还可制备漂白粉,其反应的化学方程式为_______ 。
(6)步骤④中用硫酸酸化可提高Cl2的利用率,理由是_______ 。含高浓度Br2的水溶液经过蒸馏可得到Br2,蒸馏的温度为80~90℃,温度过高或过低都不利于生产,请解释原因:_______ 。

(1)从海水中得到的粗盐中含Mg2+、Ca2+、
 等杂质离子,如用试剂BaCl2、NaOH、盐酸和Na2CO3溶液,除去杂质离子,则加入试剂的顺序是
等杂质离子,如用试剂BaCl2、NaOH、盐酸和Na2CO3溶液,除去杂质离子,则加入试剂的顺序是(2)氨碱工业的主要反应是电解饱和氯化钠溶液,写出反应的离子方程式
(3)MgCl2·6H2O脱水过程中易水解生成碱式氯化镁,涉及的离子方程式为
(4)第⑤步是用热空气将Br2吹入SO2溶液中,写出反应的化学方程式
(5)电解无水MgCl2可得金属镁和氯气,利用副产品氯气还可制备漂白粉,其反应的化学方程式为
(6)步骤④中用硫酸酸化可提高Cl2的利用率,理由是
您最近一年使用:0次



