下列有关碱金属元素和卤素的说法中,错误的是
A.溴单质与 的反应比碘单质与 的反应比碘单质与 的反应更剧烈 的反应更剧烈 |
| B.碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子的能力最强 |
| C.钾与水的反应比钠与水的反应更剧烈 |
| D.随着核电荷数的增加,卤素单质的熔、沸点逐渐降低 |
更新时间:2020-09-08 12:29:53
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列各组物质的性质的比较结论正确的是
A.分子的极性: | B.常温下密度:Na<K |
| C.物质的沸点:HF<HCl | D.在甲苯中的溶解度: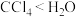 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关碱金属、卤素原子结构和性质的描述,正确的个数为
①随着核电荷数的增加,碱金属单质的熔、沸点依次升高,密度依次增大
② 、
、 、
、 、
、 的最外层电子数都是7,次外层电子数都是8
的最外层电子数都是7,次外层电子数都是8
③碱金属单质的金属性很强,均易与氧气发生反应,加热时生成的氧化物形式为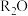
④根据同族元素性质的递变规律推测,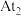 与
与 化合较难,破化银也难溶于水
化合较难,破化银也难溶于水
⑤根据 、
、 、
、 的非金属性依次减弱,可推出
的非金属性依次减弱,可推出 、
、 、
、 的酸性依次减弱
的酸性依次减弱
⑥碱金属都应保存在煤油中
⑦卤素按 、
、 、
、 、
、 的顺序非金属性逐渐减弱的原因是随着核电荷数的增加,电子层数增多,原子半径增大
的顺序非金属性逐渐减弱的原因是随着核电荷数的增加,电子层数增多,原子半径增大
⑧碳酸铯不易发生分解反应生成氧化铯和二氧化碳
①随着核电荷数的增加,碱金属单质的熔、沸点依次升高,密度依次增大
②
 、
、 、
、 、
、 的最外层电子数都是7,次外层电子数都是8
的最外层电子数都是7,次外层电子数都是8③碱金属单质的金属性很强,均易与氧气发生反应,加热时生成的氧化物形式为
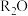
④根据同族元素性质的递变规律推测,
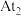 与
与 化合较难,破化银也难溶于水
化合较难,破化银也难溶于水⑤根据
 、
、 、
、 的非金属性依次减弱,可推出
的非金属性依次减弱,可推出 、
、 、
、 的酸性依次减弱
的酸性依次减弱⑥碱金属都应保存在煤油中
⑦卤素按
 、
、 、
、 、
、 的顺序非金属性逐渐减弱的原因是随着核电荷数的增加,电子层数增多,原子半径增大
的顺序非金属性逐渐减弱的原因是随着核电荷数的增加,电子层数增多,原子半径增大⑧碳酸铯不易发生分解反应生成氧化铯和二氧化碳
| A.2 | B.3 | C.4 | D.5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列对碱金属的叙述正确的是
①K通常保存在煤油中以隔绝与空气的接触
②碱金属常温下呈固态,取用时可直接用手拿
③碱金属中还原性最弱的是锂
④碱金属阳离子中氧化性最强的是
⑤碱金属的原子半径随核电荷数的增大而增大
⑥从 到
到 ,碱金属的密度越来越大,熔、沸点越来越低
,碱金属的密度越来越大,熔、沸点越来越低
①K通常保存在煤油中以隔绝与空气的接触
②碱金属常温下呈固态,取用时可直接用手拿
③碱金属中还原性最弱的是锂
④碱金属阳离子中氧化性最强的是

⑤碱金属的原子半径随核电荷数的增大而增大
⑥从
 到
到 ,碱金属的密度越来越大,熔、沸点越来越低
,碱金属的密度越来越大,熔、沸点越来越低| A.①③④⑤ | B.②③⑤⑥ | C.①②③④ | D.①②③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】卤素互化物具有和卤素相似的化学性质。下列有关BrCl的说法错误的是
| A.BrCl中的溴元素显+1价 |
| B.BrCl中的原子均符合8电子稳定结构 |
| C.BrCl、Cl2、Br2 的熔、沸点大小:Br2>BrCl>Cl2 |
| D.BrCl与 H2O 反应的生成物为 HBr和 HClO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】结合元素周期律,判断下列各组中的性质比较,错误的是
| A.最高正化合价:N>C>B | B.酸性:HClO4>H2SO4>H3PO4 |
| C.原子半径大小:S>Na>O | D.碱性强弱: KOH>NaOH>LiOH |
您最近一年使用:0次

 为共价晶体,推测
为共价晶体,推测 也是共价晶体
也是共价晶体 也是直线型分子
也是直线型分子 的沸点高于
的沸点高于 ,推测
,推测 的沸点高于
的沸点高于


