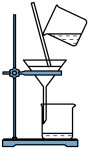
下列有关实验的叙述正确的是
| A.用水润湿的pH试纸来测量溶液的pH |
| B.实验需要480mL2.0mol•L-1的氢氧化钠溶液.配制该溶液时先称量氢氧化钠固体38.4g,然后再按照溶解、冷却、移液、洗涤、定容、摇匀的步骤进行操作 |
| C.用溴水,淀粉、KI溶液比较Br2与I2的氧化性强弱,所需玻璃仪器主要有:试管、胶头滴管 |
D.向溶液中滴加盐酸酸化的Ba(NO3)2溶液出现白色沉淀,说明溶液中一定有 |
更新时间:2020-09-08 16:11:02
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】为了证明(NH4)2Fe(SO4)2·6H2O(硫酸亚铁铵晶体)的成分中含有NH4+、Fe2+、SO42-和H2O,下列实验叙述中不正确的是
| A.取少量硫酸亚铁铵晶体放入试管,加热,试管口有液体生成,则可证明晶体的成分中含有结晶水 |
| B.硫酸亚铁铵晶体溶于水,得淡绿色溶液,滴入2滴KSCN溶液,溶液不显红色,再滴入几滴新制氯水,溶液变为红色,则可证明晶体的成分中含有Fe2+ |
| C.硫酸亚铁铵晶体溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42- |
| D.取少量硫酸亚铁铵晶体放入试管,加入少量稀NaOH溶液,在试管口用湿润的红色石蕊试纸检验,则可证明晶体的成分中含有NH4+ |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】为了检验 ,甲、乙、丙、丁四位同学设计了如下四种方案,其中方案最优的是
,甲、乙、丙、丁四位同学设计了如下四种方案,其中方案最优的是
 ,甲、乙、丙、丁四位同学设计了如下四种方案,其中方案最优的是
,甲、乙、丙、丁四位同学设计了如下四种方案,其中方案最优的是A.方案甲:试液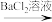 白色沉淀 白色沉淀 沉淀不溶解 沉淀不溶解 |
B.方案乙:试液 无沉淀(也无气泡) 无沉淀(也无气泡)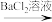 白色沉淀 白色沉淀 |
C.方案丙:试液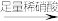 无沉淀 无沉淀 白色沉淀 白色沉淀 |
D.方案丁:试液 白色沉淀(过滤) 白色沉淀(过滤) 沉淀不溶解 沉淀不溶解 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列说法正确的是
| A.配制一定物质的量浓度的NaOH溶液时,NaOH固体溶解后未恢复到室温就转移、定容,所配制的溶液浓度偏大 |
| B.用广泛pH试纸测得氯水的pH为3 |
| C.用托盘天平称取5.86g食盐 |
| D.用细铁丝放在酒精灯火焰上灼烧至无色,然后蘸取少量待测液,透过蓝色钴玻璃观察火焰呈紫色,说明待测液中一定含有K+,没有Na+ |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】用下列实验装置进行相应实验,能达到实验目的的是(夹持装置未画出)
A.转移溶液 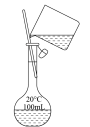 | B.萃取分液  |
C.稀释浓硫酸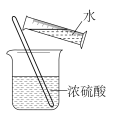 | D.加热熔融NaOH固体 |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】进行化学实验时,下列仪器可直接用酒精灯加热的是
A. | B. | C.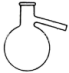 | D. |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列实验操作中,没有错误 的是
| A.pH试纸测出稀盐酸的pH为3.5 |
| B.用量筒取8.60mL的水 |
| C.实验室制O2时,先检查装置的气密性再装药品 |
| D.称量氢氧化钠时,将氢氧化钠直接放在纸上进行称量 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列有关实验操作中,正确的是
| A.用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 |
| B.自来水中氯离子的检验:取少量自来水于试管中,加入硝酸银溶液,产生白色沉淀,说明有氯离子 |
| C.用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干 |
| D.温度计水银球打破的时候,要在水银表面上撒硫磺粉,再打扫干净 |
您最近半年使用:0次