硫氰化铵在一定条件下发生如下转化,下列相关物质的说法正确的是
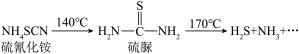

| A.鉴别硫氰化铵与硫脲可用FeCl3溶液 | B.H2S在水中的电离方程式为H2S⇌2H++S2- |
| C.NH3只有还原性没有氧化性 | D.非金属性N>C,因此沸点NH3>CH4 |
更新时间:2020-09-09 16:00:48
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列物质形成的水溶液中,所含微粒种类最少的是
A. | B. | C. | D. |
您最近一年使用:0次
【推荐2】实验室可利用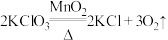 制取氧气,下列说法正确的是
制取氧气,下列说法正确的是
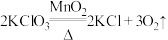 制取氧气,下列说法正确的是
制取氧气,下列说法正确的是A. 的结构示意图: 的结构示意图: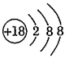 |
| B.KClO3、KCl、MnO2均为盐 |
C.KClO3电离方程式: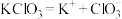 |
D.单线桥表示Na在O2中燃烧的电子转移过程: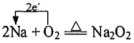 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某白色固体混合物可能含有Ba(NO3)2、CaCl2、K2CO3,现进行如下实验:
①将部分粉末加入水中,振荡,有白色沉淀;
②向①的悬浊液中加入过量的稀硝酸,白色沉淀消失,并有气泡产生;
③取少量②的溶液滴入AgNO3溶液,有白色沉淀生成。
下列判断正确的是
①将部分粉末加入水中,振荡,有白色沉淀;
②向①的悬浊液中加入过量的稀硝酸,白色沉淀消失,并有气泡产生;
③取少量②的溶液滴入AgNO3溶液,有白色沉淀生成。
下列判断正确的是
| A.若做焰色反应,通过蓝色钴玻璃可观察到紫色 |
B.②中现象对应的离子方程式为CO +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
| C.白色固体中一定含有Ba(NO3)2、K2CO3,可能含有CaCl2 |
| D.将步骤②中的稀硝酸改用稀盐酸,对整个实验结果没有影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某100mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法不正确的是


| A.原溶液一定存在CO32-和SO42-,一定不存在Fe3+ |
| B.原溶液一定存在Cl-,可能存在Na+ |
| C.原溶液中c(CO32-)是0.1mol·L-1 |
| D.若原溶液中不存在Na+,则c(Cl-)<0.1mol·L-1 |
您最近一年使用:0次
【推荐1】实验室利用Bi(OH)3制取高锰酸钠的相关反应的离子方程式如下:
I.ClO +6H++5Cl-=3Cl2+3H2O;
+6H++5Cl-=3Cl2+3H2O;
II.Bi(OH)3+3OH-+Cl2+Na+=NaBiO3↓+2Cl-+3H2O;
III.5NaBiO3+2Mn2++14H+=2MnO +5Bi3++5Na++7H2O。
+5Bi3++5Na++7H2O。
下列说法正确的是
A.反应I中氧化产物和还原产物的物质的量比为1∶5
B.酸性条件下的氧化性:ClO > Cl2 > NaBiO3 > MnO
> Cl2 > NaBiO3 > MnO
C.NaBiO3可与盐酸发生反应:NaBiO3+6H++2Cl-=Bi3++Cl2↑+3H2O+Na+
D.制得142g高锰酸钠时,理论上消耗氯酸钠的物质的量为1mol
I.ClO
 +6H++5Cl-=3Cl2+3H2O;
+6H++5Cl-=3Cl2+3H2O;II.Bi(OH)3+3OH-+Cl2+Na+=NaBiO3↓+2Cl-+3H2O;
III.5NaBiO3+2Mn2++14H+=2MnO
 +5Bi3++5Na++7H2O。
+5Bi3++5Na++7H2O。下列说法正确的是
A.反应I中氧化产物和还原产物的物质的量比为1∶5
B.酸性条件下的氧化性:ClO
 > Cl2 > NaBiO3 > MnO
> Cl2 > NaBiO3 > MnO
C.NaBiO3可与盐酸发生反应:NaBiO3+6H++2Cl-=Bi3++Cl2↑+3H2O+Na+
D.制得142g高锰酸钠时,理论上消耗氯酸钠的物质的量为1mol
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是硫元素在自然界中的循环示意图,下列有关说法错误的是
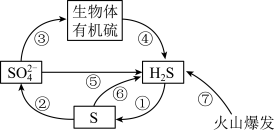

| A.硫元素的循环过程中既有硫的还原也有硫的氧化 |
| B.硫在自然界中既有游离态又有化合态 |
| C.过程②宜在土壤的缺氧区实现 |
D.若生物体有机硫的成键方式为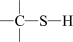 ,则过程④中 ,则过程④中 未发生氧化还原反应 未发生氧化还原反应 |
您最近一年使用:0次

 S2–+H3O+
S2–+H3O+

