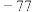凯氏定氮法是测定蛋白质中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐,再通过滴定测量。已知:NH3+ H3BO3=NH3·H3BO3;NH3·H3BO3+ HCl = NH4Cl + H3BO3。
回答下列问题:
(1)a的作用是___________________________ 。
(2)b中放入少量碎瓷片的目的是____________ 。f的名称是_______________ 。
(3)清洗仪器:g中加蒸馏水;打开k1,关闭k2、k3,加热b,蒸气充满管路;停止加热,关闭k1,g中蒸馏水倒吸进入c,原因是________________________________________ 。打开k2放掉水,重复操作2~3次。
(4)仪器清洗后,g中加入硼酸(H3BO3)和指示剂。铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭k3,d中保留少量水。打开k1,加热b,使水蒸气进入e。
①d中保留少量水的目的是____________________________ 。
②e中主要反应的离子方程式为.____________________________________________ ,e采用中空双层玻璃瓶的作用是___________________________________ 。
(5)取某甘氨酸(C2H5NO2)样品mg进行测定,滴定g中吸收液时消耗浓度为cmol·L-1的盐酸VmL,则样品中氮的质量分数为__________________________ (不需化简),选择指示剂为____________________ 。

回答下列问题:
(1)a的作用是
(2)b中放入少量碎瓷片的目的是
(3)清洗仪器:g中加蒸馏水;打开k1,关闭k2、k3,加热b,蒸气充满管路;停止加热,关闭k1,g中蒸馏水倒吸进入c,原因是
(4)仪器清洗后,g中加入硼酸(H3BO3)和指示剂。铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭k3,d中保留少量水。打开k1,加热b,使水蒸气进入e。
①d中保留少量水的目的是
②e中主要反应的离子方程式为.
(5)取某甘氨酸(C2H5NO2)样品mg进行测定,滴定g中吸收液时消耗浓度为cmol·L-1的盐酸VmL,则样品中氮的质量分数为
更新时间:2020-09-13 12:23:39
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】硫代硫酸钠(Na2S2O3)为白色结晶粉末,易溶于水,在中性或碱性条件下稳定,在酸性条件下发生反应(S2O32-+2H+=S↓+SO2+H2O),是一种重要的化工原料。请回答下列问题:
(1)Na2S2O3溶液可用作照相底片(AgBr)中的定影剂,其原理是将未感光的AgBr转化为可溶于水的稳定络合物Na3[Ag(S2O3)2]。写出该络合反应的离子方程式___ 。
(2)工业上利用硫化碱残渣(主要成分Na2S,Na2CO3)与硫黄废气(主要成分SO2)反应,经吸硫、蒸发、结晶,制得硫代硫酸钠。已知该反应中C(碳)原子化合价不变,则氧化剂和还原剂物质的量之比为___ 。
(3)Na2S2O3长期暴露在空气中易被氧化生成Na2SO4,设计实验方案检验Na2S2O3是否变质(已知BaS2O3微溶于水)___ 。
(4)现有含Na2S2O3·5H2O的样品,用以下方法计算Na2S2O3·5H2O的质量分数。
a.取样品7.0g溶于蒸馏水中,并定容至500mL容量瓶中待用。
b.取0.01mol.L-1的K2Cr2O7标准溶液20.00mL于锥形瓶中,加过量KI溶液并酸化,加2滴淀粉指示剂,用a中未知浓度的Na2S2O3待测液滴定至终点,共用去25.00mL。(已知2S2O32-+I2=S4O62-+2I-),在酸性环境中Cr2O72-被还原为绿色的Cr3+)。
回答下列问题:
①滴定终点的现象是___ 。
②样品中Na2S2O3·5H2O的质量分数为___ (保留2位有效数字)。
(1)Na2S2O3溶液可用作照相底片(AgBr)中的定影剂,其原理是将未感光的AgBr转化为可溶于水的稳定络合物Na3[Ag(S2O3)2]。写出该络合反应的离子方程式
(2)工业上利用硫化碱残渣(主要成分Na2S,Na2CO3)与硫黄废气(主要成分SO2)反应,经吸硫、蒸发、结晶,制得硫代硫酸钠。已知该反应中C(碳)原子化合价不变,则氧化剂和还原剂物质的量之比为
(3)Na2S2O3长期暴露在空气中易被氧化生成Na2SO4,设计实验方案检验Na2S2O3是否变质(已知BaS2O3微溶于水)
(4)现有含Na2S2O3·5H2O的样品,用以下方法计算Na2S2O3·5H2O的质量分数。
a.取样品7.0g溶于蒸馏水中,并定容至500mL容量瓶中待用。
b.取0.01mol.L-1的K2Cr2O7标准溶液20.00mL于锥形瓶中,加过量KI溶液并酸化,加2滴淀粉指示剂,用a中未知浓度的Na2S2O3待测液滴定至终点,共用去25.00mL。(已知2S2O32-+I2=S4O62-+2I-),在酸性环境中Cr2O72-被还原为绿色的Cr3+)。
回答下列问题:
①滴定终点的现象是
②样品中Na2S2O3·5H2O的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
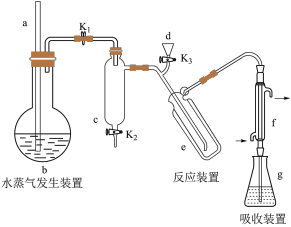
【推荐2】三氯乙醛( )是无色油状液体,是制取农药的常用原料。某小组探究制备三氯乙醛的实验装置如图所示(夹持、加热装置均略去)。
)是无色油状液体,是制取农药的常用原料。某小组探究制备三氯乙醛的实验装置如图所示(夹持、加热装置均略去)。
已知:①制备原理: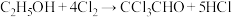 ,(保持70℃左右)
,(保持70℃左右)
②有关物质的性质:
请回答:
(1)仪器a的名称为_______ 。若发现D中导管口处气泡速率过快,合理的解决方法是_______ 。
(2)下列说法不正确的是_______。
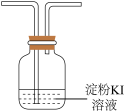
(3)若撤去装置C会导致 产率降低,原因是
产率降低,原因是_______ 。
(4)粗产品纯度的测定:称取5.00g粗产品溶于水配成100mL溶液,量取10.00mL于锥形瓶中,加入25.00mL 碘标准溶液,再加入适量
碘标准溶液,再加入适量 溶液。反应完全后加适量盐酸调节溶液的pH,立即用
溶液。反应完全后加适量盐酸调节溶液的pH,立即用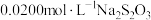 溶液滴定至淡黄色,加入淀粉指示剂,继续滴定至终点。重复上述操作3次,平均消耗
溶液滴定至淡黄色,加入淀粉指示剂,继续滴定至终点。重复上述操作3次,平均消耗 溶液20.00mL。(测定原理:
溶液20.00mL。(测定原理: 、
、 、
、 )
)
①选出正确的滴定操作并排序:检查是否漏水→蒸馏水洗涤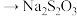 标准溶液润洗滴定管→
标准溶液润洗滴定管→_______ →到达滴定终点,停止滴定,记录读数。
a.调整管中液面至“0”或“0”刻度以下,记录读数
b.调整管中液面,用胶头滴管滴加标准液恰好到“0”刻度
c.锥形瓶放于滴定管下,边滴边摇动锥形瓶,眼睛注视锥形瓶内颜色变化
d.装入标准液至“0”刻度以上2~3mL,固定好滴定管
e.锥形瓶放于滴定管下,边滴边摇动锥形瓶,眼睛注视滴定管内液面变化
f.如图操作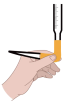 ,排出滴定管尖嘴部分的气泡
,排出滴定管尖嘴部分的气泡
g.如图操作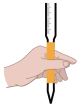 ,排出滴定管尖嘴部分的气泡
,排出滴定管尖嘴部分的气泡
②产品的纯度是_______ %(计算结果保留2位小数)
 )是无色油状液体,是制取农药的常用原料。某小组探究制备三氯乙醛的实验装置如图所示(夹持、加热装置均略去)。
)是无色油状液体,是制取农药的常用原料。某小组探究制备三氯乙醛的实验装置如图所示(夹持、加热装置均略去)。
已知:①制备原理:
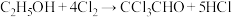 ,(保持70℃左右)
,(保持70℃左右)②有关物质的性质:
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | 密度/ | |
| 乙醇 | 46 | -117 | 78.5 | 与水互溶 | 0.789 |
| 三氯乙醛 | 147.5 | -57.5 | 97.8 | 溶于水、乙醇 | 1.51 |
(1)仪器a的名称为
(2)下列说法不正确的是_______。

| A.本实验较合理的加热方式是水浴加热 |
| B.多孔球泡可以增大反应物接触面积,提高反应速率 |
| C.为证明D中产生HCl,需要在D和E之间增加装置(如图) |
| D.反应后的混合物可采用分液操作进一步分离、提纯三氯乙醛 |
 产率降低,原因是
产率降低,原因是(4)粗产品纯度的测定:称取5.00g粗产品溶于水配成100mL溶液,量取10.00mL于锥形瓶中,加入25.00mL
 碘标准溶液,再加入适量
碘标准溶液,再加入适量 溶液。反应完全后加适量盐酸调节溶液的pH,立即用
溶液。反应完全后加适量盐酸调节溶液的pH,立即用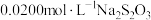 溶液滴定至淡黄色,加入淀粉指示剂,继续滴定至终点。重复上述操作3次,平均消耗
溶液滴定至淡黄色,加入淀粉指示剂,继续滴定至终点。重复上述操作3次,平均消耗 溶液20.00mL。(测定原理:
溶液20.00mL。(测定原理: 、
、 、
、 )
)①选出正确的滴定操作并排序:检查是否漏水→蒸馏水洗涤
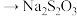 标准溶液润洗滴定管→
标准溶液润洗滴定管→a.调整管中液面至“0”或“0”刻度以下,记录读数
b.调整管中液面,用胶头滴管滴加标准液恰好到“0”刻度
c.锥形瓶放于滴定管下,边滴边摇动锥形瓶,眼睛注视锥形瓶内颜色变化
d.装入标准液至“0”刻度以上2~3mL,固定好滴定管
e.锥形瓶放于滴定管下,边滴边摇动锥形瓶,眼睛注视滴定管内液面变化
f.如图操作
 ,排出滴定管尖嘴部分的气泡
,排出滴定管尖嘴部分的气泡g.如图操作
 ,排出滴定管尖嘴部分的气泡
,排出滴定管尖嘴部分的气泡②产品的纯度是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】己二酸是合成尼龙-66的主要原料之一, 通常为白色结晶体,微溶于冷水,易溶于热水和乙醇,环己醇熔点为24°C,熔融时为粘稠液体,易附着在玻璃容器内壁上。实验室中可利用环己醇与硝酸制备己二酸,反应原理为 (未配平,为强烈放热反应),制备装置如图所示(夹持、加热装置省略)。
(未配平,为强烈放热反应),制备装置如图所示(夹持、加热装置省略)。
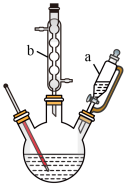
实验步骤:
①向三颈烧瓶中加入16 mL 50%的硝酸,加入少量偏钒酸铵作催化剂,向滴液漏斗a内加入环己醇5.2mL(5.0g)。
②将三颈烧瓶水浴加热至约60°C,撤去水浴,搅拌,慢慢滴入环己醇;边搅拌边严格控制滴加速度,保持三颈烧瓶内温度在50~60°C。
③滴加完环己醇(约需30min)后,再用80~90°C的热水浴保持2h。
④冷却至室温后,在冰水浴中冷却、抽滤(减压过滤)、洗涤、重结晶、干燥,获得产品。
回答下列问题:
(1)环己醇在取用时___________ (填“需要”“不需要”)用蒸馏水冲洗量筒,图中实验装置的不足之处为___________ 。
(2)步骤②中标志着反应已经开始的现象是_______________________ ;边搅拌边严格控制滴加速度的目的是___________ 。
(3)可以替代硝酸的试剂为___________。
(4)己二酸溶液的浓度与温度的关系曲线如图所示。
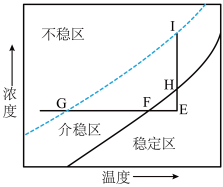
介稳区表示己二酸溶液处于饱和状态,稳定区表示己二酸溶液处于___________ 状态。重结晶时,实验室常根据直线EHI从溶液中获取己二酸晶体,对应的实验操作为 ___________ 、过滤。
(5)称取实验所得产品0.292g于锥形瓶中,用煮沸的50.00 mL热水溶解,滴加2滴指示剂,用0.150 mol·L-1NaOH标准溶液滴定,进行三次平行实验,平均消耗NaOH标准溶液的体积为20.00mL。滴定时所选用的指示剂为___________ , 己二酸的纯度为___________ 。
 (未配平,为强烈放热反应),制备装置如图所示(夹持、加热装置省略)。
(未配平,为强烈放热反应),制备装置如图所示(夹持、加热装置省略)。
实验步骤:
①向三颈烧瓶中加入16 mL 50%的硝酸,加入少量偏钒酸铵作催化剂,向滴液漏斗a内加入环己醇5.2mL(5.0g)。
②将三颈烧瓶水浴加热至约60°C,撤去水浴,搅拌,慢慢滴入环己醇;边搅拌边严格控制滴加速度,保持三颈烧瓶内温度在50~60°C。
③滴加完环己醇(约需30min)后,再用80~90°C的热水浴保持2h。
④冷却至室温后,在冰水浴中冷却、抽滤(减压过滤)、洗涤、重结晶、干燥,获得产品。
回答下列问题:
(1)环己醇在取用时
(2)步骤②中标志着反应已经开始的现象是
(3)可以替代硝酸的试剂为___________。
| A.酸性KMnO4 | B.Na2S2O3 | C.维生素C | D.酸性K2Cr2O7 |

介稳区表示己二酸溶液处于饱和状态,稳定区表示己二酸溶液处于
(5)称取实验所得产品0.292g于锥形瓶中,用煮沸的50.00 mL热水溶解,滴加2滴指示剂,用0.150 mol·L-1NaOH标准溶液滴定,进行三次平行实验,平均消耗NaOH标准溶液的体积为20.00mL。滴定时所选用的指示剂为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】铝氢化钠 是有机合成的重要还原剂,其合成线路如图所示。
是有机合成的重要还原剂,其合成线路如图所示。 。
。___________  。
。
②装置 中应盛装的试剂是
中应盛装的试剂是___________ ,装置 的作用是
的作用是___________ 。
③装置 中发生反应的离子方程式为
中发生反应的离子方程式为___________ 。
(2)测定铝氢化钠样品纯度。
① 遇水反应生成氢气的化学方程式为
遇水反应生成氢气的化学方程式为___________ 。
②现设计如图四种装置测定铝氢化钠样品的纯度(假设杂质不参与反应)。___________ (填编号)。
③取样品 ,若实验测得氢气的体积为
,若实验测得氢气的体积为 (标准状况),则铝氢化钠样品纯度为
(标准状况),则铝氢化钠样品纯度为___________ (用代数式表示)。
 是有机合成的重要还原剂,其合成线路如图所示。
是有机合成的重要还原剂,其合成线路如图所示。
 。
。
 。
。②装置
 中应盛装的试剂是
中应盛装的试剂是 的作用是
的作用是③装置
 中发生反应的离子方程式为
中发生反应的离子方程式为(2)测定铝氢化钠样品纯度。
①
 遇水反应生成氢气的化学方程式为
遇水反应生成氢气的化学方程式为②现设计如图四种装置测定铝氢化钠样品的纯度(假设杂质不参与反应)。

③取样品
 ,若实验测得氢气的体积为
,若实验测得氢气的体积为 (标准状况),则铝氢化钠样品纯度为
(标准状况),则铝氢化钠样品纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
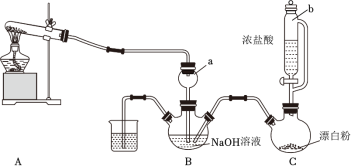
【推荐2】实验室模拟拉希法用氨气和次氯酸钠反应制备肼(N2H4),并探究肼的性质。制备装置如图所示。
已知:硫酸肼为无色无味鳞状结晶或斜方结晶,微溶于冷水,易溶于热水。
回答下列问题:
(1)装置C中仪器b的名称是_____ 。
(2)装置A试管中发生反应的化学方程式为_____ 。
(3)装置B中制备肼反应的离子方程式为_____ 。
(4)上述装置存在一处缺陷,会导致肼的产率降低,改进方法是_____ 。
(5)①探究性质。取装置B中溶液,加入适量稀硫酸振荡,置于冰水浴冷却,容器底部有无色晶体析出。过滤后用_____ 洗涤,洗涤是否完成,可通过检测洗出液中是否存在 来判断。检测的方法是
来判断。检测的方法是_____ 。
②测定产品中肼的质量分数。称取mg装置B中溶液,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成100mL溶液,移取25.00mL置于锥形瓶中,用cmol/L的碘溶液滴定,滴定过程中有无色无味无毒气体产生。终点消耗标准溶液VmL,产品中肼的质量分数表达式为_____ 。
已知:硫酸肼为无色无味鳞状结晶或斜方结晶,微溶于冷水,易溶于热水。

回答下列问题:
(1)装置C中仪器b的名称是
(2)装置A试管中发生反应的化学方程式为
(3)装置B中制备肼反应的离子方程式为
(4)上述装置存在一处缺陷,会导致肼的产率降低,改进方法是
(5)①探究性质。取装置B中溶液,加入适量稀硫酸振荡,置于冰水浴冷却,容器底部有无色晶体析出。过滤后用
 来判断。检测的方法是
来判断。检测的方法是②测定产品中肼的质量分数。称取mg装置B中溶液,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成100mL溶液,移取25.00mL置于锥形瓶中,用cmol/L的碘溶液滴定,滴定过程中有无色无味无毒气体产生。终点消耗标准溶液VmL,产品中肼的质量分数表达式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
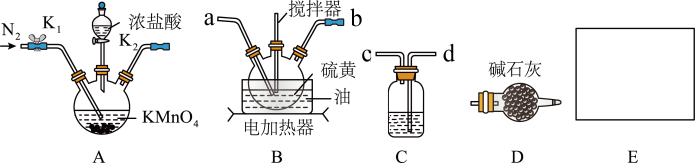
【推荐3】二氯化二硫( )常用作橡胶硫化剂。实验室利用硫与少量氯气反应制得
)常用作橡胶硫化剂。实验室利用硫与少量氯气反应制得 粗品,并测量粗品纯度的装置及操作如下:
粗品,并测量粗品纯度的装置及操作如下:
已知:
① ,
,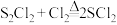 ;
;
② 易挥发,遇水可剧烈水解的,反应为
易挥发,遇水可剧烈水解的,反应为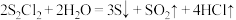 ;
;
③相关物质的熔、沸点见下表。
回答下列问题:
(1)将装置按A→______ (按气流方向,用装置B、C的小写字母表示)→E→D顺序进行连接。其中装置C中的试剂为______ ;装置D的作用是______ ;装置E为收集装置,下列仪器用于组装装置E的有______ (填序号)。组装完毕后,称量E装置的质量为 g。
g。
(2)制备 的操作为:①检查装置气密性,向A、B中放入药品,通氮气;②加热B中三颈烧瓶至115℃~125℃,使A产生氯气通入B;③……;④停止通氯气,改通氮气至装置B电加热器逐渐降温至冷却。
的操作为:①检查装置气密性,向A、B中放入药品,通氮气;②加热B中三颈烧瓶至115℃~125℃,使A产生氯气通入B;③……;④停止通氯气,改通氮气至装置B电加热器逐渐降温至冷却。
操作①通氮气的目的是_________ ;操作②反应过程应控制 的量,原因是
的量,原因是______________ ;操作③是______ 。
(3)制备完毕后,进行纯度的测定,此时称量E装置的质量为 。取出
。取出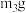 产品后,利用剩余产品进行如下实验:
产品后,利用剩余产品进行如下实验:
I.配制500mL 盐酸标准溶液。需用量筒量取
盐酸标准溶液。需用量筒量取______ mL 浓盐酸进行配制。
浓盐酸进行配制。
II.将E装置取下,接一个盛有足量NaOH溶液的C;
III.向E中通入足量的水蒸气,充分反应后再通入一段时间的水蒸气;
IV.实验结束后,取下C,加入几滴酚酞,用 盐酸标准溶液滴定剩余的NaOH溶液,消耗盐酸
盐酸标准溶液滴定剩余的NaOH溶液,消耗盐酸 ;
;
V.不加样品做空白对照实验,消耗盐酸 。
。
产品中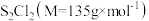 的纯度表达式为
的纯度表达式为______ %;下列操作可能会导致测定结果偏高的是______ (填标号)。
A.水蒸气的通入时间较短
B.操作I定容时仰视刻度线
C.操作IV滴定后仰视滴定管读数
D.操作V滴定前滴定管尖嘴处有气泡,滴定后消失
 )常用作橡胶硫化剂。实验室利用硫与少量氯气反应制得
)常用作橡胶硫化剂。实验室利用硫与少量氯气反应制得 粗品,并测量粗品纯度的装置及操作如下:
粗品,并测量粗品纯度的装置及操作如下:
已知:
①
 ,
,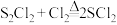 ;
;②
 易挥发,遇水可剧烈水解的,反应为
易挥发,遇水可剧烈水解的,反应为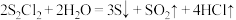 ;
;③相关物质的熔、沸点见下表。
物质 | S |
|
|
熔点/℃ | 112.8 |
|
|
沸点/℃ | 444.6 | 137 | 59.6 |
(1)将装置按A→
 g。
g。
(2)制备
 的操作为:①检查装置气密性,向A、B中放入药品,通氮气;②加热B中三颈烧瓶至115℃~125℃,使A产生氯气通入B;③……;④停止通氯气,改通氮气至装置B电加热器逐渐降温至冷却。
的操作为:①检查装置气密性,向A、B中放入药品,通氮气;②加热B中三颈烧瓶至115℃~125℃,使A产生氯气通入B;③……;④停止通氯气,改通氮气至装置B电加热器逐渐降温至冷却。操作①通氮气的目的是
 的量,原因是
的量,原因是(3)制备完毕后,进行纯度的测定,此时称量E装置的质量为
 。取出
。取出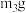 产品后,利用剩余产品进行如下实验:
产品后,利用剩余产品进行如下实验:I.配制500mL
 盐酸标准溶液。需用量筒量取
盐酸标准溶液。需用量筒量取 浓盐酸进行配制。
浓盐酸进行配制。II.将E装置取下,接一个盛有足量NaOH溶液的C;
III.向E中通入足量的水蒸气,充分反应后再通入一段时间的水蒸气;
IV.实验结束后,取下C,加入几滴酚酞,用
 盐酸标准溶液滴定剩余的NaOH溶液,消耗盐酸
盐酸标准溶液滴定剩余的NaOH溶液,消耗盐酸 ;
;V.不加样品做空白对照实验,消耗盐酸
 。
。产品中
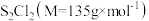 的纯度表达式为
的纯度表达式为A.水蒸气的通入时间较短
B.操作I定容时仰视刻度线
C.操作IV滴定后仰视滴定管读数
D.操作V滴定前滴定管尖嘴处有气泡,滴定后消失
您最近一年使用:0次