将铁粉、铜粉、FeCl3溶液、FeCl2溶液和CuCl2溶液混合于某容器中充分反应(容器不参与反应),试判断下列情况溶液中存在的金属离子和金属单质。
(1)若铁粉有剩余,则容器不可能有__ 。
(2)若CuCl2有剩余,则容器中一定有__ ,可能有__ 。
(3)若FeCl3和CuCl2都有剩余,则容器中不可能有__ ,一定有__ 。
(4)FeCl3和Fe粉反应时,氧化产物与还原产物的物质的量之比为__ 。
(1)若铁粉有剩余,则容器不可能有
(2)若CuCl2有剩余,则容器中一定有
(3)若FeCl3和CuCl2都有剩余,则容器中不可能有
(4)FeCl3和Fe粉反应时,氧化产物与还原产物的物质的量之比为
更新时间:2020-09-14 09:23:10
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】依据如图中氮元素及其化合物的转化关系,回答问题:_______ 。
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为:_______ 。
②下列试剂用于干燥NH3的是_______ (填字母)。
A.浓硫酸 B.碱石灰 C.氯化钙固体
③氨气是重要的化工原料,可用于工业制硝酸,写出氨气催化氧化的化学方程式:_______ 。
(3)回答下列关于NO、NO2的问题:
①汽车尾气中的CO、NOx在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO2被CO还原的化学方程式:_______ 。
②用氨可将氮氧化物转化为无毒气体。如 ,该反应中,被氧化的物质是
,该反应中,被氧化的物质是_______ (填化学式),若反应中生成1molN2,则转移电子_______ mol。
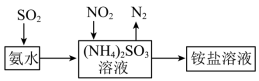
(4)工业生产中利用氨水吸收SO2和NO2,原理如图所示:_______ 。
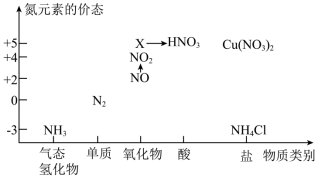
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为:
②下列试剂用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.氯化钙固体
③氨气是重要的化工原料,可用于工业制硝酸,写出氨气催化氧化的化学方程式:
(3)回答下列关于NO、NO2的问题:
①汽车尾气中的CO、NOx在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO2被CO还原的化学方程式:
②用氨可将氮氧化物转化为无毒气体。如
 ,该反应中,被氧化的物质是
,该反应中,被氧化的物质是(4)工业生产中利用氨水吸收SO2和NO2,原理如图所示:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。
(1)生活中常用的“84”消毒液与洁厕净(主要成分是盐酸)混合时会产生大量的有毒气体,写出该反应的离子方程式:_______ 。
(2)苹果汁是人们喜欢的饮料。由于此饮料中含有 ,现榨的会由淡绿色(含
,现榨的会由淡绿色(含 )变为棕黄色(含
)变为棕黄色(含 )。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有_______。
)。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有_______。
(3)焊接铜器时,可用 除去表面的
除去表面的 再进行焊接,该反应是:
再进行焊接,该反应是: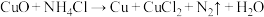
①配平该反应方程式_______ 。
②该反应的氧化产物是_______ 。氧化剂和还原剂的个数比是_______ 。
(4)一定条件下,分别以 、
、 、
、 为原料制取
为原料制取 ,当制得相同质量的
,当制得相同质量的 时,三个反应中转移的电子数目之比为
时,三个反应中转移的电子数目之比为_______ 。
(1)生活中常用的“84”消毒液与洁厕净(主要成分是盐酸)混合时会产生大量的有毒气体,写出该反应的离子方程式:
(2)苹果汁是人们喜欢的饮料。由于此饮料中含有
 ,现榨的会由淡绿色(含
,现榨的会由淡绿色(含 )变为棕黄色(含
)变为棕黄色(含 )。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有_______。
)。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有_______。| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
 除去表面的
除去表面的 再进行焊接,该反应是:
再进行焊接,该反应是: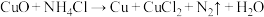
①配平该反应方程式
②该反应的氧化产物是
(4)一定条件下,分别以
 、
、 、
、 为原料制取
为原料制取 ,当制得相同质量的
,当制得相同质量的 时,三个反应中转移的电子数目之比为
时,三个反应中转移的电子数目之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】将Fe粉、Cu粉、FeCl3溶液、FeCl2和CuCl2溶液,混合于某容器中充分反应(假定容器不参与反应),试判断下列情况下溶液中存在的金属离子和金属单质。
(1)若铁粉有剩余,则容器中不可能_______________________ ;
(2)若氯化铜有剩余,则容器中还可能有____________________________ ;
(3)若氯化铁和氯化铜都有剩余,则容器中不可能有_____________ , 可能有______________ 。
(4)若氯化铁有剩余,则容器中不可能有__________________ 。
(1)若铁粉有剩余,则容器中不可能
(2)若氯化铜有剩余,则容器中还可能有
(3)若氯化铁和氯化铜都有剩余,则容器中不可能有
(4)若氯化铁有剩余,则容器中不可能有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题
(1)在一定量的稀 中慢慢加入铁粉,得到的
中慢慢加入铁粉,得到的 的物质的量(纵坐标)与所加铁粉的物质的量(横坐标)的关系如图所示。
的物质的量(纵坐标)与所加铁粉的物质的量(横坐标)的关系如图所示。
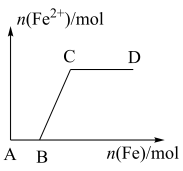
请将正确答案的序号填在相应的横线上。
①Fe3+②Fe2+③Fe、Fe2+ ④Fe2+、Fe3+
i.AB段铁元素以_________ 形式存在。
ii.BC段铁元素以_________ 形式存在
iii.CD段铁元素以__________ 形式存在。
(2)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:__________________ 。
(1)在一定量的稀
 中慢慢加入铁粉,得到的
中慢慢加入铁粉,得到的 的物质的量(纵坐标)与所加铁粉的物质的量(横坐标)的关系如图所示。
的物质的量(纵坐标)与所加铁粉的物质的量(横坐标)的关系如图所示。
请将正确答案的序号填在相应的横线上。
①Fe3+②Fe2+③Fe、Fe2+ ④Fe2+、Fe3+
i.AB段铁元素以
ii.BC段铁元素以
iii.CD段铁元素以
(2)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】向FeCl3溶液中加入a g铜粉,搅拌全部溶解,然后再向其中加入b g铁粉,经充分反应后得滤渣c g,若已知a>b>c,则推断c g滤渣是_________ ,滤液中存在的阳离子是_________ (填化学式).
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】除去括号中的杂质,填写涉及的反应方程式。
| 编号 | 混合物 | 方程式 |
| ① | 溶液: | |
| ② | 固体: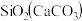 | |
| ③ | 气体: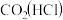 | |
| ④ | 固体: |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
(1)所含铁元素既有氧化性又有还原性的物质是________(用字母代号填)。
(2)向沸水中逐滴滴加1 mol/L FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是________ nm。
(3)电子工业需要用30 %的FeCl3溶液腐蚀敷在绝缘板上的铜片制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式_____________________ 。某同学对FeCl3腐蚀铜后所得溶液的组成进行测定:取少量待测溶液,滴入KSCN溶液呈红色,则溶液中所含金属阳离子有___________ 。
(4)若要验证该溶液中含有Fe2+,正确的实验方法是___________ (用字母代号填)。
A.向试管中加入试液,滴入KSCN溶液,若显血红色,证明含有Fe2+
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+
(5)欲从废液中回收铜,并重新获得FeCl3溶液设计实验方案如下:
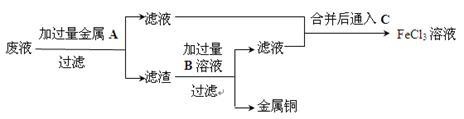
①写出上述实验中有关物质的化学式:A:_____________ ;B:_____________ 。
②写出通入C的化学方程式__________________________________ 。
(1)所含铁元素既有氧化性又有还原性的物质是________(用字母代号填)。
| A.Fe | B.FeCl3 | C.FeSO4 | D.Fe2O3 |
(3)电子工业需要用30 %的FeCl3溶液腐蚀敷在绝缘板上的铜片制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式
(4)若要验证该溶液中含有Fe2+,正确的实验方法是
A.向试管中加入试液,滴入KSCN溶液,若显血红色,证明含有Fe2+
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+
(5)欲从废液中回收铜,并重新获得FeCl3溶液设计实验方案如下:

①写出上述实验中有关物质的化学式:A:
②写出通入C的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6mol电子时,所得还原产物的物质的量为___________ mol。
(2)用铝粉和 做铝热反应实验,需要的试剂还有
做铝热反应实验,需要的试剂还有___________ (填序号)。
a.KCl b.KClO3 c. d.Mg
d.Mg
取少量铝热反应所得的固体混合物,将其溶于足量稀 ,滴加KSCN溶液无明显现象,
,滴加KSCN溶液无明显现象,______ (填“能”或“不能”)说明固体混合物中无 ,理由是
,理由是_________ (用离子方程式说明)。
(2)用铝粉和
 做铝热反应实验,需要的试剂还有
做铝热反应实验,需要的试剂还有a.KCl b.KClO3 c.
 d.Mg
d.Mg取少量铝热反应所得的固体混合物,将其溶于足量稀
 ,滴加KSCN溶液无明显现象,
,滴加KSCN溶液无明显现象, ,理由是
,理由是
您最近一年使用:0次

 的电子式
的电子式 溶液反应的化学方程式
溶液反应的化学方程式 溶液的电离方程式
溶液的电离方程式 可制备金属钠,其反应方程式为
可制备金属钠,其反应方程式为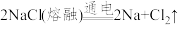 ,请用双线桥标出该反应电子转移的方向和数目
,请用双线桥标出该反应电子转移的方向和数目

