Ⅰ.工业上以铝土矿(主要成分Al2O3·3H2O)为原料生产铝,主要过程如下图所示:
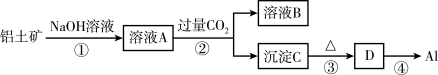
(1)反应①的化学方程式是________________________________ 。
(2)反应②的离子方程式是________________________________ 。
(3)反应④的化学方程式是________________________________ 。
(4)在上述四步转化过程中,消耗能量最多的是________ (填序号)。
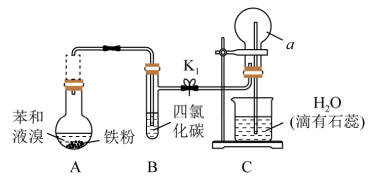
Ⅱ.某课外小组同学设计了如图所示装置(夹持、加热仪器省略)进行系列实验。请根据下列实验回答问题:
(1)甲同学用此装置验证物质的氧化性:KMnO4>Cl2>Br2,则a中加浓盐酸,b中加KMnO4,c中加_______ 溶液。将浓盐酸滴入b中后,发生反应的化学方程式是______________________________ ;b中反应结束后再向c中加入少量CCl4,振荡静置后观察到c中的现象为____________________________ 。
(2)乙同学用此装置制少量溴苯,a中盛液溴,b中为铁屑和苯,c中盛水。将液溴滴入b中后,发生反应的化学方程式是:____________ ,________________________ 。向c中滴加AgNO3溶液,可观察到的现象是________________ 。

(1)反应①的化学方程式是
(2)反应②的离子方程式是
(3)反应④的化学方程式是
(4)在上述四步转化过程中,消耗能量最多的是
Ⅱ.某课外小组同学设计了如图所示装置(夹持、加热仪器省略)进行系列实验。请根据下列实验回答问题:

(1)甲同学用此装置验证物质的氧化性:KMnO4>Cl2>Br2,则a中加浓盐酸,b中加KMnO4,c中加
(2)乙同学用此装置制少量溴苯,a中盛液溴,b中为铁屑和苯,c中盛水。将液溴滴入b中后,发生反应的化学方程式是:
更新时间:2020-09-18 17:17:22
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
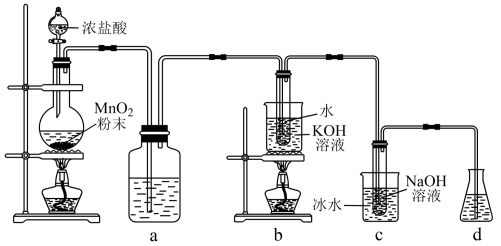
【推荐1】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。
回答下列问题:
(1)盛放 粉末的仪器名称是
粉末的仪器名称是___________ 。
(2)c中化学反应的离子方程式是___________ 。
(3)d的作用是___________ ,可选用试剂___________ (填标号)。
A.NaOH B.NaCl C. D.
D.
(4)实验室也可用高锰酸钾与浓盐酸反应制取
①写出上述方法制取 的化学方程式
的化学方程式___________
②在反应后的溶液中加入 (不溶于冷水),溶液又变为紫红色,
(不溶于冷水),溶液又变为紫红色, 反应后变为无色的
反应后变为无色的 。写出该实验中涉及反应的离子方程式
。写出该实验中涉及反应的离子方程式___________ ,该反应的发生说明还原性
___________  (填>,<或=)
(填>,<或=)
 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。
回答下列问题:
(1)盛放
 粉末的仪器名称是
粉末的仪器名称是(2)c中化学反应的离子方程式是
(3)d的作用是
A.NaOH B.NaCl C.
 D.
D.
(4)实验室也可用高锰酸钾与浓盐酸反应制取

①写出上述方法制取
 的化学方程式
的化学方程式②在反应后的溶液中加入
 (不溶于冷水),溶液又变为紫红色,
(不溶于冷水),溶液又变为紫红色, 反应后变为无色的
反应后变为无色的 。写出该实验中涉及反应的离子方程式
。写出该实验中涉及反应的离子方程式
 (填>,<或=)
(填>,<或=)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】FeBr2是一种黄绿色固体,某学习小组制备并探究它的还原性。
I.制备FeBr2固体
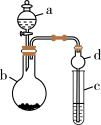
实验室用如图所示装置制取溴化亚铁。其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两个耐高温的瓷皿,其中盛有细铁粉。
实验开始时,先将干燥、纯净的CO2气流通入D中,再将铁粉加热至600-700℃,E管中铁粉开始反应。不断将d中液溴滴入温度为100-120℃的D中,经过一段时间的连续反应,在不锈钢管内产生黄绿色鳞片状溴化亚铁。
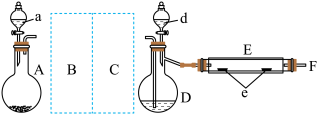
(1)若在A中盛固体CaCO3,a中盛有6mol/L的盐酸。为使导入D中的CO2为干燥纯净的气体,图中C处的洗气瓶中装有浓硫酸,则B中为___ ,若进入E装置中的CO2未干燥,则可能发生的副反应的化学方程式为___ 。
(2)E管中的反应开始前通入CO2的主要作用是___ ;E管中的反应开始后持续通入CO2的主要作用是___ 。
II.探究FeBr2的还原性
(3)现实验需要90mL0.2mol/LFeBr2溶液,取上述反应制得的FeBr2固体配制该溶液,所需仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需要的玻璃仪器是___ 。
(4)已知:Cl2的CCl4溶液呈黄绿色,Br2的CCl4溶液呈橙红色。Cl2既能氧化Br-,也能氧化Fe2+。取10mL上述FeBr2溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为血红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。以上实验结论表明还原性:Fe2+___ Br-(填“>”或“<”)。
(5)若向30mL步骤(3)的FeBr2溶液中通入标准状况下179.2mL的Cl2,取少量反应后的溶液加入CCl4,振荡后下层液体呈___ 色,写出该反应的离子方程式___ 。
I.制备FeBr2固体
实验室用如图所示装置制取溴化亚铁。其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管,e是两个耐高温的瓷皿,其中盛有细铁粉。
实验开始时,先将干燥、纯净的CO2气流通入D中,再将铁粉加热至600-700℃,E管中铁粉开始反应。不断将d中液溴滴入温度为100-120℃的D中,经过一段时间的连续反应,在不锈钢管内产生黄绿色鳞片状溴化亚铁。

(1)若在A中盛固体CaCO3,a中盛有6mol/L的盐酸。为使导入D中的CO2为干燥纯净的气体,图中C处的洗气瓶中装有浓硫酸,则B中为
(2)E管中的反应开始前通入CO2的主要作用是
II.探究FeBr2的还原性
(3)现实验需要90mL0.2mol/LFeBr2溶液,取上述反应制得的FeBr2固体配制该溶液,所需仪器除烧杯、量筒、玻璃棒、胶头滴管外,还需要的玻璃仪器是
(4)已知:Cl2的CCl4溶液呈黄绿色,Br2的CCl4溶液呈橙红色。Cl2既能氧化Br-,也能氧化Fe2+。取10mL上述FeBr2溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为血红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。以上实验结论表明还原性:Fe2+
(5)若向30mL步骤(3)的FeBr2溶液中通入标准状况下179.2mL的Cl2,取少量反应后的溶液加入CCl4,振荡后下层液体呈
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】为验证卤素单质Cl2、Br2、I2氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
已知:稀溴水的颜色是黄色,浓溴水的颜色为红棕色。
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体对应的化学方程式是___________ 。
(2)B中溶液发生反应的离子方程式是___________ 。
(3)浸有NaOH溶液的棉花的作用是___________ ,反应的离子方程式为:___________ 。
(4)过程Ⅲ实验的目的是___________ 。
(5)为验证溴的氧化性强于碘,过程Ⅳ的操作是___________ ,现象是___________ 。
(6)结合元素周期律推断氯、溴、碘三种元素最高价氧化物对应水化物的酸性由强到弱的顺序是___________ (填化学式)。
已知:稀溴水的颜色是黄色,浓溴水的颜色为红棕色。
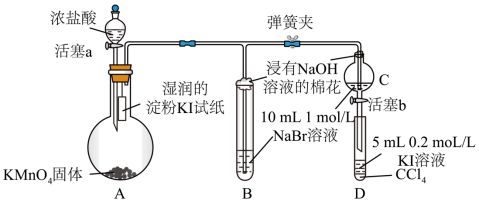
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体对应的化学方程式是
(2)B中溶液发生反应的离子方程式是
(3)浸有NaOH溶液的棉花的作用是
(4)过程Ⅲ实验的目的是
(5)为验证溴的氧化性强于碘,过程Ⅳ的操作是
(6)结合元素周期律推断氯、溴、碘三种元素最高价氧化物对应水化物的酸性由强到弱的顺序是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】Ⅰ.铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:

(1)沉淀A的成分是(填化学式)_________ 。
(2)步骤②中加入过量NaOH溶液发生反应的离子方程式,除了H+ + OH﹣= H2O外,还有:_____________________________ 、________________________________ ;
(3)步骤③中加入(或通入)的过量试剂b的结构式是______________ 。
Ⅱ. 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:

(4)从硫元素化合价的角度分析,图中只具有还原性的化合物有______________ (填化学式)。
(5)将X与Y混合,可生成淡黄色固体,该反应的化学方程式为_________________________ 。
(6)Na2S2O3是重要的化工原料,从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是______ (填代号).
a.Na2S + S b.SO2 + Na2SO4 c.Na2SO3 + S d.Na2SO3 + Na2SO4

(1)沉淀A的成分是(填化学式)
(2)步骤②中加入过量NaOH溶液发生反应的离子方程式,除了H+ + OH﹣= H2O外,还有:
(3)步骤③中加入(或通入)的过量试剂b的结构式是
Ⅱ. 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:

(4)从硫元素化合价的角度分析,图中只具有还原性的化合物有
(5)将X与Y混合,可生成淡黄色固体,该反应的化学方程式为
(6)Na2S2O3是重要的化工原料,从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是
a.Na2S + S b.SO2 + Na2SO4 c.Na2SO3 + S d.Na2SO3 + Na2SO4
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
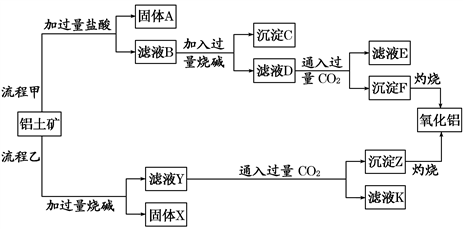
(1)写出流程甲加入盐酸后生成Al3+的离子方程式:______ 。
(2)写出流程乙加入烧碱后生成SiO 的离子方程式:
的离子方程式:______ 。
(3)为了验证滤液B中含Fe3+,可取少量滤液并加入______ (填试剂名称)。
(4)滤液E 、K中溶质的主要成分是______ (填化学式),写出该溶液的一种用途:______ 。

(1)写出流程甲加入盐酸后生成Al3+的离子方程式:
(2)写出流程乙加入烧碱后生成SiO
 的离子方程式:
的离子方程式:(3)为了验证滤液B中含Fe3+,可取少量滤液并加入
(4)滤液E 、K中溶质的主要成分是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】从铝土矿中提取铝的工艺流程如下图所示,回答下列问题:
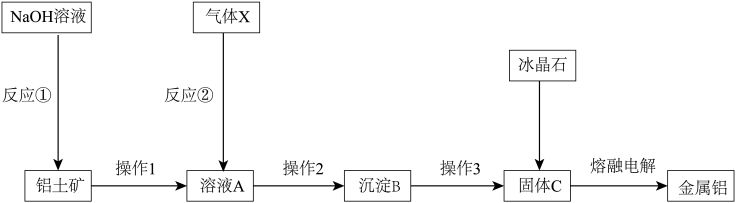
(1)气体X是___________ (填化学式)。
(2)操作1和操作2都是_____________________________ 。
(3)冰晶石的作用是_____________________________ 。
(4)写出反应①、反应②的离子方程式:①__________________________________________ ;②___________________________________________ 。

(1)气体X是
(2)操作1和操作2都是
(3)冰晶石的作用是
(4)写出反应①、反应②的离子方程式:①
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:按下列合成步骤回答问题:
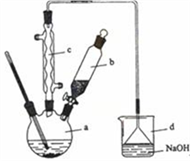
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了_____ 气体。继续滴加至液溴滴完。装置d的作用是________ ;制取溴苯的化学方程式____________________________ 。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是:______ 。
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_____ ;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为_______________ ,要进一步提纯,下列操作中必须的是_________ (填入正确选项前的字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)取反应后烧杯中的溶液2 mL加入足量的稀硝酸酸化,再滴入AgNO3溶液,有浅黄色沉淀生成___ (能或不能)证明苯与液溴反生了取代反应,为什么? _______________________ 。

| 苯 | 溴 | 溴苯 | |
| 密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/°C | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是:
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)取反应后烧杯中的溶液2 mL加入足量的稀硝酸酸化,再滴入AgNO3溶液,有浅黄色沉淀生成
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】苯和溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑。填写下列空白:
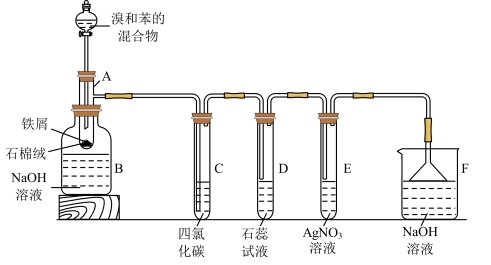
(1)试管A中的有机反应方程式为___ 。
(2)试管C中四氯化碳的作用是:___ 。反应开始后,观察D试管,看到的现象为:___ 。
(3)反应2~3min后,在B中的NaOH溶液里可观察到的现象是___ 。

(1)试管A中的有机反应方程式为
(2)试管C中四氯化碳的作用是:
(3)反应2~3min后,在B中的NaOH溶液里可观察到的现象是
您最近一年使用:0次

 。
。