化学反应 N2(g)+
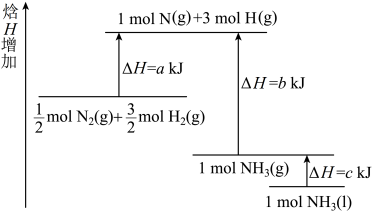
N2(g)+ H2(g)===NH3(l)的能量变化如图所示,则该反应的ΔH等于
H2(g)===NH3(l)的能量变化如图所示,则该反应的ΔH等于
 N2(g)+
N2(g)+ H2(g)===NH3(l)的能量变化如图所示,则该反应的ΔH等于
H2(g)===NH3(l)的能量变化如图所示,则该反应的ΔH等于
| A.+(a-b-c) kJ·mol-1 | B.+(b-a) kJ·mol-1 | C.+ (b+c-a) kJ·mol-1 (b+c-a) kJ·mol-1 | D.+ (a+b) kJ·mol-1 (a+b) kJ·mol-1 |
20-21高二·全国·课时练习 查看更多[3]
(已下线)第01章 化学反应的热效应(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)山东省临沂市沂水一中2020-2021学年高二9月月考化学试题云南省曲靖市罗平县第五中学2021-2022学年高二上学期期末考试化学试题
更新时间:2020-09-20 16:21:27
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】已知C(s,石墨)=C(s,金刚石) ∆H>0,下列判断正确的是
| A.此反应为放热反应 |
| B.断裂1mol石墨的化学键需要吸收的能量小于生成1mol金刚石化学键所放出的能量 |
| C.石墨比金刚石稳定 |
| D.此变化为物理变化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在发生化学变化时,下述物质的有关量在反应前后一定不发生变化的是
①质子总数;②原子总数;③分子总数;④总质量;⑤总能量;⑥共价键总数;⑦总键能
①质子总数;②原子总数;③分子总数;④总质量;⑤总能量;⑥共价键总数;⑦总键能
| A.②④⑤ | B.①②⑦ | C.②③⑥ | D.①②④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知:H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1,根据反应过程的能量变化示意图判断,下列说法正确的是


| A.1molCO和1molH2O完全反应吸热41kJ |
| B.使用催化剂使反应历程改变,能量变化曲线可能为① |
| C.升高温度,CO2(g)+H2(g)⇌CO(g)+H2O(g)的平衡常数减小 |
| D.CO2(g)+H2(g)⇌CO(g)+H2O(l)是放热反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】根据能量示意图,下列判断正确的是
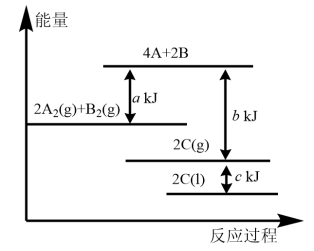

| A.化学反应中断键要放出能量,形成化学键要吸收能量 |
| B.该反应的反应物总能量小于生成物总能量 |
| C.2A2(g)+B2(g)= 2C(g)ΔH=-(b+c-a)kJ·mol-1 |
D.由图可知,生成1 mol C(l),放出 (b+c-a)kJ热量 (b+c-a)kJ热量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】甲醇是一种重要的化工原料,广泛应用于化工生产,也可以直接用作燃料。已知:
CH3OH(1)+O2(g)=CO(g)+2H2O(g) ΔH1=﹣443.64kJ•mol﹣1
2CO(g)+O2(g)=2CO2(g) ΔH2=﹣566.0kJ•mol﹣1
下列说法或热化学方程式正确的是
CH3OH(1)+O2(g)=CO(g)+2H2O(g) ΔH1=﹣443.64kJ•mol﹣1
2CO(g)+O2(g)=2CO2(g) ΔH2=﹣566.0kJ•mol﹣1
下列说法或热化学方程式正确的是
| A.CO的燃烧热为﹣566.0kJ•mol﹣1 |
| B.2molCO和1molO2的总能量比2molCO2的总能量低 |
| C.完全燃烧20g甲醇,生成二氧化碳和水蒸气时放出的热量为908.3kJ |
| D.2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g) ΔH=﹣1453.28kJ•mol﹣1 |
您最近一年使用:0次
【推荐2】以太阳能为热源分解 ,经热化学铁氧化合物循环分解水制
,经热化学铁氧化合物循环分解水制 的过程如图所示。下列叙述正确的是
的过程如图所示。下列叙述正确的是

 ,经热化学铁氧化合物循环分解水制
,经热化学铁氧化合物循环分解水制 的过程如图所示。下列叙述正确的是
的过程如图所示。下列叙述正确的是
A.过程中 是中间产物 是中间产物 |
B.该过程的热化学方程式可以表示为: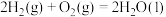  |
C.过程II中3  的总能量高于1 的总能量高于1  |
D.铁氧化合物循环制 具有节约能源、产物易分离等优点 具有节约能源、产物易分离等优点 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】已知:2H2(g)+O2(g)=2H2O(g) △H1= -483.6kJ·mol-1
2H2(g)+O2(g)=2H2O⑴△H2=-571.6kJ·mol-1;据此判断,下列说法正确的是
2H2(g)+O2(g)=2H2O⑴△H2=-571.6kJ·mol-1;据此判断,下列说法正确的是
| A.2H2O(l)=2H2(g)+O2(g) △H3=+XkJ·mol-1,X小于571.6 |
| B.2mol氢气和lmol氧气的能量大于2mol液态水的能量 |
| C.1 mol H2O(1)转变成1 mol H2O(g)放出44.0 kJ热量 |
| D.1mol H2O(g)转变成1 mol H2O(1)放出88.0 kJ热量 |
您最近一年使用:0次



