N2H4是一种高效清洁的火箭燃料。0.25molN2H4(g)完全燃烧生成氮气和气态水时,放出133.5kJ热量。则下列热化学方程式中正确的是( )
| A.N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=+267kJ·mol-1 |
| B.N2H4(g)+O2(g)=N2(g)+2H2O(l) △H=-534kJ·mol-1 |
| C.N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-133.5kJ·mol-1 |
| D.N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534kJ·mol-1 |
20-21高二上·广西梧州·阶段练习 查看更多[9]
宁夏六盘山高级中学2023-2024学年高二上学期第一次月考化学试题河南省鹤壁市淇滨高级中学2021-2022学年高二下学期开学考试化学试题甘肃省甘南藏族自治州舟曲县第一中学2021-2022学年高二上学期期中考试化学试题黑龙江省齐齐哈尔市恒昌中学校2021-2022学年高二上学期期中考试化学试题河南省平顶山市郏县第一高级中学2021-2022学年高二下学期开学收心考试化学试题 湖北省罗田第一中学2021-2022学年高二10月月考化学试题(已下线)1.1.2 热化学方程式 燃烧热-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)重庆市第三十二中学2020-2021学年高二上学期期末考试化学试题广西梧州市岑溪二中2020-2021学年高二9月月考化学试题
更新时间:2020-09-27 12:05:34
|
相似题推荐
单选题
|
容易
(0.94)
解题方法
【推荐1】大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知25℃时,相关物质的燃烧热数据如下表:
则25℃时,6C(石墨,s)+3H2(g)=C6H6(l) △H=
| 物质 | H2(g) | C(石墨,s) | C6H6(l) |
| 燃烧热△H(kJ•mol-1) | -285.8 | -393.5 | -3267.5 |
| A.-30.9kJ/mol | B.+49.1kJ/mol | C.+104.7kJ/mol | D.-2588.2kJ/mol |
您最近一年使用:0次
单选题
|
容易
(0.94)
解题方法
【推荐2】在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知
 kJ·mol
kJ·mol )
)
下列说法正确的是

 kJ·mol
kJ·mol )
)| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
NH3的浓度(mol·L ) ) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 |  |  |  |
下列说法正确的是
A. | B. | C.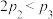 | D.α1+α2>1 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐1】已知: ①2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ/mol;②Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g) ΔH=-226 kJ/mol根据以上热化学方程式判断,下列说法正确的是
| A.CO的燃烧热为 283 kJ |
| B.反应①正反应活化能与逆反应活化能之差为+566 kJ/mol |
| C.反应 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol |
| D.CO(g)与 Na2O2(s)反应放出 509 kJ 热量时,电子转移数为 6.02×1023 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐2】已知:H2(g)+F2(g)====2HF(g) ΔH=-546.6 kJ·mol-1,下列说法中不正确的是
| A.44.8 L氟化氢气体分解成22.4 L的氢气和22.4 L的氟气吸收546.6 kJ热量 |
| B.1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量大于546.6 kJ |
| C.相同条件下,1 mol氢气与1 mol氟气的能量总和高于2 mol氟化氢气体的能量 |
| D.2 mol H—F键的键能比1 mol H—H键和1 mol F—F 键的键能之和大546.6 kJ |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐1】已知1mol下列物质完全燃烧生成稳定的产物时放出的热量如下:
则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的ΔH为( )
| 名称 | 化学式 |  H/kJ H/kJ mol-1 mol-1 |
| 一氧化碳 | CO(g) | -283.0 |
| 乙烯 | C2H4(g) | -1411.0 |
| 乙醇 | C2H5OH(l) | -1366.8 |
则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的ΔH为( )
| A.-44.2kJ·mol-1 | B.44.2kJ·mol-1 |
| C.-330kJ·mol-1 | D.330kJ·mol-1 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合制备甲醇,该反应的热化学方程式为CO(g)+2H2(g)=CH3OH(g) ΔH=-116kJ·mol-1。某些化学键的键能数据如表:
则CO中碳氧键的键能是
| 化学键 | C—H | H—H | C—O | H—O |
| 键能/kJ·mol-1 | 413 | 436 | 358 | 463 |
| A.431kJ·mol-1 | B.946kJ·mol-1 |
| C.1072kJ·mol-1 | D.1130kJ·mol-1 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐3】将TiO2转化为TiCl4是工业冶炼金属Ti的主要反应之一。已知:
TiO2(s)+2Cl2(g)=TiCl4(1)+O2(g) ∆H=+140.5kJ/mol
2CO(g)=2C(s,石墨)+O2(g) ∆H=+221.0 kJ/mol
则反应TiO2(s)+2Cl2(g)+2C(s,石墨)=TiCl4(1)+2CO(g)的∆H为
TiO2(s)+2Cl2(g)=TiCl4(1)+O2(g) ∆H=+140.5kJ/mol
2CO(g)=2C(s,石墨)+O2(g) ∆H=+221.0 kJ/mol
则反应TiO2(s)+2Cl2(g)+2C(s,石墨)=TiCl4(1)+2CO(g)的∆H为
| A.-30.0kJ/mol | B.+30.0 kJ/mol | C.-80.5kJ/mol | D.+80.5kJ/mol |
您最近一年使用:0次



